El virus de la hepatitis B ( VHB ) es un virus de ADN parcialmente bicatenario, [1] una especie del género Orthohepadnavirus y miembro de la familia de virus Hepadnaviridae . [2] [3] Este virus causa la enfermedadde la hepatitis B. [4]
El virus de la hepatitis B se clasifica en el género Orthohepadnavirus , que contiene otras 11 especies. [3] El género está clasificado como parte de la familia Hepadnaviridae , que contiene otros cuatro géneros, Avihepadnavirus , Herpetohepadnavirus , Metahepadnavirus y Parahepadnavirus . [3] Esta familia de virus es el único miembro del orden viral Blubervirales . [3] Se han encontrado virus similares a la hepatitis B en todos los simios ( orangutanes , gibones , bonobos , gorilas y chimpancés ), en monos del Viejo Mundo , [5] y en monos lanudos del Nuevo Mundo (el virus de la hepatitis B del mono lanudo ), lo que sugiere un origen antiguo de este virus en primates.
El virus se divide en cuatro serotipos principales (adr, adw, ayr, ayw) según los epítopos antigénicos presentes en las proteínas de su envoltura . Estos serotipos se basan en un determinante común (a) y dos pares de determinantes mutuamente excluyentes (d/y y w/r). Las cepas virales también se han dividido en diez genotipos (A-J) y cuarenta subgenotipos según la variación general de la secuencia de nucleótidos del genoma. [6] Los genotipos tienen una distribución geográfica distinta y se utilizan para rastrear la evolución y transmisión del virus. Las diferencias entre genotipos afectan la gravedad de la enfermedad, el curso y la probabilidad de complicaciones y la respuesta al tratamiento. [7] [8] Los serotipos y genotipos no necesariamente corresponden.
El genotipo D tiene 10 subgenotipos. [9] [6]
Se han aislado en murciélagos varias especies similares a la hepatitis B, aún no clasificadas. [10]
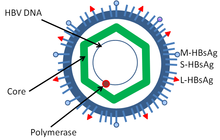
El virus de la hepatitis B es un miembro de la familia Hepadnavirus . [11] La partícula del virus, llamada partícula Dane [12] ( virión ), consta de una envoltura lipídica externa y un núcleo de nucleocápside icosaédrico compuesto de proteínas . La nucleocápside encierra el ADN viral y una ADN polimerasa que tiene actividad transcriptasa inversa similar a la de los retrovirus. [13] La envoltura exterior contiene proteínas incrustadas que participan en la unión viral y la entrada a las células susceptibles. El virus es uno de los virus animales con envoltura más pequeños con un diámetro de virión de 42 nm, pero existen formas pleomórficas , incluidos cuerpos filamentosos y esféricos que carecen de núcleo. Estas partículas no son infecciosas y están compuestas por el lípido y la proteína que forma parte de la superficie del virión, que se denomina antígeno de superficie ( HBsAg ), y se produce en exceso durante el ciclo de vida del virus. [14]
Consiste en:
El virus de la hepatitis D requiere que las partículas de la envoltura del VHB se vuelvan virulentas. [26]
La evolución temprana del VHB, como la de todos los virus, es difícil de establecer. La identificación de hepadnavirus en una amplia gama de vertebrados sugiere una larga coevolución. La identificación de elementos endógenos de hepadnaviridae compartidos por varias especies de aves muestra la presencia de estos virus en aves durante al menos 70 millones de años. [27] Aunque falta evidencia similar para los mamíferos, la posición filogenética de los ortohepadnavirus como un clado hermano de los avihepadnavirus sugiere una presencia del virus en el ancestro amniota y una coevolución posterior con aves y mamíferos después de su divergencia (hace >300 millones de años). . También se ha propuesto que un hepadnavirus de murciélago del Nuevo Mundo puede ser el origen de los hepadnavirus de primates. [28] Los avihepadnavirus carecen de la proteína X, pero hay un marco de lectura X vestigial en el genoma del hepadnavirus del pato. [29] La proteína X puede haber evolucionado a partir de una ADN glicosilasa .
Recientemente, la reconstrucción de genomas del VHB a partir de restos humanos antiguos ha permitido investigar con más detalle la evolución de este virus en humanos. [30] [31] [32] En 2021, un estudio reconstruyó 137 genomas antiguos del VHB y demostró la presencia del virus en humanos desde al menos 10.000 años. [30] El ancestro común más reciente de todos los linajes humanos conocidos de VHB data de hace entre 20.000 y 12.000 años. Sin embargo, no se puede decir si el virus ya estaba presente en los humanos mucho antes o si se había adquirido poco antes de otra especie animal. Se demostró que la evolución del VHB en humanos refleja eventos conocidos de la historia humana, como el primer poblamiento de América durante el Pleistoceno tardío y la transición neolítica en Europa. [30] Estos estudios también demostraron que algunas cepas antiguas del VHB todavía infectan a los humanos, mientras que otras se extinguieron. [30] [31] [32] Las cepas de VHB encontradas en simios africanos y del sudeste asiático ( chimpancés , gorilas , orangutanes , bonobos y gibones ) parecen estar relacionadas con cepas de VHB humanas, lo que podría reflejar eventos pasados de transmisión entre especies. [33] [30]
Un estudio de aislados de la población humana circumpolar del Ártico ha propuesto que el ancestro del subgenotipo B5 (el tipo endémico que se encuentra en esta población) es el virus ancestral que se originó en Asia hace unos 2000 años (95% HPD 900 a. C. - 830 d. C.). [34] La coalescencia se produjo alrededor del año 1000 d.C. Este subgenotipo se extendió desde Asia inicialmente hasta Groenlandia y luego se extendió hacia el oeste en los últimos 400 años.
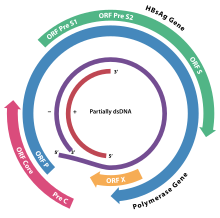
El genoma del VHB está formado por ADN circular , pero es inusual porque el ADN no es completamente bicatenario. Un extremo de la cadena de longitud completa está unido a la ADN polimerasa viral . El genoma tiene una longitud de 3020 a 3320 nucleótidos (para la cadena de longitud completa) y de 1700 a 2800 nucleótidos de longitud (para la cadena de longitud corta). [35]
La cadena de sentido negativo (no codificante) es complementaria al ARNm viral. El ADN viral se encuentra en el núcleo poco después de la infección de la célula. El ADN parcialmente bicatenario se convierte en completamente bicatenario al completar la cadena sentido (+) mediante ADN polimerasas celulares (la ADN polimerasa viral se usa para una etapa posterior) y la eliminación de la proteína polimerasa viral (P) del (- ) cadena sentido y una secuencia corta de ARN de la cadena sentido (+). Las bases no codificantes se eliminan de los extremos de la hebra sentido (-) y los extremos se vuelven a unir.
Los genes virales son transcritos por la ARN polimerasa II celular en el núcleo celular a partir de una plantilla de ADN circular cerrada covalentemente (cccDNA). En el genoma del VHB se han identificado dos potenciadores denominados potenciador I (EnhI) y potenciador II (EnhII). Ambos potenciadores exhiben una mayor actividad en células de origen hepático y juntos impulsan y regulan la expresión de los transcritos virales completos. [36] [37] [38]
Hay cuatro genes conocidos codificados por el genoma llamados C, P, S y X. La proteína central está codificada por el gen C (HBcAg) y su codón de inicio está precedido por un codón de inicio AUG en el marco aguas arriba a partir del cual se origina el codón de inicio. Se produce la proteína pre-núcleo. HBeAg se produce mediante procesamiento proteolítico de la proteína prenuclear. La ADN polimerasa está codificada por el gen P. El gen S es el gen que codifica el antígeno de superficie (HBsAg). El gen HBsAg es un marco de lectura largo y abierto , pero contiene tres codones de "inicio" (ATG) en marco que dividen el gen en tres secciones, pre-S1, pre-S2 y S. Debido a los múltiples codones de inicio, los polipéptidos de tres Se producen diferentes tamaños llamados grande (pre-S1 + pre-S2 + S), mediano (pre-S2 + S) y pequeño (S). [39]
La función de la proteína codificada por el gen X no se comprende completamente, [40] pero algunas pruebas sugieren que puede funcionar como un transactivador transcripcional. Curiosamente, una proteína de fusión X-Core de 40 kDa está codificada por una transcripción viral larga de 3,9 kb, cuya función aún no está clara. [41] La síntesis del ARN de 3,9 kb se inicia en la región promotora del gen X y el transcrito se poliadenila sólo después de la segunda ronda de transcripción. Otras especies de ARN pregenómico/pre-núcleo (pg/pc) comparten un comportamiento similar. Por tanto, la maquinaria de transcripción viral debe ignorar la señal poli(A) en la primera ronda de transcripción.
Se han identificado varios elementos de ARN no codificantes en el genoma del VHB. Estos incluyen VHB PREalfa , VHB PREbeta y señal épsilon de encapsidación de ARN del VHB . [42] [43]
Los genotipos difieren en al menos un 8% de la secuencia y tienen distribuciones geográficas distintas y esto se ha asociado con la historia antropológica. Dentro de los genotipos se han descrito subtipos: estos difieren entre un 4% y un 8% del genoma.
Hay ocho genotipos conocidos etiquetados de la A a la H. [7]
Se ha descrito un posible nuevo genotipo "I", [44] pero la aceptación de esta notación no es universal. [45]
Desde entonces se han reconocido dos genotipos más. [46] La lista actual (2014) ahora va de la A a la J. También se reconocen varios subtipos.
Hay al menos 24 subtipos.
Diferentes genotipos pueden responder al tratamiento de diferentes maneras. [47] [48]
El tipo F, que difiere de los otros genomas en un 14%, es el tipo más divergente conocido. El tipo A prevalece en Europa , África y el sudeste asiático , incluidas Filipinas . Los tipos B y C son predominantes en Asia ; el tipo D es común en la zona del Mediterráneo, Oriente Medio y la India ; el tipo E está localizado en el África subsahariana; el tipo F (o H) está restringido a Centro y Sudamérica . El tipo G se ha encontrado en Francia y Alemania . Los genotipos A, D y F son predominantes en Brasil y todos los genotipos se encuentran en los Estados Unidos con frecuencias que dependen del origen étnico.
Las cepas E y F parecen haberse originado en poblaciones aborígenes de África y el Nuevo Mundo, respectivamente.
El tipo A tiene dos subtipos: Aa (A1) en África/Asia y Filipinas y Ae (A2) en Europa/Estados Unidos.
El tipo B tiene dos distribuciones geográficas distintas: Bj/B1 ('j': Japón) y Ba/B2 ('a': Asia). El tipo Ba se ha subdividido en cuatro clados (B2-B4).
El tipo C tiene dos subtipos geográficos: Cs (C1) en el sudeste asiático y Ce (C2) en el este de Asia. Los subtipos C se han dividido en cinco clados (C1-C5). Se ha descrito un sexto clado (C6) en Filipinas, pero hasta la fecha sólo en un aislado. [49] El tipo C1 está asociado con Vietnam , Myanmar y Tailandia ; tipo C2 con Japón , Corea y China ; tipo C3 con Nueva Caledonia y Polinesia ; C4 con Australia ; y C5 con Filipinas . Otro subtipo ha sido descrito en Papua , Indonesia . [50]
El tipo D se ha dividido en 7 subtipos (D1-D7).
El tipo F se ha subdividido en 4 subtipos (F1-F4). F1 se ha dividido en 1a y 1b. En Venezuela, los subtipos F1, F2 y F3 se encuentran en los amerindios del este y del oeste. Entre los amerindios del sur sólo se encontró F3. Los subtipos Ia, III y IV exhiben una distribución geográfica restringida (Centroamérica, Norte y Sur de Sudamérica respectivamente), mientras que los clados Ib y II se encuentran en todas las Américas excepto en el norte de Sudamérica y Norteamérica respectivamente.

El ciclo de vida del virus de la hepatitis B es complejo. La hepatitis B es uno de los pocos virus no retrovirales conocidos que utilizan la transcripción inversa como parte de su proceso de replicación.
A pesar de que existe una vacuna para prevenir la hepatitis B, el VHB sigue siendo un problema de salud mundial. La hepatitis B puede ser aguda y luego crónica, dando lugar a otras enfermedades y problemas de salud. [55] Además de causar hepatitis, la infección por el VHB puede provocar cirrosis y carcinoma hepatocelular . [56]
También se ha sugerido que puede aumentar el riesgo de cáncer de páncreas . [4]
La infección viral por el virus de la hepatitis B (VHB) provoca muchos cambios en los hepatocitos debido a la acción directa de una proteína codificada por el virus, HBx , y a cambios indirectos debido a un gran aumento de especies reactivas de oxígeno (ROS) intracelulares después de la infección. HBx parece desregular varias vías celulares. HBx causa desregulación en parte al unirse al ADN genómico , cambiar los patrones de expresión de los miARN, afectar las histonas metiltransferasas, unirse a la proteína SIRT1 para activar la transcripción y cooperar con las histonas metilasas y desmetilasas para cambiar los patrones de expresión celular. [57] HBx es en parte responsable del aumento aproximado de 10.000 veces en las especies reactivas de oxígeno (ROS) intracelulares tras la infección crónica por VHB. [ cita necesaria ] El aumento de ROS puede ser causado, en parte, por la localización de HBx en las mitocondrias , donde HBx disminuye el potencial de membrana mitocondrial. [58] Además, otra proteína del VHB , el HBsAg , también aumenta las ROS a través de interacciones con el retículo endoplásmico . [58]
El aumento de ROS después de la infección por VHB provoca inflamación, lo que conduce a un aumento adicional de ROS. [ cita necesaria ] Las ROS causan más de 20 tipos de daños en el ADN. [59] El daño oxidativo del ADN es mutagénico. [60] Además, la reparación del daño del ADN puede causar alteraciones epigenéticas en el sitio del daño durante la reparación del ADN. [61] Las alteraciones y mutaciones epigenéticas pueden causar defectos en la maquinaria celular que luego contribuyen a la enfermedad hepática . Cuando los cambios epigenéticos y mutacionales acumulados eventualmente causan la progresión al cáncer , las alteraciones epigenéticas parecen tener un papel más importante en esta carcinogénesis que las mutaciones. Sólo uno o dos genes, TP53 [62] y quizás ARID1A , [63] están mutados en más del 20% de los cánceres de hígado , mientras que 41 genes tienen cada uno promotores hipermetilados (que reprimen la expresión genética ) en más del 20% de los cánceres de hígado, con siete de estos genes están hipermetilados en más del 75% de los cánceres de hígado. [62] Además de las alteraciones en los sitios de reparación del ADN , las alteraciones epigenéticas también son causadas por el HBx que recluta las enzimas ADN metiltransferasa , DNMT1 y/o DNMT3A , en loci genéticos específicos para alterar sus niveles de metilación y expresión génica. [64] HBx también altera la acetilación de histonas que pueden afectar la expresión genética. [64]
Varios miles de genes codificadores de proteínas parecen tener sitios de unión a HBx. [57] [65] Además de los genes codificantes de proteínas, alrededor de 15 microARN y 16 ARN largos no codificantes también se ven afectados por la unión de HBx a sus promotores. [65] Cada microARN alterado puede afectar la expresión de varios cientos de ARN mensajeros (ver microARN ).
El origen del virus de la hepatitis B se remonta al siglo V a. C. e incluso se menciona en tablillas de arcilla babilónicas. Hipócrates describió más tarde una epidemia de ictericia entre sus pacientes que se caracterizaba por el color amarillento de la piel y el blanco de los ojos. La ictericia es un signo clínico de infección por el virus de la hepatitis B. [66] [67] Sin embargo, debido al largo intervalo de tiempo, medido en semanas, entre la exposición al agente causal y el desarrollo de la enfermedad impidió el reconocimiento de la ictericia como una enfermedad infecciosa hasta el siglo XX. [68] Los primeros casos registrados de infección por el virus de la hepatitis B ocurrieron en 1883 después de que se administrara a un grupo de personas la vacuna contra la viruela que contenía linfa humana. [68] La vacuna contra la viruela se administró a los trabajadores de los astilleros en Alemania y los trabajadores posteriormente desarrollaron síntomas de hepatitis. [68] La hepatitis sérica, ahora conocida como hepatitis B, se observó a menudo después del uso de agujas y jeringas contaminadas. Estas agujas y jeringas contaminadas no fueron limpiadas adecuadamente y/o fueron reutilizadas entre los pacientes. [69] En 1943, la transmisión del virus de la hepatitis B a través de la sangre se enfatizó aún más cuando Paul Beeson describió la ictericia que ocurría en pacientes que acababan de recibir transfusiones de sangre. En 1942 se observó otra epidemia de ictericia entre los soldados, después de haber recibido la vacuna contra la fiebre amarilla. [69] La distinción entre el virus de la hepatitis A y el virus de la hepatitis B no se determinó hasta 1947, cuando fueron reconocidos como dos agentes filtrables diferentes a través de numerosos estudios realizados en voluntarios humanos. [69]
En 1965, se descubrió e identificó el “antígeno australiano” como el antígeno de superficie del virus de la hepatitis B, HBsAg. Este fue uno de los primeros avances en el esfuerzo por comprender la patología de la hepatitis viral que provocaba ictericia en las personas infectadas por el VHB. Permitió a los países industrializados diagnosticar de manera confiable a los portadores asintomáticos del virus de la hepatitis B y el descubrimiento brindó a los profesionales de la salud una forma de analizar la sangre para detectar la hepatitis B antes de administrar transfusiones de sangre. [69] [68]
Hoy en día, la infección por el virus de la hepatitis B se evita fácilmente recibiendo una de las vacunas contra la hepatitis B. La vacuna HepB derivada de plasma se autorizó en 1981 y posteriormente fue reemplazada en 1986 por la vacuna HepB recombinante. Engerix B se aprobó en 1989 y Heplisav-B se aprobó en 2017. [70] [71] [68] Todos los cuales brindan protección contra el VHB.
Las tasas de infección por hepatitis B son iguales entre hombres y mujeres. El virus de la hepatitis B se encuentra más prominentemente en ciudadanos estadounidenses de ascendencia asiática, isleña del Pacífico o africana y aproximadamente el 25% de estos individuos recibirán un diagnóstico. [72] El VHB se transmite más fácilmente en grupos con comportamientos de alto riesgo, como el uso de drogas intravenosas, múltiples parejas sexuales y hombres que tienen relaciones sexuales con hombres. [73]
El virus de la hepatitis B causa la enfermedad de la hepatitis B. La hepatitis se considera la principal causa de cáncer de hígado en todo el mundo (referencia). El virus de la hepatitis B se puede encontrar en casi todas las regiones del mundo, pero es más frecuente en países donde el virus es endémico. El VHB es endémico en algunos países ubicados en Asia, África, América del Sur y el Caribe. [74]
Aproximadamente dos mil millones de personas han sido infectadas con el VHB, lo que significa que casi 1 de cada 3 personas ha sido infectada. Se estima que cada año 1,5 millones de personas se infectarán y aproximadamente el 10% de esas personas no serán diagnosticadas. Cada año, se estima que 820.000 personas mueren a causa de la infección por hepatitis B y las complicaciones relacionadas con el VHB. [75]
La propagación del VHB durante el embarazo sigue siendo el mayor riesgo de desarrollar hepatitis B crónica más adelante en la niñez. Aproximadamente el 90% de los bebés infectados padecerán una infección crónica. Sólo entre el 2% y el 6% de los adultos que alguna vez se infectaron con el VHB pasarán a tener una infección crónica. [76] De los 350 millones de personas estimadas crónicamente infectadas con VHB en todo el mundo, el 50% o más de esas personas adquirieron la infección prenatalmente o durante su primera infancia. En los países donde el VHB es endémico, la transmisión vertical del VHB plantea un riesgo importante para la salud debido a que un gran número de mujeres en edad fértil tienen HBeAg positivo, lo que les permite transmitir el VHB a sus recién nacidos. En áreas donde el VHB es endémico, la transmisión no se limita a grupos con conductas de alto riesgo. En cambio, la infección puede ocurrir a través de diferentes vías de transmisión, pero principalmente durante la primera infancia. [77]
La propagación del virus de la hepatitis B en el mundo occidental se produce con mayor frecuencia a través de las relaciones sexuales o el intercambio de agujas entre usuarios de drogas intravenosas (UDV). Los IVDU muestran la tasa más alta de infección por VHB en Europa y América del Norte. [73] También hay tasas más altas de infección por hepatitis B entre hombres que tienen sexo con hombres (HSH). El riesgo de infectarse con el VHB aumenta al tener múltiples parejas sexuales. (necesita referencia)
La propagación del virus de la hepatitis B se produce con mayor frecuencia mediante transmisión vertical de madre a hijo durante el nacimiento y el parto. El VHB también se puede transmitir a través del contacto con sangre u otros fluidos corporales durante las relaciones sexuales con una pareja infectada. También se transmite a través de agujas compartidas con personas infectadas o por exposición a objetos punzantes. Las agujas de cualquier tipo pueden suponer un riesgo si no son de un solo uso o no se desinfectan adecuadamente, preferiblemente en autoclave. Esto incluye agujas utilizadas en salones de tatuajes y perforaciones corporales. [74]
Además, el virus de la hepatitis B también se puede transmitir al compartir aretes y otras joyas para perforar el cuerpo. [75] También se transmite a través de unidades de hemodiálisis que han sido utilizadas por pacientes HBeAg positivos. Debido a que las unidades de HD generalmente tratan a varios pacientes a la vez, puede ocurrir contaminación de la sangre de los pacientes. La incidencia de infección por VHB a través de unidades de HD es del 1% en los Estados Unidos. El personal sanitario también corre un mayor riesgo de infección. [78] [79] La transmisión del VHB se puede limitar administrando la vacuna contra la hepatitis B. En las zonas donde el virus es endémico, las vacunas son limitadas, especialmente en las zonas rurales donde las clínicas médicas son escasas.
Aunque el VHB puede ser infeccioso en superficies hasta por siete días, no se transmite a través de la lactancia materna, el compartir utensilios para comer, los abrazos, los besos, las manos, la tos o los estornudos. A diferencia de otros virus de la hepatitis, el VHB no se transmite a través de agua o alimentos contaminados. Sin embargo, vivir con una persona infectada con el virus de la hepatitis B aumenta el riesgo de contraer el virus. [68]
También puede producirse una coinfección por hepatitis B y otros virus. La hepatitis C , la hepatitis D (un virus satélite de la hepatitis B) y el VIH pueden coinfectar a una persona junto con el VHB.
Debido a que el VHB y el VHC comparten un modo de transmisión similar, es posible que se produzcan coinfecciones. La mayoría de los casos de coinfección por VHB y VHC se producen entre usuarios de drogas intravenosas, productos sanguíneos no analizados o exposición a agujas sucias y equipos médicos no esterilizados. La coinfección de estos dos virus puede causar una enfermedad hepática más grave y aumentar el riesgo de cáncer primario de hígado (carcinoma hepatocelular). Es posible que los informes de esta coinfección no se notifiquen debido a la capacidad de la hepatitis C de convertirse en el virus hepático dominante durante la coinfección, lo que reduce la cantidad detectable de VHB que se encuentra en el cuerpo. [80] Estadísticas recientes muestran que el 10% de todas las personas infectadas con el VIH también están infectadas con la hepatitis B. Sin embargo, esta estadística aumenta a casi el 20% en el sudeste asiático. La infección por hepatitis B es una de las principales causas de hospitalizaciones y muerte entre pacientes con VIH desde el desarrollo y uso de terapias antirretrovirales. Aquellos que están infectados con VIH y VHB tienen seis veces más probabilidades de desarrollar hepatitis B crónica. Algunos estudios sugieren que esto puede deberse a que las personas coinfectadas tienen recuentos más bajos de células T CD4+. [81]