El yodo-131 ( 131 I , I-131 ) es un importante radioisótopo de yodo descubierto por Glenn Seaborg y John Livingood en 1938 en la Universidad de California, Berkeley. [1] Tiene una vida media de desintegración radiactiva de aproximadamente ocho días. Está asociado con la energía nuclear, los procedimientos de diagnóstico y tratamiento médico y la producción de gas natural. También desempeña un papel importante como isótopo radiactivo presente en los productos de fisión nuclear y contribuyó significativamente a los riesgos para la salud derivados de las pruebas de bombas atómicas al aire libre en la década de 1950 y del desastre de Chernobyl , además de ser una gran fracción de el peligro de contaminación en las primeras semanas de la crisis nuclear de Fukushima . Esto se debe a que el 131I es un importante producto de fisión del uranio y el plutonio , y comprende casi el 3% del total de productos de fisión (en peso). Consulte el rendimiento del producto de fisión para comparar con otros productos de fisión radiactivos. El 131 I es también un importante producto de fisión del uranio-233 , producido a partir del torio .
Debido a su modo de desintegración beta , el yodo-131 provoca mutación y muerte en las células en las que penetra y en otras células que se encuentran a varios milímetros de distancia. Por esta razón, las dosis altas del isótopo son a veces menos peligrosas que las dosis bajas, ya que tienden a matar los tejidos de la tiroides que de otro modo se volverían cancerosos como resultado de la radiación. Por ejemplo, los niños tratados con dosis moderadas de 131 I para los adenomas de tiroides tuvieron un aumento detectable de cáncer de tiroides, pero los niños tratados con una dosis mucho más alta no. [2] Asimismo, la mayoría de los estudios de dosis muy altas de 131 I para el tratamiento de la enfermedad de Graves no han logrado encontrar ningún aumento en el cáncer de tiroides, a pesar de que existe un aumento lineal en el riesgo de cáncer de tiroides con la absorción de 131 I en dosis moderadas. [3] Por lo tanto, el yodo-131 se utiliza cada vez menos en pequeñas dosis en uso médico (especialmente en niños), pero cada vez más se utiliza sólo en dosis de tratamiento grandes y máximas, como una forma de matar los tejidos objetivo. Esto se conoce como "uso terapéutico".
El yodo-131 se puede "ver" mediante técnicas de imágenes de medicina nuclear (p. ej., cámaras gamma ) siempre que se administre para uso terapéutico, ya que aproximadamente el 10% de su energía y dosis de radiación provienen de radiación gamma. Sin embargo, dado que el otro 90% de la radiación (radiación beta) causa daño tisular sin contribuir a ninguna capacidad de ver o "imaginar" el isótopo, se prefieren otros radioisótopos de yodo menos dañinos, como el yodo-123 (ver isótopos de yodo ). en situaciones en las que sólo se requieren imágenes nucleares. El isótopo 131 I todavía se utiliza ocasionalmente para trabajos puramente de diagnóstico (es decir, de obtención de imágenes), debido a su bajo coste en comparación con otros radioisótopos de yodo. Dosis muy pequeñas de imágenes médicas de 131 I no han mostrado ningún aumento en el cáncer de tiroides. La disponibilidad de bajo costo del 131 I, a su vez, se debe a la relativa facilidad de crear 131 I mediante bombardeo de neutrones de teluro natural en un reactor nuclear, y luego separar el 131 I mediante varios métodos simples (es decir, calentar para expulsar el 131 I). yodo volátil). Por el contrario, otros radioisótopos de yodo suelen crearse mediante técnicas mucho más caras, empezando por la radiación ciclotrón de cápsulas de gas xenón presurizado . [4]
El yodo-131 es también uno de los trazadores industriales radiactivos emisores de rayos gamma más utilizados . Se inyectan isótopos trazadores radiactivos con fluido de fracturación hidráulica para determinar el perfil de inyección y la ubicación de las fracturas creadas por fracturación hidráulica. [5]
Algunos estudios suponen que dosis incidentales de yodo-131 mucho más pequeñas que las utilizadas en procedimientos terapéuticos médicos son la causa principal del aumento de los cánceres de tiroides después de una contaminación nuclear accidental. Estos estudios suponen que los cánceres se producen por el daño residual de la radiación tisular causado por el 131 I, y deberían aparecer principalmente años después de la exposición, mucho después de que el 131 I se haya desintegrado. [6] [7] Otros estudios no encontraron una correlación. [8] [9]
La mayor parte de la producción de 131 I proviene de la irradiación de neutrones de un objetivo de teluro natural en un reactor nuclear. La irradiación del teluro natural produce casi exclusivamente 131 I, único radionúclido con una vida media superior a horas, ya que la mayoría de los isótopos más ligeros del teluro se convierten en isótopos estables más pesados, o bien en yodo o xenón estables. Sin embargo, el nucleido de telurio natural más pesado, el 130 Te (34% del telurio natural) absorbe un neutrón para convertirse en telurio-131, que decae beta con una vida media de 25 minutos a 131 I.
Un compuesto de teluro puede irradiarse mientras está unido como óxido a una columna de intercambio iónico, y luego el 131 I desprendido se eluye en una solución alcalina. [10] Más comúnmente, el teluro elemental en polvo se irradia y luego se separa mediante destilación seca del yodo, que tiene una presión de vapor mucho más alta . Luego, el elemento se disuelve en una solución ligeramente alcalina de la manera habitual, para producir 131 I en forma de yoduro e hipoyodato (que pronto se reduce a yoduro). [11]
El 131 I es un producto de fisión con un rendimiento del 2,878 % a partir del uranio-235 , [12] y puede liberarse en pruebas de armas nucleares y accidentes nucleares . Sin embargo, la corta vida media significa que no está presente en cantidades significativas en el combustible nuclear gastado enfriado , a diferencia del yodo-129 , cuya vida media es casi mil millones de veces mayor que la del 131 I.
Algunas centrales nucleares lo descargan a la atmósfera en pequeñas cantidades. [13]
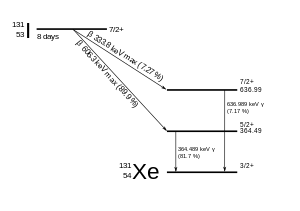
131 I se desintegra con una vida media de 8,02 días con emisiones beta menos y gamma . Este isótopo de yodo tiene 78 neutrones en su núcleo, mientras que el único nucleido estable, el 127 I, tiene 74. Al desintegrarse, el 131 I gasta con mayor frecuencia (89% del tiempo) sus 971 keV de energía de desintegración transformándose en xenón estable. 131 en dos pasos, con la desintegración gamma siguiendo rápidamente a la desintegración beta:
Las emisiones primarias de la desintegración del 131 I son, por tanto, electrones con una energía máxima de 606 keV (89% de abundancia, otros 248-807 keV) y rayos gamma de 364 keV (81% de abundancia, otros 723 keV). [14] La desintegración beta también produce un antineutrino , que elimina cantidades variables de energía de la desintegración beta. Los electrones, debido a su elevada energía media (190 keV, con espectros típicos de desintegración beta) tienen una penetración en el tejido de 0,6 a 2 mm . [15]
El cuerpo absorbe el yodo de los alimentos y se concentra preferentemente en la tiroides, donde es necesario para el funcionamiento de esa glándula. Cuando el 131 I está presente en niveles elevados en el medio ambiente debido a la lluvia radiactiva , puede absorberse a través de alimentos contaminados y también se acumulará en la tiroides. A medida que se descompone, puede causar daño a la tiroides. El principal riesgo de la exposición al 131 I es un mayor riesgo de cáncer inducido por la radiación en la vejez. Otros riesgos incluyen la posibilidad de crecimientos no cancerosos y tiroiditis . [3]
El riesgo de cáncer de tiroides en la vejez parece disminuir a medida que aumenta la edad en el momento de la exposición. La mayoría de las estimaciones de riesgo se basan en estudios en los que se produjeron exposiciones a la radiación en niños o adolescentes. Cuando los adultos están expuestos, ha sido difícil para los epidemiólogos detectar una diferencia estadísticamente significativa en las tasas de enfermedad de la tiroides por encima de la de un grupo similar pero no expuesto. [3] [17]
El riesgo puede mitigarse tomando suplementos de yodo, lo que aumenta la cantidad total de yodo en el cuerpo y, por lo tanto, reduce la absorción y retención en la cara y el pecho y reduce la proporción relativa de yodo radiactivo. Sin embargo, estos suplementos no se distribuyeron sistemáticamente entre la población que vivía más cerca de la central nuclear de Chernobyl después del desastre, [18] aunque sí se distribuyeron ampliamente entre los niños de Polonia.
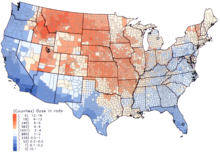
En Estados Unidos, las dosis más altas de lluvia radiactiva de 131 I se produjeron durante los años cincuenta y principios de los sesenta en niños que habían consumido leche fresca procedente de fuentes contaminadas como resultado de pruebas de armas nucleares en la superficie. [6] El Instituto Nacional del Cáncer proporciona información adicional sobre los efectos en la salud de la exposición al 131 I en la lluvia radiactiva, [19] así como estimaciones individualizadas, para los nacidos antes de 1971, para cada uno de los 3070 condados de EE. UU. Los cálculos se toman de los datos recopilados sobre las consecuencias de las pruebas de armas nucleares realizadas en el Sitio de Pruebas de Nevada . [20]
El 27 de marzo de 2011, el Departamento de Salud Pública de Massachusetts informó que se detectó 131 I en concentraciones muy bajas en el agua de lluvia de muestras recolectadas en Massachusetts, EE. UU., y que probablemente se originó en la central eléctrica de Fukushima. [21] Los agricultores cercanos a la planta arrojaron leche cruda, mientras que las pruebas en los Estados Unidos encontraron 0,8 picocurios por litro de yodo-131 en una muestra de leche, pero los niveles de radiación eran 5.000 veces más bajos que el "nivel de intervención definido" de la FDA. Se esperaba que los niveles cayeran relativamente rápido [22]
Un método de tratamiento común para prevenir la exposición al yodo-131 es saturar la tiroides con yodo-127 regular y estable , como yoduro o sal de yodato .

El yodo-131 se utiliza en radioterapia con fuente abierta en medicina nuclear para tratar varias afecciones. También puede detectarse mediante cámaras gamma para diagnóstico por imágenes ; sin embargo, rara vez se administra únicamente con fines de diagnóstico; las imágenes normalmente se realizarán después de una dosis terapéutica. [24] El uso del 131 I como sal de yoduro explota el mecanismo de absorción del yodo por las células normales de la glándula tiroides .
Los usos principales del 131 I incluyen el tratamiento de la tirotoxicosis (hipertiroidismo) debido a la enfermedad de Graves y, a veces, de los nódulos tiroideos hiperactivos (tejido tiroideo anormalmente activo que no es maligno). El uso terapéutico del yodo radiactivo para tratar el hipertiroidismo causado por la enfermedad de Graves fue informado por primera vez por Saul Hertz en 1941. La dosis generalmente se administra por vía oral (ya sea en forma líquida o en cápsulas), de forma ambulatoria , y suele ser de 400 a 600 megabecquerelios (MBq). ). [25] El yodo radiactivo (yodo-131) por sí solo puede empeorar potencialmente la tirotoxicosis en los primeros días después del tratamiento. Un efecto secundario del tratamiento es un período inicial de unos pocos días de aumento de los síntomas de hipertiroidismo. Esto ocurre porque cuando el yodo radiactivo destruye las células tiroideas, estas pueden liberar hormona tiroidea al torrente sanguíneo. Por esta razón, en ocasiones los pacientes son pretratados con medicamentos tirostáticos como el metimazol y/o reciben un tratamiento sintomático como el propranolol. El tratamiento con yodo radiactivo está contraindicado en la lactancia y el embarazo [26]
El yodo-131, en dosis más altas que para la tirotoxicosis, se usa para la ablación del tejido tiroideo remanente después de una tiroidectomía completa para tratar el cáncer de tiroides . [27] [25]
Las dosis terapéuticas típicas de I-131 están entre 2220 y 7400 megabecquerelios (MBq). [28] Debido a esta alta radiactividad y debido a que la exposición del tejido del estómago a la radiación beta sería alta cerca de una cápsula no disuelta, a veces se administra I-131 a pacientes humanos en una pequeña cantidad de líquido. La administración de esta forma líquida suele realizarse mediante pajita que se utiliza para aspirar lenta y cuidadosamente el líquido de un recipiente protegido. [29] Para la administración a animales (por ejemplo, gatos con hipertiroidismo), por razones prácticas, el isótopo debe administrarse mediante inyección. Las directrices europeas recomiendan la administración de una cápsula, debido a "una mayor facilidad para el paciente y la protección radiológica superior para los cuidadores". [30]
Las dosis de ablación generalmente se administran en régimen de internación y las Normas Básicas Internacionales de Seguridad de la OIEA recomiendan que los pacientes no sean dados de alta hasta que la actividad descienda por debajo de 1100 MBq. [31] El consejo de la CIPR establece que "las personas que consuelan y cuidan" de los pacientes sometidos a terapia con radionúclidos deben ser tratados como miembros del público a efectos de restricción de dosis y cualquier restricción impuesta al paciente debe diseñarse sobre la base de este principio. [32]
A los pacientes que reciben tratamiento con yodo radiactivo I-131 se les puede advertir que no tengan relaciones sexuales durante un mes (o menos, dependiendo de la dosis administrada), y a las mujeres que no queden embarazadas durante los seis meses posteriores. "Esto se debe a que existe un riesgo teórico para el feto en desarrollo, aunque la cantidad de radiactividad retenida pueda ser pequeña y no existan pruebas médicas de un riesgo real por el tratamiento con yodo radiactivo. Tal precaución esencialmente eliminaría la exposición fetal directa a la radiactividad y notablemente reducir la posibilidad de concepción con espermatozoides que, en teoría, podrían haber sido dañados por la exposición al yodo radiactivo". [33] Estas pautas varían de un hospital a otro y dependerán de la legislación y orientación nacionales, así como de la dosis de radiación administrada. Algunos también aconsejan no abrazar ni sostener a los niños cuando la radiación aún es alta, y puede recomendarse una distancia de uno o dos metros con los demás. [34]
El I-131 se eliminará del cuerpo durante las próximas semanas después de su administración. La mayor parte del I-131 se eliminará del cuerpo humano en 3 a 5 días, mediante desintegración natural y mediante excreción en el sudor y la orina. Se seguirán liberando cantidades más pequeñas durante las próximas semanas, a medida que el cuerpo procese las hormonas tiroideas creadas con el I-131. Por este motivo, se aconseja limpiar periódicamente los sanitarios, lavabos, sábanas y ropa utilizada por la persona que recibió el tratamiento. También se puede recomendar a los pacientes que usen pantuflas o calcetines en todo momento y que eviten el contacto cercano prolongado con otras personas. Esto minimiza la exposición accidental de los miembros de la familia, especialmente los niños. [35] Se puede recomendar el uso de un descontaminante elaborado especialmente para la eliminación del yodo radiactivo. No se recomienda el uso de soluciones de cloro o limpiadores que contengan cloro para la limpieza, ya que se puede liberar gas yodo elemental radiactivo. [36] La I-131 en el aire puede causar un mayor riesgo de exposición de segunda mano, propagando la contaminación en un área amplia. Se recomienda al paciente, si es posible, que permanezca en una habitación con un baño conectado para limitar la exposición no deseada de los miembros de la familia.
Muchos aeropuertos cuentan con detectores de radiación para detectar el contrabando de materiales radiactivos. Se debe advertir a los pacientes que si viajan en avión, pueden activar los detectores de radiación en los aeropuertos hasta 95 días después de su tratamiento con 131 I. [37]
El isótopo 131 I también se utiliza como marcador radiactivo para ciertos radiofármacos que pueden usarse con fines terapéuticos, por ejemplo, 131 I- metayodobencilguanidina ( 131 I-MIBG) para obtener imágenes y tratar el feocromocitoma y el neuroblastoma . En todos estos usos terapéuticos, el 131 I destruye el tejido mediante radiación beta de corto alcance . Aproximadamente el 90% del daño por radiación al tejido se debe a la radiación beta, y el resto se produce a través de la radiación gamma (a una distancia mayor del radioisótopo). Puede observarse en exploraciones de diagnóstico después de su uso como terapia, porque el 131 I también es un emisor gamma.
Debido a la carcinogenicidad de su radiación beta en la tiroides en pequeñas dosis, el I-131 rara vez se usa principal o exclusivamente para el diagnóstico (aunque en el pasado esto era más común debido a la relativa facilidad de producción y el bajo costo de este isótopo). En cambio , el yodo-123, que emite rayos gamma y es más puro, se utiliza en pruebas de diagnóstico ( exploración de medicina nuclear de la tiroides). El yodo-125 de vida media más larga también se utiliza ocasionalmente cuando se necesita yodo radiactivo de vida media más larga para el diagnóstico y en el tratamiento de braquiterapia (isótopo confinado en pequeñas cápsulas metálicas similares a semillas), donde la radiación gamma de baja energía sin beta componente hace que el yodo-125 sea útil. Los demás radioisótopos del yodo nunca se utilizan en braquiterapia.
Se ha culpado al uso de 131 I como isótopo médico por el rechazo de un envío rutinario de biosólidos al cruzar la frontera entre Canadá y Estados Unidos. [38] Dicho material puede ingresar a las alcantarillas directamente desde las instalaciones médicas o ser excretado por los pacientes después de un tratamiento.
Utilizado por primera vez en 1951 para localizar fugas en un sistema de suministro de agua potable de Munich , Alemania, el yodo-131 se convirtió en uno de los trazadores radiactivos industriales con emisión gamma más utilizados , con aplicaciones en hidrología isotópica y detección de fugas. [39] [40] [41] [42]
Desde finales de la década de 1940, la industria petrolera ha utilizado trazadores radiactivos. Etiquetada en la superficie, el agua se rastrea en el fondo del pozo, utilizando el detector gamma apropiado, para determinar los flujos y detectar fugas subterráneas. El I-131 ha sido el isótopo de marcado más utilizado en una solución acuosa de yoduro de sodio . [43] [44] [45] Se utiliza para caracterizar el fluido de fracturación hidráulica para ayudar a determinar el perfil de inyección y la ubicación de las fracturas creadas por fracturación hidráulica . [46] [47] [48]
En 1997, el NCI llevó a cabo una evaluación detallada de las dosis recibidas en las glándulas tiroides de los residentes de EE. UU. por la I-131 en las consecuencias de las pruebas en Nevada. (...) evaluamos los riesgos de cáncer de tiroides por esa exposición y estimamos que alrededor de 49.000 casos relacionados con las radiaciones radiactivas podrían ocurrir en los Estados Unidos, casi todos ellos entre personas menores de 20 años en algún momento durante el período 1951– 57, con límites de incertidumbre del 95 por ciento de 11.300 y 212.000.
{{cite journal}}: Mantenimiento CS1: DOI inactivo a partir de enero de 2024 ( enlace )no se observaron asociaciones entre las liberaciones de yodo-131 de Hanford y la enfermedad de la tiroides. [Los hallazgos] muestran que si existe un mayor riesgo de enfermedad de la tiroides por la exposición al yodo-131 de Hanford, probablemente sea demasiado pequeño para observarlo utilizando los mejores métodos epidemiológicos disponibles.Resumen ejecutivo
{{cite book}}: |website=ignorado ( ayuda ){{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace )