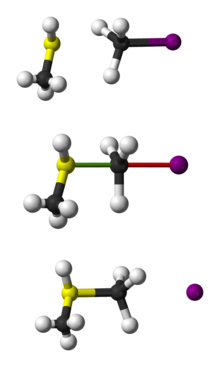
Reacción SN2
Dado que las dos especies reaccionantes están involucradas en esta etapa limitante lenta de la reacción química, esto conduce al nombre de sustitución nucleofílica bimolecular, o SN2.
Entre los químicos inorgánicos, la reacción SN2 es conocida frecuentemente como el mecanismo de intercambio.
La ruptura del enlace C-L, y la formación del nuevo enlace C-Nu sucede simultáneamente para formar un estado de transición en el que el carbono bajo ataque nucleofílico está pentacoordinado, en una hibridación aproximadamente sp2.
Si hay hacinamiento estérico en el sustrato, cerca al grupo saliente, tal como un centro carbono terciario, la sustitución involucrará un mecanismo SN1, en vez de SN2 (una SN1 sería más probable en este caso, debido a que se podría formar un intermediario carbocatiónico suficientemente estable).
Por ejemplo, el ion yoduro es una base muy débil, y debido a esto, es un excelente grupo saliente.
Si una reacción es llevada a cabo en un solvente prótico, cuyas moléculas tienen un átomo de hidrógeno enlazado a un oxígeno o nitrógeno, el átomo más grande es un mejor nucleófilo en una reacción SN2.
En otras palabras, la base más débil es el mejor nucleófilo en un solvente prótico.
Las reacciones SN2 son favorecidas generalmente en halogenuros de alquilo primarios o secundarios, con un solvente aprótico.
Una reacción secundaria común que se presenta en las reacciones SN2 es la eliminación E2: el anión entrante puede actuar como una base en vez de como un nucleófilo, sustrayendo un protón, y conduciendo a la formación del alqueno.
En general, las reacciones en fase gaseosa y las reacciones en fase solución, de este tipo, siguen la misma tendencia, aunque en el primer caso, los efectos del solvente son eliminados.