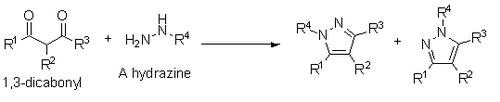
Síntesis de Paal-Knorr
Se reportó inicialmente de forma independiente por los químicos alemanes Carl Paal y Ludwig Knorr en 1884.
[4] El mecanismo de la síntesis del pirrol fue investigado por Amarnath en el año 1991.
La dicetona inicial se convierte en una ti r lo tanto favorecen la reacción.
En la síntesis de pirrol (X = N), R1 puede ser H, arilo, alquilo, amino o hidroxilo.
[7] Diversas condiciones se pueden utilizar para llevar a cabo estas reacciones, la mayoría de los cuales son suaves.
Los métodos actuales permiten condiciones más suaves que se pueden evitar por completo el calentamiento, incluyendo ciclizaciones con microondas.
Se ha reportado que los β-epoxycarbonilos han ciclizado a furanos.
En este procedimiento se puede utilizar un compuesto carbonílico β,γ-insaturado como material de partida, el cual puede ser epoxidado.
El epoxicarbonilo resultante puede ser ciclado a un furano en condiciones ácidas o básicas.
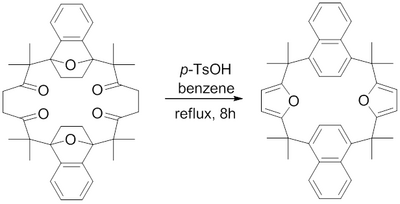
Un diacetal a 3 enlaces de distancia (un 2,5-dihidroxioxolano) se puede convertir exactamente en las mismas condiciones que una 1,4-dicetona en el heterociclo correspondiente.
El empleo de microondas ha demostrado que las reacciones se producen en minutos y en frascos abiertos a temperatura ambiente.
[15] En 2000, Trost y sus colaboradores informaron de una síntesis formal del antibiótico roseofilina.



![[5]](http://upload.wikimedia.org/wikipedia/commons/thumb/7/7d/Paal-Knorr-Furan-Synthesis_mechanism.svg/900px-Paal-Knorr-Furan-Synthesis_mechanism.svg.png)
![[7]](http://upload.wikimedia.org/wikipedia/commons/thumb/3/3d/Paal-Knorr-pyrrole-synthesis_mechanism.svg/550px-Paal-Knorr-pyrrole-synthesis_mechanism.svg.png)
![[9]](http://upload.wikimedia.org/wikipedia/commons/thumb/0/08/Paal-Knorr-thiophen-synth_mechanism.svg/900px-Paal-Knorr-thiophen-synth_mechanism.svg.png)