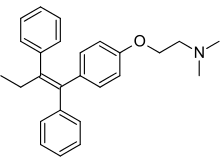
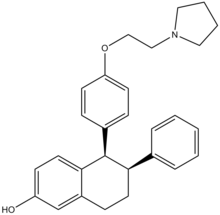
Modulador selectivo de los receptores estrogénicos
[5][6] El tamoxifeno también se utiliza para el tratamiento de la osteoporosis y los lípidos sanguíneos en mujeres posmenopáusicas.
Se asocia a un perfil endometrial aceptable y no ha demostrado efectos similares al tamoxifeno en el útero, pero se ha asociado a efectos adversos como tromboembolismo venoso y síntomas vasomotores, incluidos sofocos.
No se dispone de datos clínicos sobre el cáncer de mama, pero tanto datos in vitro como in vivo sugieren que el ospemifeno puede tener actividad quimiopreventiva en el tejido mamario.
[10] Un ejemplo de un SERM con una IA elevada y, por tanto, con efectos principalmente estrogénicos es el clorotrianiseno, mientras que un ejemplo de un SERM con una IA baja y, por tanto, con efectos principalmente antiestrogénicos es el etamoxitrifetol.
Las hélices 3, 5 y 12 juntas forman una superficie de unión para un motivo de caja NR contenido en coactivadores con la secuencia canónica LXXLL (donde L representa leucina o isoleucina y X es cualquier aminoácido).
Múltiples vías de señalización del crecimiento, como HER2, PKC, PI3K y otras, se regulan a la baja en respuesta al tratamiento antiestrógeno.
Juntas desempeñan un papel importante en la interacción con otras proteínas co-reguladoras que controlan la transcripción génica.
[4][19][20] Aunque, el raloxifeno y la forma activa del tamoxifeno pueden estimular genes informadores regulados por AF-1 tanto en ERα como en ERβ.
[4] Sin embargo, la forma externa del complejo resultante es lo que se convierte en el catalizador para cambiar la respuesta en un tejido diana a un SERM.
[24] El tamoxifeno se somete a un metabolismo de fase I en el hígado por las enzimas microsomales del citocromo P450 (CYP).
[7][22] La fracción de trifeniletileno y la cadena lateral son necesarias para la unión del tamoxifeno al RE, mientras que en el caso del 4-hidroxitamoxifeno, la cadena lateral y el fenil-propeno no parecen ser elementos estructurales cruciales para la unión al RE.
[7] El toremifeno se somete a un metabolismo de fase I por enzimas microsomales del citocromo P450, como el tamoxifeno, pero principalmente por la isoforma CYP3A4.
Tiene una gran afinidad por el RE, con una potente actividad antiestrogénica y efectos específicos en los tejidos distintos del estradiol.
El grupo bisagra flexible, así como la cadena lateral fenil 4-piperidinoetoxi antiestrogénica, son importantes para minimizar los efectos uterinos.
La interacción entre la cadena lateral antiestrogénica del SERM y el aminoácido Asp-351 es el primer paso importante en el silenciamiento de la AF-2.
Pero con la hidrogenación, el doble enlace del nafoxideno se redujo, y ambos fenilos están orientados en cis.
La neutralización de la carga en esta región ER puede explicar algunos efectos antiestrogénicos ejercidos por el lasofoxifeno.
[12] El sistema indol ha servido de unidad central en los SERM, y cuando se une una amina al indol con un benciloxietilo, se demostró que los compuestos resultantes no tenían actividad uterina preclínica, a la vez que preservaban el hueso de la rata con plena eficacia a dosis bajas.
Los estudios de relación estructura-actividad demostraron que al eliminar ese grupo del tamoxifeno se reducía significativamente la actividad agonista en el útero, pero no en el sistema óseo y cardiovascular.
Los datos preclínicos y clínicos muestran que el ospemifeno se tolera bien, sin efectos secundarios importantes.
[32] Se sabe que los SERM presentan cuatro modos distintivos de unión al RE.
Esto provoca una unión preferente al ERα de los sustituyentes del ligando que están alineados hacia abajo frente a Met-336, mientras que los sustituyentes del ligando alineados hacia arriba frente a Met-336 tienen más probabilidades de unirse al ERβ.
[33] El 4-hidroxitamoxifeno se une a los ER dentro del mismo bolsillo de unión que reconoce el 17β-estradiol.
[12] El clomifeno y el torimefeno producen afinidades de unión similares a las del tamoxifeno.
El lasofoxifeno desvía la hélice 12 e impide la unión de proteínas coactivadoras con motivos LXXLL.
Además, el lasofoxifeno también interfiere directamente en la conformación de la hélice 12 mediante el grupo etilpirrolidina del fármaco.
[5]Se ha demostrado que el toremifeno es compatible con el tamoxifeno, y en 1996 se aprobó su uso para el tratamiento del cáncer de mama en mujeres posmenopáusicas.
[36] El raloxifeno fracasó originalmente como fármaco contra el cáncer de mama debido a su escaso rendimiento en comparación con el tamoxifeno en el laboratorio,[19] pero los efectos estrogénicos del raloxifeno sobre los huesos llevaron a su redescubrimiento y aprobación en 1997.
[6] La búsqueda de un potente SERM con eficacia ósea y mejor biodisponibilidad que el raloxifeno condujo al descubrimiento del lasofoxifeno.
En la India, el ormeloxifeno se ha utilizado para la hemorragia uterina disfuncional y el control de la natalidad.