Fosfonato
Son compuestos organofosforados caracterizados por un enlace estable de carbono-fósforo (C-P), que generalmente resiste la descomposición bioquímica, térmica y fotoquímica.
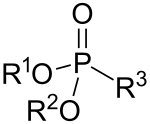
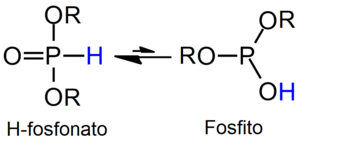
Debido a la tautomería que se da en el ácido fosforoso, podemos tener dos grupos de fosfonatos, los que contienen los grupos R-PO(OH)2 o R-PO(OR')2 (o su versiones "ácidas" con un H en vez de un radical R) o los que contienen el grupo P(OR')3(donde R'= alquilo, arilo...).
La introducción de un grupo amino en la molécula para obtener aminofosfonatos (-NH2-C-PO(OH)2) aumenta las habilidades para atrapar metales por parte del fosfonato.
Estos fosfonatos comunes son los análogos estructurales de los bien conocidos aminopolicarboxilatos NTA, EDTA, y DTPA.
Aunque muchos compuestos de fósforo son reconocidos como reactivos importantes en química orgánica, los fosfonatos en sí han sido prácticamente descuidados.
[3][4] El fósforo es un nutriente esencial para todos los organismos vivos, requerido para la síntesis de ácidos nucleicos, fosfolípidos y otros numerosos metabolitos.
Sin embargo, debido a que la mayoría de las sales de fosfato son altamente insolubles, este ion rara vez está disponible en concentraciones que respalden el crecimiento desenfrenado.
El aminofosfonato natural ciliatina (nombre original) o ácido 2-aminoetilfosfónico (2-AEP), que es un análogo del aminoácido β-alanina y el aminosulfonato taurina, fue el primer fosfonato identificado (en 1959)[8] y se encontró posteriormente como el grupo principal de fosfonolípidos producidos por muchos otros microorganismos, animales, e incluso plantas, donde está localizado en las membranas.
[9] Los fosfonatos son bastante comunes entre diferentes organismos, desde procariotas a eubacterias, fungi, moluscos, insectos y otros.
Prácticamente todos los compuestos biogénicos C–P se sintetizan por una vía en la que el paso clave es la reorganización intramolecular del fosfoenolpiruvato a fosfonopiruvato.
[14] El 2-AEP y el metilfosfonato son componentes de los fosfonoglucanos producidos por arqueas, bacterias, protozoos e invertebrados.
La inhibición del crecimiento fúngico también se usó, consiguiendo aislar los antifúngicos fosfazinomicinas[24] y rizocticinas.
Por lo tanto, el fosfonopiruvato tiene que convertirse rápidamente en compuestos metabólicamente útiles, favoreciendo ese desplazamiento mediante reacciones irreversibles.
Además, se encontró una relación logarítmica entre esta estabilidad y la permitividad relativa del medio disolvente, siendo la forma H-fosfonato más estable en disolventes que tienen mayor permitividad relativa.
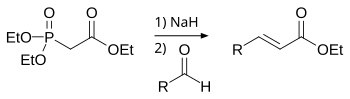
[30] Los diésteres de H-fosfonato, o dialquil H-fosfonatos, como el dimetilfosfito o el dietilfosfito, se presentan únicamente en la forma tautomérica fosfonato, no hay pruebas de su existencia en la forma fosfito.
[34] Este proceso es reversible y puede usarse para producir fosfitos de alquilo mixtos.
El ácido H-fosfónico reacciona con trimetilclorosilano en presencia de trietilamina para dar tris(trimetilsilil)fosfito con un rendimiento del 78-86%:[36] La sililación se produce porque el grupo sililo se transfiere fácilmente al átomo de oxígeno cargado negativamente debido a la fuerte afinidad del silicio por el oxígeno.
Los aminofosfonatos son objetivos importantes en síntesis orgánica como análogos de α-aminoácidos bioisostéricos.
Los ésteres de fosfonato son generalmente susceptibles a la hidrólisis tanto en condiciones ácidas como básicas.
La escisión del enlace P-C o P-H no es fácil de lograr.
Serían el equivalente a un ácido dicarboxílico, en el que se sustituyen los grupos carboxilo por fosfonato.
Los ejemplos incluyen al ácido etidrónico (HEDP), que se prepara a partir de ácido fosforoso y anhídrido acético:[2] Destacan también otros medicamentos para la osteoporosis: ibandronato, risedronato, alendronato, zoledronato... Al igual que los ácidos policarboxílicos, cuando hay más de dos grupos fosfonato en la misma molécula se pueden llamar polifosfonatos.
Esta es una propiedad que comparten con grupos funcionales relacionados, como los ácidos tiocarboxílicos y los organotiofosfatos.
En la manufactura de pulpa y papel y en la industria textil, sirven como estabilizadores de blanqueadores peróxido, al quelar a los metales que podrían desactivar al peróxido.
Junto con los organosilicatos, los fosfonatos también son utilizados para tratar la muerte súbita causada por Phytophthora ramorum.
Los polifosfonatos usados en la industria difieren significativamente de los fosfonatos naturales, tales como el ácido 2-aminoetilfosfónico, porque son más grandes, portan una mayor carga negativa, y están complejados con los metales.