La volatilidad del fluoruro es la tendencia de las moléculas altamente fluoradas a vaporizarse a temperaturas comparativamente bajas. Los heptafluoruros , hexafluoruros y pentafluoruros tienen puntos de ebullición mucho más bajos que los fluoruros de valencia más baja . La mayoría de los difluoruros y trifluoruros tienen puntos de ebullición altos, mientras que la mayoría de los tetrafluoruros y monofluoruros se encuentran en un punto intermedio. El término "volatilidad del fluoruro" es una jerga que se utiliza particularmente en el contexto de la separación de radionucleidos .
Las valencias de la mayoría de los elementos se basan en el fluoruro más alto conocido.
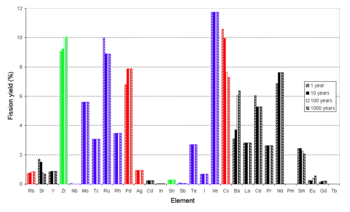
En términos generales, la volatilidad del fluoruro se puede utilizar para eliminar elementos con una valencia de 5 o más: uranio , neptunio , plutonio , metaloides ( telurio , antimonio ), no metales ( selenio ), halógenos ( yodo , bromo ) y los metales de transición intermedios ( niobio , molibdeno , tecnecio , rutenio y posiblemente rodio ). Esta fracción incluye los actínidos más fácilmente reutilizables como combustible nuclear en un reactor térmico y los dos productos de fisión de larga duración más adecuados para su eliminación por transmutación, Tc-99 e I-129 , así como Se-79 .
Los gases nobles ( xenón , criptón ) son volátiles incluso sin fluoración y no se condensan excepto a temperaturas mucho más bajas.
Atrás quedaron los metales alcalinos ( cesio , rubidio ), los metales alcalinotérreos ( estroncio , bario ), los lantánidos , los actínidos restantes ( americio , curio ), los metales de transición restantes ( itrio , circonio , paladio , plata ) y los metales post-transición ( estaño , indio , cadmio ). Esta fracción contiene los productos de fisión que son peligros de radiación en una escala de décadas ( Cs-137 , Sr-90 , Sm-151 ), los cuatro productos de fisión restantes de larga duración Cs-135 , Zr-93 , Pd-107 , Sn-126 de los cuales solo el último emite una fuerte radiación, la mayoría de los venenos neutrónicos y los actínidos superiores ( americio , curio , californio ) que son peligros de radiación en una escala de cientos o miles de años y son difíciles de trabajar debido a la radiación gamma pero son fisionables en un reactor rápido . El americio se utiliza en detectores de humo de ionización, mientras que el californio se utiliza como una fuente de neutrones basada en fisión espontánea . El curio tiene solo usos muy limitados fuera de los reactores nucleares. Los actinoides fisionables pero no fisionables se pueden usar o eliminar en un reactor nuclear subcrítico utilizando una fuente de neutrones externa como un sistema impulsado por acelerador .
Los óxidos de uranio reaccionan con el flúor para formar hexafluoruro de uranio gaseoso , la mayor parte del plutonio reacciona para formar hexafluoruro de plutonio gaseoso, la mayoría de los productos de fisión (especialmente elementos electropositivos: lantánidos , estroncio , bario , itrio , cesio ) forman fluoruros no volátiles. Algunos metales en los productos de fisión (los metales de transición niobio , rutenio , tecnecio , molibdeno y el halógeno yodo ) forman fluoruros volátiles (punto de ebullición <200 °C) que acompañan a los hexafluoruros de uranio y plutonio, junto con gases inertes . Luego se utiliza la destilación para separar el hexafluoruro de uranio de la mezcla. [1] [2]
Los productos de fisión alcalina no volátiles y la fracción menor de actínidos son los más adecuados para su posterior procesamiento con métodos no acuosos de procesamiento electroquímico "seco" ( piroquímico ) . Los fluoruros de lantánidos son difíciles de disolver en el ácido nítrico utilizado para los métodos de reprocesamiento acuoso, como PUREX , DIAMEX y SANEX , que utilizan extracción con solventes . La volatilidad del fluoruro es solo uno de los varios procesos piroquímicos diseñados para reprocesar el combustible nuclear usado.
El instituto de investigación nuclear de Řež en Řež , en la República Checa, probó dosificadores de tornillo que alimentaban óxido de uranio molido (simulando pastillas de combustible usadas) en un fluorador donde las partículas se quemaban en gas flúor para formar hexafluoruro de uranio . [3]
Hitachi ha desarrollado una tecnología, llamada FLUOREX, que combina la volatilidad del fluoruro para extraer uranio, con la extracción con solventes más tradicional (PUREX), para extraer plutonio y otros transuránicos. [4] El ciclo de combustible basado en FLUOREX está diseñado para usarse con el reactor de agua de moderación reducida . [5]
Algunos fluoruros son solubles en agua mientras que otros no (ver la tabla de solubilidad ) y pueden separarse en solución acuosa. Sin embargo, todos los procesos acuosos que tienen lugar sin la eliminación completa del tritio (un producto común de la fisión ternaria ) [6] [7] antes de la adición de agua contaminarán el agua con agua tritiada que es difícil de eliminar del agua. [8] [9] [10] Algunos elementos que forman fluoruros solubles forman cloruros insolubles. La adición de un cloruro soluble adecuado (por ejemplo, cloruro de sodio ) salará esos cationes. Un ejemplo es el fluoruro de plata (I) (soluble en agua) que forma un precipitado de cloruro de plata tras la adición de un cloruro soluble.
Algunos fluoruros reaccionan agresivamente con el agua y pueden formar fluoruro de hidrógeno altamente corrosivo . Esto debe tenerse en cuenta si se van a utilizar procesos acuosos que involucren fluoruros. [11]
Si se desea, se puede utilizar una serie de adiciones de aniones adicionales similares al método de des:Kationentrennungsgang para separar diferentes cationes para su eliminación, procesamiento posterior o uso.