
La transición vidrio-líquido , o transición vítrea , es la transición gradual y reversible en materiales amorfos (o en regiones amorfas dentro de materiales semicristalinos ) de un estado "vítreo" duro y relativamente quebradizo a un estado viscoso o gomoso a medida que aumenta la temperatura. [2] Un sólido amorfo que presenta una transición vítrea se llama vidrio . La transición inversa, lograda al sobreenfriar un líquido viscoso al estado vítreo, se llama vitrificación .
La temperatura de transición vítrea Tg de un material caracteriza el rango de temperaturas en las que se produce esta transición vítrea (como definición experimental, típicamente marcada como 100 s de tiempo de relajación). Siempre es inferior a la temperatura de fusión , Tm , del estado cristalino del material, si existe, porque el vidrio tiene un estado de energía (o entalpía a presión constante) más alto que el cristal correspondiente.
Los plásticos duros como el poliestireno y el poli(metacrilato de metilo) se utilizan muy por debajo de sus temperaturas de transición vítrea, es decir, cuando están en su estado vítreo. Sus valores de T g se sitúan ambos en torno a los 100 °C (212 °F). Los elastómeros de caucho como el poliisopreno y el poliisobutileno se utilizan por encima de su Tg , es decir, en estado gomoso, donde son suaves y flexibles; la reticulación impide el libre flujo de sus moléculas, lo que confiere al caucho una forma fija a temperatura ambiente (a diferencia de un líquido viscoso). [3]
A pesar del cambio en las propiedades físicas de un material a través de su transición vítrea, la transición no se considera una transición de fase ; más bien es un fenómeno que se extiende sobre un rango de temperatura y se define por una de varias convenciones. [4] [5] Tales convenciones incluyen una velocidad de enfriamiento constante (20 kelvin por minuto (36 °F/min)) [2] y un umbral de viscosidad de 10 12 Pa·s , entre otros. Al enfriarse o calentarse a través de este rango de transición vítrea, el material también muestra un paso suave en el coeficiente de expansión térmica y en el calor específico , y la ubicación de estos efectos depende nuevamente de la historia del material. [6] La cuestión de si alguna transición de fase subyace a la transición vítrea es una cuestión de investigación en curso. [4] [5] [7] [ ¿cuándo? ]
Transición vítrea (en ciencia de los polímeros): proceso en el que un polímero fundido cambia al enfriarse a un vidrio polimérico o un vidrio polimérico cambia al calentarse a un polímero fundido. [8]
- Los fenómenos que ocurren en la transición vítrea de los polímeros todavía están sujetos a investigación y debate científicos en curso. La transición vítrea presenta características de transición de segundo orden, ya que los estudios térmicos a menudo indican que las energías molares de Gibbs, las entalpías molares y los volúmenes molares de las dos fases, es decir, la masa fundida y el vidrio, son iguales, mientras que la capacidad calorífica y la expansividad son discontinuas. Sin embargo, la transición vítrea generalmente no se considera una transición termodinámica en vista de la dificultad inherente de alcanzar el equilibrio en un vidrio polimérico o en una masa fundida de polímero a temperaturas cercanas a la temperatura de transición vítrea.
- En el caso de los polímeros, los cambios conformacionales de los segmentos, que normalmente constan de 10 a 20 átomos de la cadena principal, se vuelven infinitamente lentos por debajo de la temperatura de transición vítrea.
- En un polímero parcialmente cristalino, la transición vítrea ocurre sólo en las partes amorfas del material.
- La definición es diferente a la de la ref. [9]
- No se recomienda el término comúnmente utilizado “transición vidrio-caucho” para la transición vítrea. [8]
La transición vítrea de un líquido a un estado sólido puede ocurrir mediante enfriamiento o compresión. [10] La transición comprende un aumento suave de la viscosidad de un material de hasta 17 órdenes de magnitud dentro de un rango de temperatura de 500 K sin ningún cambio pronunciado en la estructura del material. [11] Esta transición contrasta con la transición de congelación o cristalización , que es una transición de fase de primer orden en la clasificación de Ehrenfest e implica discontinuidades en propiedades termodinámicas y dinámicas como el volumen, la energía y la viscosidad. En muchos materiales que normalmente experimentan una transición de congelación, un enfriamiento rápido evitará esta transición de fase y, en cambio, dará como resultado una transición vítrea a una temperatura más baja. Otros materiales, como muchos polímeros , carecen de un estado cristalino bien definido y forman vidrios fácilmente, incluso tras un enfriamiento o compresión muy lentos. La tendencia de un material a formar vidrio mientras se enfría se denomina capacidad de formación de vidrio. Esta capacidad depende de la composición del material y puede predecirse mediante la teoría de la rigidez . [12]
Por debajo del rango de temperatura de transición, la estructura vítrea no se relaja de acuerdo con la velocidad de enfriamiento utilizada. El coeficiente de expansión del estado vítreo es aproximadamente equivalente al del sólido cristalino. Si se utilizan velocidades de enfriamiento más lentas, el mayor tiempo para que se produzca la relajación estructural (o reordenamiento intermolecular) puede dar como resultado un producto de vidrio de mayor densidad. De manera similar, al recocer (y permitir así una relajación estructural lenta), la estructura del vidrio se acerca con el tiempo a una densidad de equilibrio correspondiente al líquido sobreenfriado a esta misma temperatura. Tg se encuentra en la intersección entre la curva de enfriamiento (volumen versus temperatura) para el estado vítreo y el líquido sobreenfriado . [13] [14] [15] [16] [17]
La configuración del vidrio en este rango de temperaturas cambia lentamente con el tiempo hacia la estructura de equilibrio. El principio de minimización de la energía libre de Gibbs proporciona la fuerza impulsora termodinámica necesaria para el eventual cambio. A temperaturas algo más altas que Tg , la estructura correspondiente al equilibrio a cualquier temperatura se logra con bastante rapidez. Por el contrario, a temperaturas considerablemente más bajas, la configuración del vidrio se mantiene sensiblemente estable durante periodos de tiempo cada vez más prolongados.
Así, la transición líquido-vidrio no es una transición entre estados de equilibrio termodinámico . Se cree ampliamente que el verdadero estado de equilibrio es siempre cristalino. Se cree que el vidrio existe en un estado cinéticamente bloqueado, y su entropía, densidad, etc., dependen de la historia térmica. Por tanto, la transición vítrea es principalmente un fenómeno dinámico. El tiempo y la temperatura son cantidades intercambiables (hasta cierto punto) cuando se trata de vasos, un hecho que a menudo se expresa en el principio de superposición tiempo-temperatura . Al enfriar un líquido, los grados de libertad internos se desequilibran sucesivamente . Sin embargo, existe un debate de larga data sobre si existe una transición de fase de segundo orden subyacente en el límite hipotético de tiempos de relajación infinitamente largos. [ se necesita aclaración ] [6] [18] [19] [20]
En un modelo más reciente de transición vítrea, la temperatura de transición vítrea corresponde a la temperatura a la que las aberturas más grandes entre los elementos vibrantes en la matriz líquida se vuelven más pequeñas que las secciones transversales más pequeñas de los elementos o partes de ellos cuando la temperatura disminuye. . Como resultado de la entrada fluctuante de energía térmica en la matriz líquida, los armónicos de las oscilaciones se alteran constantemente y se crean cavidades temporales ("volumen libre") entre los elementos, cuyo número y tamaño dependen de la temperatura. La temperatura de transición vítrea Tg0 definida de esta manera es una constante fija del material en estado desordenado (no cristalino) que depende únicamente de la presión. Debido a la creciente inercia de la matriz molecular al acercarse a Tg0 , el establecimiento del equilibrio térmico se retrasa sucesivamente, de modo que los métodos de medición habituales para determinar la temperatura de transición vítrea dan en principio valores de Tg demasiado altos. En principio, cuanto más lentamente se ajusta la velocidad de cambio de temperatura durante la medición, más se aproxima el valor Tg medido Tg0 . [21] Se pueden utilizar técnicas como el análisis mecánico dinámico para medir la temperatura de transición vítrea. [22]
La definición de vidrio y transición vítrea no está establecida y se han propuesto muchas definiciones durante el siglo pasado. [23]
Franz Simon : [24] El vidrio es un material rígido que se obtiene por congelación de un líquido sobreenfriado en un estrecho rango de temperaturas.
Zachariasen : [25] El vidrio es una red topológicamente desordenada, con un orden de corto alcance equivalente al del cristal correspondiente. [26]
El vidrio es un "líquido congelado" (es decir, líquidos cuya ergodicidad se ha roto), que se relaja espontáneamente hacia el estado líquido sobreenfriado durante un tiempo suficientemente largo.
Los vidrios son sólidos amorfos estabilizados cinéticamente y en desequilibrio termodinámico, en los que el desorden molecular y las propiedades termodinámicas correspondientes al estado de la respectiva masa fundida subenfriada a una temperatura T* están congelados. Por este motivo T* difiere de la temperatura real T . [27]
El vidrio es un estado de materia condensado no cristalino y sin equilibrio que presenta una transición vítrea. La estructura de los vasos es similar a la de sus líquidos superenfriados (SCL) originales y se relajan espontáneamente hacia el estado SCL. Su destino final es solidificarse, es decir, cristalizar. [23]


Consulte la figura en la parte inferior derecha que representa la capacidad calorífica en función de la temperatura. En este contexto, T g es la temperatura correspondiente al punto A de la curva. [28]
Se utilizan diferentes definiciones operativas de la temperatura de transición vítrea Tg , y varias de ellas están respaldadas como estándares científicos aceptados. Sin embargo, todas las definiciones son arbitrarias y todas arrojan resultados numéricos diferentes: en el mejor de los casos, los valores de T g para una sustancia determinada coinciden dentro de unos pocos kelvin. Una definición se refiere a la viscosidad , fijando T g en un valor de 10 13 poise (o 10 12 Pa·s). Como se demuestra experimentalmente, este valor está cerca del punto de recocido de muchos vidrios. [29]
A diferencia de la viscosidad, la expansión térmica , la capacidad calorífica , el módulo de corte y muchas otras propiedades de los vidrios inorgánicos muestran un cambio relativamente repentino en la temperatura de transición vítrea. Cualquier paso o torsión de este tipo se puede utilizar para definir Tg . Para que esta definición sea reproducible, se debe especificar la velocidad de enfriamiento o calentamiento.
La definición de Tg más utilizada utiliza la energía liberada al calentarse en calorimetría diferencial de barrido (DSC, ver figura). Normalmente, la muestra primero se enfría a 10 K/min y luego se calienta a la misma velocidad.
Otra definición más de T g utiliza la torsión en dilatometría (también conocida como expansión térmica): consulte la figura en la parte superior derecha. Aquí, son comunes velocidades de calentamiento de 3 a 5 K/min (5,4 a 9,0 °F/min). Las secciones lineales debajo y encima de T g están coloreadas en verde. T g es la temperatura en la intersección de las líneas de regresión rojas. [28]
A continuación se resumen los valores de T g característicos de ciertas clases de materiales.
El nailon-6 seco tiene una temperatura de transición vítrea de 47 °C (117 °F). [35] El nailon-6,6 en estado seco tiene una temperatura de transición vítrea de aproximadamente 70 °C (158 °F). [36] [37] Mientras que el polietileno tiene un rango de transición vítrea de −130 a −80 °C (−202 a −112 °F) [38] Los anteriores son solo valores medios, ya que la temperatura de transición vítrea depende de la velocidad de enfriamiento y la distribución del peso molecular y podrían verse influenciados por los aditivos. Para un material semicristalino, como el polietileno , que es entre un 60% y un 80% cristalino a temperatura ambiente, la transición vítrea citada se refiere a lo que le sucede a la parte amorfa del material al enfriarse.

En 1971, Zeller y Pohl descubrieron que [42] cuando el vidrio está a una temperatura muy baja ~1K, su calor específico tiene un componente lineal: . Este es un efecto inusual, porque el material cristalino suele tener , como en el modelo Debye . Esto se explica por la hipótesis del sistema de dos niveles, [43] que afirma que un vaso está poblado por sistemas de dos niveles, que parecen un doble pozo de potencial separado por una pared. La pared es lo suficientemente alta como para que no se produzcan túneles de resonancia, pero sí se producen túneles térmicos. Es decir, si los dos pozos tienen diferencia de energía , entonces una partícula en un pozo puede hacer un túnel hacia el otro mediante interacción térmica con el medio ambiente. Ahora, imagine que hay muchos sistemas de dos niveles en el vidrio, y están distribuidos aleatoriamente pero son fijos ("desorden apagado"), luego, a medida que la temperatura baja, más y más de estos niveles de dos niveles se congelan (lo que significa que Se necesita tanto tiempo para que se produzca un túnel que no se pueden observar experimentalmente).
Considere un sistema único de dos niveles que no está congelado, cuya brecha de energía es . Está en una distribución de Boltzmann, por lo que su energía promedio .
Ahora supongamos que todos los sistemas de dos niveles están templados, de modo que cada uno varía poco con la temperatura. En ese caso, podemos escribir como la densidad de estados con brecha energética . También asumimos que es positivo y suave cerca .
Entonces, la energía total aportada por esos sistemas de dos niveles es
El efecto es que la energía promedio en estos sistemas de dos niveles es , lo que lleva a un término.
En mediciones experimentales, se mide la capacidad calorífica específica del vidrio a diferentes temperaturas y se traza un gráfico. Suponiendo que , el gráfico debería mostrar , es decir, una línea recta con pendiente que muestra la capacidad calorífica típica de Debye y una intersección vertical que muestra el componente lineal anómalo. [41]

A medida que un líquido se sobreenfría, la diferencia de entropía entre la fase líquida y la sólida disminuye. Extrapolando la capacidad calorífica del líquido sobreenfriado por debajo de su temperatura de transición vítrea , es posible calcular la temperatura a la que la diferencia de entropías se vuelve cero. Esta temperatura ha sido denominada temperatura de Kauzmann .
Si un líquido pudiera sobreenfriarse por debajo de su temperatura Kauzmann, y de hecho mostrara una entropía más baja que la fase cristalina, esto sería paradójico, ya que la fase líquida debería tener la misma entropía vibratoria, pero una entropía posicional mucho mayor, que la fase cristalina. . Esta es la paradoja de Kauzmann , aún no resuelta definitivamente. [44] [45]
Hay muchas soluciones posibles a la paradoja de Kauzmann.
El propio Kauzmann resolvió la paradoja de la entropía postulando que todos los líquidos sobreenfriados deben cristalizar antes de alcanzar la temperatura de Kauzmann.
Quizás a la temperatura de Kauzmann, el vidrio alcanza una fase vítrea ideal , que todavía es amorfa, pero tiene un orden amorfo de largo alcance que disminuye su entropía general a la del cristal. El vaso ideal sería una verdadera fase de la materia. [45] [46] Se plantea la hipótesis del vidrio ideal, pero no se puede observar de forma natural, ya que tardaría demasiado en formarse. Se ha observado algo parecido a un vidrio ideal como "vidrio ultraestable" formado por deposición de vapor , [47]
Quizás deba haber una transición de fase antes de que disminuya la entropía del líquido. En este escenario, la temperatura de transición se conoce como temperatura de transición vítrea calorimétrica ideal T 0c . Desde este punto de vista, la transición vítrea no es simplemente un efecto cinético , es decir, simplemente el resultado de un enfriamiento rápido de una masa fundida, sino que existe una base termodinámica subyacente para la formación del vidrio. La temperatura de transición vítrea:
Quizás la capacidad calorífica del líquido sobreenfriado cerca de la temperatura de Kauzmann disminuya suavemente hasta un valor menor.
Quizás la transición de fase de primer orden a otro estado líquido ocurra antes de la temperatura de Kauzmann, siendo la capacidad calorífica de este nuevo estado menor que la obtenida por extrapolación a partir de una temperatura más alta.
La sílice (el compuesto químico SiO 2 ) tiene varias formas cristalinas distintas además de la estructura de cuarzo. Casi todas las formas cristalinas involucran unidades tetraédricas de SiO 4 unidas entre sí por vértices compartidos en diferentes disposiciones ( la stishovita , compuesta de octaedros de SiO 6 unidos , es la principal excepción). Las longitudes de los enlaces Si-O varían entre las diferentes formas cristalinas. Por ejemplo, en el cuarzo α la longitud del enlace es de 161 picometros (6,3 × 10 −9 pulgadas), mientras que en la tridimita α oscila entre 154 y 171 pm (6,1 × 10 −9 –6,7 × 10 −9 pulgadas). El ángulo del enlace Si-O-Si también varía de 140° en α-tridimita a 144° en α-cuarzo y 180° en β-tridimita. Cualquier desviación de estos parámetros estándar constituye diferencias o variaciones microestructurales que representan una aproximación a un sólido amorfo , vítreo o vítreo . La temperatura de transición Tg en silicatos está relacionada con la energía requerida para romper y volver a formar enlaces covalentes en una red amorfa (o red aleatoria) de enlaces covalentes . La Tg está claramente influenciada por la química del vidrio. Por ejemplo, la adición de elementos como B , Na , K o Ca a un vidrio de sílice , que tienen una valencia inferior a 4, ayuda a romper la estructura de la red, reduciendo así la Tg . Alternativamente, P , que tiene una valencia de 5, ayuda a reforzar una red ordenada y, por lo tanto, aumenta la Tg . [48] T g es directamente proporcional a la fuerza del enlace, por ejemplo, depende de los parámetros termodinámicos de cuasi equilibrio de los enlaces, por ejemplo, de la entalpía H d y la entropía S d de configuraciones – enlaces rotos: T g = H d / [ S d + R ln[(1 − f c )/ f c ] donde R es la constante de los gases y f c es el umbral de percolación. Para fundidos fuertes como el Si O 2, el umbral de percolación en la ecuación anterior es la densidad crítica universal de Scher-Zallen en el espacio tridimensional, por ejemplo, f c= 0,15, sin embargo, para materiales frágiles los umbrales de percolación dependen del material y f c ≪ 1. [49] La entalpía H d y la entropía S d de configuraciones: enlaces rotos se pueden encontrar a partir de los datos experimentales disponibles sobre viscosidad. [50] En la superficie de las películas de SiO 2 , la microscopía de efecto túnel ha resuelto grupos de ca. 5 SiO 2 de diámetro que se mueven en dos estados en una escala de tiempo de minutos. Esto es mucho más rápido que la dinámica en masa, pero está de acuerdo con los modelos que comparan la dinámica en masa y en superficie. [51] [52]
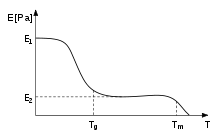
En los polímeros, la temperatura de transición vítrea, Tg , a menudo se expresa como la temperatura a la que la energía libre de Gibbs es tal que se excede la energía de activación para el movimiento cooperativo de aproximadamente 50 elementos del polímero [ cita necesaria ] . Esto permite que las cadenas moleculares se deslicen unas sobre otras cuando se aplica una fuerza. A partir de esta definición, podemos ver que la introducción de grupos químicos relativamente rígidos (como anillos de benceno ) interferirá con el proceso de flujo y, por lo tanto, aumentará la Tg . [53] La rigidez de los termoplásticos disminuye debido a este efecto (ver figura). Cuando se alcanza la temperatura del vidrio, la rigidez permanece igual por un tiempo, es decir, en o cerca de E 2 , hasta que la temperatura excede T m , y el material se derrite. Esta región se llama meseta del caucho.

Al planchar , se calienta un tejido a través de esta transición para que las cadenas de polímeros se vuelvan móviles. El peso del hierro impone entonces una orientación preferida. La Tg se puede reducir significativamente mediante la adición de plastificantes a la matriz polimérica. Moléculas más pequeñas de plastificante se incrustan entre las cadenas de polímero, aumentando el espacio y el volumen libre, y permitiéndoles moverse unas sobre otras incluso a temperaturas más bajas. La adición de plastificante puede controlar eficazmente la dinámica de la cadena del polímero y dominar las cantidades del volumen libre asociado de modo que el aumento de la movilidad de los extremos del polímero no sea evidente. [54] La adición de grupos laterales no reactivos a un polímero también puede hacer que las cadenas se separen entre sí, reduciendo la Tg . Si un plástico con algunas propiedades deseables tiene una T g demasiado alta, a veces se puede combinar con otro en un copolímero o material compuesto con una T g inferior a la temperatura de uso previsto. Tenga en cuenta que algunos plásticos se utilizan a altas temperaturas, por ejemplo, en motores de automóviles, y otros a bajas temperaturas. [32]
En los materiales viscoelásticos , la presencia de un comportamiento similar al de un líquido depende de las propiedades y, por lo tanto, varía con la tasa de carga aplicada, es decir, con qué rapidez se aplica una fuerza. El juguete de silicona Silly Putty se comporta de manera muy diferente dependiendo del tiempo de aplicación de una fuerza: se tira lentamente y fluye, actuando como un líquido muy viscoso; Golpéalo con un martillo y se rompe, actuando como un vaso.
Al enfriarse, el caucho sufre una transición líquido-vítrea , que también se ha denominado transición caucho-vítreo .
El movimiento molecular en la materia condensada se puede representar mediante una serie de Fourier cuya interpretación física consiste en una superposición de ondas longitudinales y transversales de desplazamiento atómico con direcciones y longitudes de onda variables. En los sistemas monoatómicos, estas ondas se denominan fluctuaciones de densidad . (En los sistemas poliatómicos, también pueden incluir fluctuaciones de composición). [55]
Así, el movimiento térmico en líquidos puede descomponerse en vibraciones longitudinales elementales (o fonones acústicos ), mientras que las vibraciones transversales (u ondas de corte) se describieron originalmente sólo en sólidos elásticos que exhibían el estado cristalino altamente ordenado de la materia. En otras palabras, los líquidos simples no pueden soportar una fuerza aplicada en forma de esfuerzo cortante y cederán mecánicamente mediante deformación plástica macroscópica (o flujo viscoso). Además, muchos aceptan el hecho de que un sólido se deforme localmente manteniendo su rigidez (mientras que un líquido cede a un flujo viscoso macroscópico en respuesta a la aplicación de una fuerza cortante ) como la distinción mecánica entre los dos. [56] [57]
Sin embargo, Frenkel señaló las deficiencias de esta conclusión en su revisión de la teoría cinética de los sólidos y la teoría de la elasticidad en los líquidos . Esta revisión se deriva directamente de la característica continua del cruce viscoelástico del estado líquido al sólido cuando la transición no va acompañada de cristalización, es decir, el líquido viscoso sobreenfriado . Así vemos la íntima correlación entre los fonones acústicos transversales (u ondas de corte) y la aparición de rigidez tras la vitrificación , como lo describe Bartenev en su descripción mecánica del proceso de vitrificación. [58] [59]
Las velocidades de los fonones acústicos longitudinales en la materia condensada son directamente responsables de la conductividad térmica que nivela las diferencias de temperatura entre los elementos de volumen comprimidos y expandidos . Kittel propuso que el comportamiento de los vidrios se interpreta en términos de un " camino libre medio " aproximadamente constante para los fonones reticulares, y que el valor del camino libre medio es del orden de magnitud de la escala de desorden en la estructura molecular de un líquido o sólido. Se han trazado los caminos libres medios de los fonones térmicos o las longitudes de relajación de varios formadores de vidrio frente a la temperatura de transición vítrea, lo que indica una relación lineal entre los dos. Esto ha sugerido un nuevo criterio para la formación de vidrio basado en el valor del camino libre medio del fonón. [60]
A menudo se ha sugerido que el transporte de calor en sólidos dieléctricos se produce a través de vibraciones elásticas de la red, y que este transporte está limitado por la dispersión elástica de fonones acústicos por defectos de la red (por ejemplo, vacantes espaciadas aleatoriamente). [61] Estas predicciones fueron confirmadas por experimentos con vidrios y vitrocerámicas comerciales , donde los caminos libres medios aparentemente estaban limitados por la "dispersión de límites internos" a escalas de longitud de 10 a 100 micrómetros (0,00039 a 0,00394 pulgadas). [62] [63] La relación entre estas ondas transversales y el mecanismo de vitrificación ha sido descrita por varios autores que propusieron que el inicio de correlaciones entre tales fonones da como resultado un ordenamiento orientacional o "congelación" de las tensiones de corte locales en la formación de vidrio. líquidos, produciendo así la transición vítrea. [64]
La influencia de los fonones térmicos y su interacción con la estructura electrónica es un tema que se introdujo apropiadamente en una discusión sobre la resistencia de los metales líquidos. Se hace referencia a la teoría de la fusión de Lindemann, [65] y se sugiere que la caída en la conductividad al pasar del estado cristalino al líquido se debe a la mayor dispersión de los electrones de conducción como resultado del aumento de la amplitud de la vibración atómica . Estas teorías de localización se han aplicado al transporte en vidrios metálicos , donde el camino libre medio de los electrones es muy pequeño (del orden del espaciamiento interatómico). [66] [67]
La formación de una forma no cristalina de una aleación de oro y silicio mediante el método de enfriamiento por salpicadura de la masa fundida llevó a nuevas consideraciones sobre la influencia de la estructura electrónica en la capacidad de formación del vidrio, basándose en las propiedades del enlace metálico . [68] [69] [70] [71] [72]
Otro trabajo indica que la movilidad de los electrones localizados se ve reforzada por la presencia de modos de fonones dinámicos. Una afirmación en contra de tal modelo es que si los enlaces químicos son importantes, los modelos de electrones casi libres no deberían ser aplicables. Sin embargo, si el modelo incluye la acumulación de una distribución de carga entre todos los pares de átomos como un enlace químico (por ejemplo, silicio, cuando una banda está simplemente llena de electrones), entonces debería aplicarse a los sólidos . [73]
Por tanto, si la conductividad eléctrica es baja, el camino libre medio de los electrones es muy corto. Los electrones sólo serán sensibles al orden de corto alcance en el vidrio, ya que no tienen la posibilidad de dispersarse desde átomos espaciados a grandes distancias. Dado que el orden de corto alcance es similar en vidrios y cristales, las energías electrónicas deberían ser similares en estos dos estados. Para aleaciones con menor resistividad y caminos libres medios electrónicos más largos, los electrones podrían comenzar a sentir [ dudoso - discutir ] que hay desorden en el vidrio, y esto aumentaría sus energías y desestabilizaría el vidrio con respecto a la cristalización. Por lo tanto, las tendencias de formación de vidrio de ciertas aleaciones pueden deberse en parte al hecho de que los caminos libres medios de los electrones son muy cortos, de modo que sólo el orden de corto alcance es importante para la energía de los electrones.
También se ha argumentado que la formación de vidrio en sistemas metálicos está relacionada con la "suavidad" del potencial de interacción entre átomos diferentes. Algunos autores, destacando las fuertes similitudes entre la estructura local del vidrio y el cristal correspondiente, sugieren que los enlaces químicos ayudan a estabilizar la estructura amorfa. [74] [75]
Otros autores han sugerido que la estructura electrónica ejerce su influencia en la formación del vidrio a través de las propiedades direccionales de los enlaces. Por tanto, la no cristalinidad se ve favorecida en elementos con un gran número de formas polimórficas y un alto grado de anisotropía de enlace . La cristalización se vuelve más improbable a medida que aumenta la anisotropía del enlace desde un enlace metálico isotrópico a un enlace metálico anisotrópico y a un enlace covalente , lo que sugiere una relación entre el número de grupo en la tabla periódica y la capacidad de formación de vidrio en los sólidos elementales . [76]