La ADN primasa es una enzima implicada en la replicación del ADN y es un tipo de ARN polimerasa . La primasa cataliza la síntesis de un segmento corto de ARN (o ADN en algunos organismos vivos [1] ) llamado cebador complementario a una plantilla de ADN ss (ADN monocatenario). Después de este alargamiento, el trozo de ARN se elimina mediante una exonucleasa de 5' a 3' y se vuelve a llenar con ADN.

En las bacterias , la primasa se une a la ADN helicasa formando un complejo llamado primosoma . La primasa es activada por la helicasa donde luego sintetiza un cebador de ARN corto de aproximadamente 11 ± 1 nucleótidos de largo, al que la ADN polimerasa puede agregar nuevos nucleótidos. Las primasas de arqueas y eucariotas son proteínas heterodiméricas con una subunidad reguladora grande y una subunidad catalítica minúscula. [2]
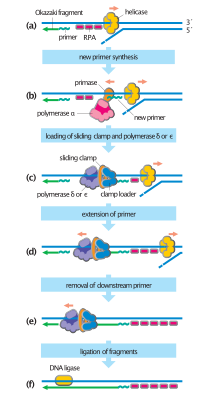
Los segmentos de ARN son primero sintetizados por primasa y luego alargados por ADN polimerasa. [3] Luego, la ADN polimerasa forma un complejo proteico con dos subunidades de primasa para formar el complejo alfa ADN polimerasa primasa. La primasa es una de las polimerasas más lentas y propensas a errores. [3] Las primasas en organismos como E. coli sintetizan alrededor de 2000 a 3000 cebadores a razón de un cebador por segundo. [4] La primasa también actúa como un mecanismo de detención para evitar que la cadena principal supere a la cadena retrasada al detener la progresión de la bifurcación de replicación . [5] El paso determinante de la velocidad en la primasa es cuando se forma el primer enlace fosfodiéster entre dos moléculas de ARN. [3]
Los mecanismos de replicación difieren entre diferentes bacterias y virus, donde la primasa se une covalentemente a la helicasa en virus como el bacteriófago T7 . [5] En virus como el virus del herpes simple (HSV-1), la primasa puede formar complejos con la helicasa. [6] El complejo primasa-helicasa se utiliza para desenrollar el ADNbc (bicatenario) y sintetiza la cadena rezagada utilizando cebadores de ARN. [6] La mayoría de los cebadores sintetizados por primasa tienen de dos a tres nucleótidos de longitud. [6]
Hay dos tipos principales de primasas: DnaG que se encuentra en la mayoría de las bacterias y la superfamilia AEP (Archaeo-Eukaryote Primase) que se encuentra en las primasas arcaicas y eucariotas. Mientras que las primasas bacterianas ( tipo DnaG ) están compuestas de una sola unidad proteica (un monómero) y sintetizan cebadores de ARN, las primasas AEP generalmente se componen de dos unidades de primasas diferentes (un heterodímero) y sintetizan cebadores de dos partes con componentes de ARN y ADN. . [7] Aunque funcionalmente similares, las dos superfamilias de primasas evolucionaron independientemente una de otra.
La estructura cristalina de primasa en E. coli con un núcleo que contiene la proteína DnaG se determinó en el año 2000. [4] El complejo DnaG y primasa tiene forma de anacardo y contiene tres subdominios. [4] El subdominio central forma un pliegue superior que está hecho de una mezcla de cinco láminas beta y seis hélices alfa . [4] [8] El pliegue superior se utiliza para unir reguladores y metales. La primasa utiliza un dominio de fosfotransferencia para la coordinación de la transferencia de metales, lo que la distingue de otras polimerasas. [4] Las subunidades laterales contienen un terminal NH 2 y COOH formado por hélices alfa y láminas beta. [4] El terminal NH 2 interactúa con un dominio de unión a zinc y una región terminal COOH que interactúa con DnaB-ID. [4]
El pliegue de Toprim también se encuentra en la topoisomerasa y en la twinkle primasa/helicasa mitocondrial. [8] Se han encontrado primasas similares a DnaG (similares a bacterias; InterPro : IPR020607 ) en genomas de arqueas. [9]
Las primasas eucariotas y arqueales tienden a ser más similares entre sí, en términos de estructura y mecanismo, que las primasas bacterianas. [10] [11] La superfamilia de primasas eucarióticas (AEP), a la que pertenecen la mayoría de las subunidades catalíticas de primasas eucariotas y arqueales, se ha redefinido recientemente como una familia de primasas-polimerasas en reconocimiento de las muchas otras funciones que desempeñan las enzimas de esta familia. . [12] Esta clasificación también enfatiza los amplios orígenes de las primasas AEP; Ahora se reconoce que la superfamilia está en transición entre las funciones de ARN y ADN. [13]
Las primasas de arqueas y eucariotas son proteínas heterodiméricas con una subunidad reguladora grande ( PRIM2 humana , p58) y una subunidad catalítica pequeña ( PRIM1 humana , p48/p49). [2] La subunidad grande contiene un grupo N-terminal 4Fe-4S, dividido en algunas arqueas como PriX/PriCT. [14] La subunidad grande está implicada en la mejora de la actividad y la especificidad de la subunidad pequeña. Por ejemplo, eliminar la parte correspondiente a la subunidad grande en una proteína de fusión PolpTN2 da como resultado una enzima más lenta con actividad de transcriptasa inversa. [13]

La familia AEP de primasas-polimerasas tiene diversas características más allá de fabricar únicamente cebadores. Además de cebar el ADN durante la replicación, las enzimas AEP pueden tener funciones adicionales en el proceso de replicación del ADN, como la polimerización de ADN o ARN, transferencia terminal , síntesis de translesión (TLS) , unión de extremos no homólogos (NHEJ) , [12] y posiblemente al reiniciar las bifurcaciones de replicación detenidas. [15] Las primasas normalmente sintetizan cebadores a partir de ribonucleótidos (NTP); sin embargo, las primasas con capacidades polimerasas también tienen afinidad por los desoxirribonucleótidos (dNTP). [16] [11] Las primasas con funcionalidad transferasa terminal son capaces de agregar nucleótidos al extremo 3' de una cadena de ADN independientemente de una plantilla. Otras enzimas implicadas en la replicación del ADN, como las helicasas, también pueden exhibir actividad primasa. [17]
Human PrimPol (ccdc111 [16] ) cumple funciones tanto primasa como polimerasa, como muchas primasas arqueales; exhibe actividad transferasa terminal en presencia de manganeso; y desempeña un papel importante en la síntesis de translesiones [18] y en el reinicio de bifurcaciones de replicación estancadas. PrimPol se recluta activamente en los sitios dañados mediante su interacción con RPA, una proteína adaptadora que facilita la replicación y reparación del ADN. [15] PrimPol tiene un dominio de dedos de zinc similar al de algunas primasas virales, que es esencial para la síntesis de translesiones y la actividad de las primasas y puede regular la longitud del cebador. [18] A diferencia de la mayoría de primasas, PrimPol es excepcionalmente capaz de iniciar cadenas de ADN con dNTP. [dieciséis]
PriS, la subunidad pequeña de primasa arqueal, tiene un papel en la síntesis de translesiones (TLS) y puede evitar lesiones comunes del ADN. La mayoría de las arqueas carecen de las polimerasas especializadas que realizan TLS en eucariotas y bacterias. [19] PriS solo sintetiza preferentemente cadenas de ADN; pero en combinación con PriL, la subunidad grande, aumenta la actividad de la ARN polimerasa. [20]
En Sulfolobus solfataricus , el heterodímero de primasa PriSL puede actuar como primasa, polimerasa y transferasa terminal. Se cree que PriSL inicia la síntesis de cebadores con NTP y luego cambia a dNTP. La enzima puede polimerizar cadenas de ARN o ADN, y los productos de ADN alcanzan hasta 7000 nucleótidos (7 kb). Se sugiere que esta funcionalidad dual puede ser una característica común de las primasas de arqueas. [11]
Las primasas multifuncionales AEP también aparecen en bacterias y fagos que las infectan. Pueden mostrar organizaciones de dominio novedosas con dominios que aportan aún más funciones más allá de la polimerización. [14]
La LigD bacteriana ( A0R3R7 ) participa principalmente en la vía NHEJ. Tiene un dominio polimerasa/primasa de la superfamilia AEP, un dominio 3'-fosfoesterasa y un dominio ligasa. También es capaz de realizar actividad primasa, ADN y ARN polimerasa y transferasa terminal. La actividad de polimerización del ADN puede producir cadenas de más de 7000 nucleótidos (7 kb) de longitud, mientras que la polimerización del ARN produce cadenas de hasta 1 kb de longitud. [21]
Las enzimas AEP están muy extendidas y se pueden encontrar codificadas en elementos genéticos móviles, incluidos virus/fagos y plásmidos. Las utilizan como única proteína de replicación o en combinación con otras proteínas asociadas a la replicación, como las helicasas y, con menor frecuencia, las ADN polimerasas. [22] Mientras que se espera la presencia de AEP en virus eucarióticos y arqueales porque reflejan a sus huéspedes, [22] los virus bacterianos y los plásmidos también codifican con tanta frecuencia enzimas de la superfamilia AEP como lo hacen primasas de la familia DnaG. [14] Se ha descubierto una gran diversidad de familias de AEP en varios plásmidos bacterianos mediante estudios genómicos comparativos . [14] Su historia evolutiva se desconoce actualmente, ya que los que se encuentran en bacterias y bacteriófagos parecen demasiado diferentes de sus homólogos arqueoeucariotas para una transferencia genética horizontal reciente . [22]
La helicasa tipo MCM en la cepa ATCC 14579 de Bacillus cereus (BcMCM; Q81EV1 ) es una helicasa SF6 fusionada con una primasa AEP. La enzima tiene funciones primasa y polimerasa además de la función helicasa. El gen que lo codifica se encuentra en un profago. [17] Tiene homología con ORF904 del plásmido pRN1 de Sulfolobus islandicus , que tiene un dominio AEP PrimPol. [23] El virus vaccinia D5 y HSV Primase también son ejemplos de fusión AEP-helicasa. [12] [6]
PolpTN2 es una primasa de Archaeal que se encuentra en el plásmido TN2. Una fusión de dominios homólogos a PriS y PriL, exhibe actividad primasa y ADN polimerasa, así como función transferasa terminal. A diferencia de la mayoría de primasas, PolpTN2 forma cebadores compuestos exclusivamente de dNTP. [13] Inesperadamente, cuando el dominio similar a PriL se truncó, PolpTN2 también pudo sintetizar ADN en la plantilla de ARN, es decir, actuó como una ADN polimerasa dependiente de ARN (transcriptasa inversa). [13]
Incluso las primasas DnaG pueden tener funciones adicionales, si se les dan los dominios adecuados. El fago gp4 T7 es una fusión DnaG primasa-helicasa y realiza ambas funciones en la replicación. [5]