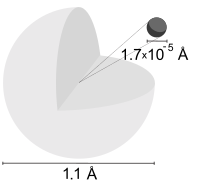
Un átomo de hidrógeno es un átomo del elemento químico hidrógeno . El átomo de hidrógeno, eléctricamente neutro, contiene un núcleo de un único protón con carga positiva y un único electrón con carga negativa unido al núcleo por la fuerza de Coulomb . El hidrógeno atómico constituye aproximadamente el 75% de la masa bariónica del universo. [1]
En la vida cotidiana en la Tierra, los átomos de hidrógeno aislados (llamados "hidrógeno atómico") son extremadamente raros. En cambio, un átomo de hidrógeno tiende a combinarse con otros átomos en compuestos, o con otro átomo de hidrógeno para formar el gas hidrógeno ordinario ( diatómico ), H2 . "Hidrógeno atómico" y "átomo de hidrógeno" en el uso común del inglés tienen significados superpuestos, pero distintos. Por ejemplo, una molécula de agua contiene dos átomos de hidrógeno, pero no contiene hidrógeno atómico (que se referiría a átomos de hidrógeno aislados).
La espectroscopia atómica muestra que existe un conjunto infinito y discreto de estados en los que puede existir un átomo de hidrógeno (o cualquier otro), contrariamente a las predicciones de la física clásica . Los intentos de desarrollar una comprensión teórica de los estados del átomo de hidrógeno han sido importantes para la historia de la mecánica cuántica , ya que todos los demás átomos pueden entenderse de manera aproximada conociendo en detalle esta estructura atómica más simple.
El isótopo más abundante , el protio ( 1 H), o hidrógeno ligero, no contiene neutrones y es simplemente un protón y un electrón . El protio es estable y constituye el 99,985 % de los átomos de hidrógeno naturales. [2]
El deuterio ( 2H ) contiene un neutrón y un protón en su núcleo. El deuterio es estable, constituye el 0,0156% del hidrógeno natural [2] y se utiliza en procesos industriales como reactores nucleares y resonancia magnética nuclear .
El tritio ( 3H ) contiene dos neutrones y un protón en su núcleo y no es estable, ya que su desintegración tiene una vida media de 12,32 años. Debido a su corta vida media, el tritio no existe en la naturaleza, salvo en cantidades mínimas.
Los isótopos más pesados del hidrógeno sólo se crean artificialmente en aceleradores de partículas y tienen vidas medias del orden de 10 −22 segundos. Son resonancias no ligadas que se encuentran más allá de la línea de goteo de neutrones ; esto da como resultado la emisión inmediata de un neutrón .
Las fórmulas siguientes son válidas para los tres isótopos del hidrógeno, pero se deben utilizar valores ligeramente diferentes de la constante de Rydberg (la fórmula de corrección se proporciona a continuación) para cada isótopo del hidrógeno.
En condiciones normales, los átomos de hidrógeno neutros solitarios son poco frecuentes. Sin embargo, el hidrógeno neutro es común cuando está unido covalentemente a otro átomo, y los átomos de hidrógeno también pueden existir en formas catiónicas y aniónicas .
Si un átomo de hidrógeno neutro pierde su electrón, se convierte en un catión. El ion resultante, que consiste únicamente en un protón para el isótopo habitual, se escribe como "H + " y a veces se lo llama hidrón . Los protones libres son comunes en el medio interestelar y en el viento solar . En el contexto de las soluciones acuosas de los ácidos de Brønsted-Lowry clásicos , como el ácido clorhídrico , en realidad se refiere al hidronio , H 3 O + . En lugar de que se forme literalmente un único átomo de hidrógeno ionizado, el ácido transfiere el hidrógeno a H 2 O, formando H 3 O + .
Si, en cambio, un átomo de hidrógeno gana un segundo electrón, se convierte en un anión. El anión hidrógeno se escribe "H – " y se denomina hidruro .
El átomo de hidrógeno tiene un significado especial en la mecánica cuántica y en la teoría cuántica de campos como un sistema físico simple de dos cuerpos que ha producido muchas soluciones analíticas simples en forma cerrada.
Los experimentos de Ernest Rutherford en 1909 mostraron que la estructura del átomo es un núcleo denso y positivo con una tenue nube de carga negativa a su alrededor. Esto planteó inmediatamente preguntas sobre cómo un sistema así podría ser estable. El electromagnetismo clásico había demostrado que cualquier carga acelerada irradia energía, como lo demuestra la fórmula de Larmor . Si se supone que el electrón orbita en un círculo perfecto e irradia energía continuamente, el electrón caería rápidamente en espiral hacia el núcleo con un tiempo de caída de: [3] donde es el radio de Bohr y es el radio clásico del electrón . Si esto fuera cierto, todos los átomos colapsarían instantáneamente, sin embargo, los átomos parecen ser estables. Además, la espiral hacia adentro liberaría una mancha de frecuencias electromagnéticas a medida que la órbita se hiciera más pequeña. En cambio, se observó que los átomos solo emitían frecuencias discretas de radiación. La resolución estaría en el desarrollo de la mecánica cuántica .
En 1913, Niels Bohr obtuvo los niveles de energía y las frecuencias espectrales del átomo de hidrógeno después de realizar una serie de suposiciones simples para corregir el modelo clásico fallido. Las suposiciones incluían:
Bohr supuso que el momento angular del electrón está cuantizado con valores posibles: donde y es la constante de Planck sobre . También supuso que la fuerza centrípeta que mantiene al electrón en su órbita es proporcionada por la fuerza de Coulomb , y que la energía se conserva. Bohr derivó la energía de cada órbita del átomo de hidrógeno como: [4] donde es la masa del electrón , es la carga del electrón , es la permitividad del vacío , y es el número cuántico (ahora conocido como el número cuántico principal ). Las predicciones de Bohr coincidieron con los experimentos de medición de la serie espectral del hidrógeno al primer orden, dando más confianza a una teoría que usaba valores cuantizados.
Para , el valor [5] se denomina unidad de energía de Rydberg. Está relacionado con la constante de Rydberg de la física atómica por
El valor exacto de la constante de Rydberg supone que el núcleo es infinitamente masivo con respecto al electrón. Para el hidrógeno-1, hidrógeno-2 ( deuterio ) e hidrógeno-3 ( tritio ), que tienen masa finita, la constante debe modificarse ligeramente para utilizar la masa reducida del sistema, en lugar de simplemente la masa del electrón. Esto incluye la energía cinética del núcleo en el problema, porque la energía cinética total (electrón más nuclear) es equivalente a la energía cinética de la masa reducida que se mueve con una velocidad igual a la velocidad del electrón en relación con el núcleo. Sin embargo, como el núcleo es mucho más pesado que el electrón, la masa del electrón y la masa reducida son casi las mismas. La constante de Rydberg RM para un átomo de hidrógeno (un electrón), R viene dada por donde es la masa del núcleo atómico. Para el hidrógeno-1, la cantidad es de aproximadamente 1/1836 (es decir, la relación de masas electrón-protón). Para el deuterio y el tritio, las relaciones son de aproximadamente 1/3670 y 1/5497 respectivamente. Estas cifras, cuando se suman a 1 en el denominador, representan correcciones muy pequeñas en el valor de R y, por lo tanto, solo pequeñas correcciones en todos los niveles de energía en los isótopos de hidrógeno correspondientes.
Todavía había problemas con el modelo de Bohr:
La mayoría de estas deficiencias se resolvieron con la modificación del modelo de Bohr por parte de Arnold Sommerfeld . Sommerfeld introdujo dos grados de libertad adicionales, lo que permite que un electrón se mueva en una órbita elíptica caracterizada por su excentricidad y declinación con respecto a un eje elegido. Esto introdujo dos números cuánticos adicionales, que corresponden al momento angular orbital y su proyección sobre el eje elegido. De este modo, se encontró la multiplicidad correcta de estados (excepto el factor 2 que explica el espín del electrón aún desconocido). Además, al aplicar la relatividad especial a las órbitas elípticas, Sommerfeld logró derivar la expresión correcta para la estructura fina de los espectros de hidrógeno (que resulta ser exactamente la misma que en la teoría de Dirac más elaborada). Sin embargo, algunos fenómenos observados, como el efecto Zeeman anómalo , permanecieron sin explicación. Estos problemas se resolvieron con el pleno desarrollo de la mecánica cuántica y la ecuación de Dirac . A menudo se afirma que la ecuación de Schrödinger es superior a la teoría de Bohr-Sommerfeld para describir el átomo de hidrógeno. No es así, ya que la mayoría de los resultados de ambos enfoques coinciden o son muy próximos (una notable excepción es el problema del átomo de hidrógeno en campos eléctricos y magnéticos cruzados, que no puede resolverse de manera autoconsistente en el marco de la teoría de Bohr-Sommerfeld), y en ambas teorías las principales deficiencias resultan de la ausencia del espín del electrón. Fue el fracaso total de la teoría de Bohr-Sommerfeld para explicar sistemas de muchos electrones (como el átomo de helio o la molécula de hidrógeno) lo que demostró su inadecuación para describir fenómenos cuánticos.
La ecuación de Schrödinger es el modelo estándar de la mecánica cuántica; permite calcular los estados estacionarios y también la evolución temporal de los sistemas cuánticos. Existen respuestas analíticas exactas para el átomo de hidrógeno no relativista. Antes de presentar una explicación formal, aquí damos una visión general elemental.
Dado que el átomo de hidrógeno contiene un núcleo y un electrón, la mecánica cuántica permite predecir la probabilidad de encontrar el electrón a cualquier distancia radial dada . Se da por el cuadrado de una función matemática conocida como " función de onda ", que es una solución de la ecuación de Schrödinger. El estado de equilibrio de energía más bajo del átomo de hidrógeno se conoce como estado fundamental. La función de onda del estado fundamental se conoce como función de onda. Se escribe como:
Aquí está el valor numérico del radio de Bohr. La densidad de probabilidad de encontrar el electrón a una distancia en cualquier dirección radial es el valor al cuadrado de la función de onda:
La función de onda es esféricamente simétrica y el área de superficie de una capa a distancia es , por lo que la probabilidad total de que el electrón esté en una capa a una distancia y un espesor es
Resulta que este es un máximo en . Es decir, la imagen de Bohr de un electrón orbitando alrededor del núcleo en el radio corresponde al radio más probable. En realidad, existe una probabilidad finita de que el electrón pueda encontrarse en cualquier lugar , con la probabilidad indicada por el cuadrado de la función de onda. Dado que la probabilidad de encontrar el electrón en algún lugar de todo el volumen es la unidad, la integral de es la unidad. Entonces decimos que la función de onda está correctamente normalizada.
Como se analiza a continuación, el estado fundamental también se indica mediante los números cuánticos . Los segundos estados de energía más bajos, justo por encima del estado fundamental, se dan mediante los números cuánticos , y . Todos estos estados tienen la misma energía y se conocen como estados y . Hay un estado: y hay tres estados:
Es más probable que un electrón en el estado o se encuentre en la segunda órbita de Bohr con la energía dada por la fórmula de Bohr.
El hamiltoniano del átomo de hidrógeno es el operador de energía cinética radial más la energía potencial electrostática de Coulomb entre el protón positivo y el electrón negativo. Utilizando la ecuación de Schrödinger independiente del tiempo, ignorando todas las interacciones de acoplamiento de espín y utilizando la masa reducida , la ecuación se escribe como:
Ampliando el Laplaciano en coordenadas esféricas:
Esta es una ecuación diferencial parcial separable que se puede resolver en términos de funciones especiales. Cuando la función de onda se separa como producto de las funciones , y aparecen tres funciones diferenciales independientes [6], donde A y B son las constantes de separación:
Las funciones de onda de posición normalizadas , dadas en coordenadas esféricas, son:
dónde:
Tenga en cuenta que los polinomios de Laguerre generalizados se definen de forma diferente según los distintos autores. El uso aquí es coherente con las definiciones utilizadas por Messiah, [7] y Mathematica. [8] En otros lugares, el polinomio de Laguerre incluye un factor de , [9] o el polinomio de Laguerre generalizado que aparece en la función de onda del hidrógeno es en su lugar. [10]
Los números cuánticos pueden tomar los siguientes valores:
Además, estas funciones de onda están normalizadas (es decir, la integral de su cuadrado de módulo es igual a 1) y son ortogonales : donde es el estado representado por la función de onda en notación de Dirac , y es la función delta de Kronecker . [11]
Las funciones de onda en el espacio de momento están relacionadas con las funciones de onda en el espacio de posición a través de una transformada de Fourier que, para los estados ligados, da como resultado [12] donde denota un polinomio de Gegenbauer y está en unidades de .
Las soluciones de la ecuación de Schrödinger para el hidrógeno son analíticas , dan una expresión simple para los niveles de energía del hidrógeno y, por lo tanto, las frecuencias de las líneas espectrales del hidrógeno y reproducen completamente el modelo de Bohr y lo superan. También proporciona otros dos números cuánticos y la forma de la función de onda del electrón ("orbital") para los diversos estados mecánico-cuánticos posibles, lo que explica el carácter anisotrópico de los enlaces atómicos.
La ecuación de Schrödinger también se aplica a átomos y moléculas más complejos . Cuando hay más de un electrón o núcleo, la solución no es analítica y se necesitan cálculos informáticos o bien se deben hacer suposiciones simplificadoras.
Como la ecuación de Schrödinger sólo es válida para la mecánica cuántica no relativista, las soluciones que arroja para el átomo de hidrógeno no son del todo correctas. La ecuación de Dirac de la teoría cuántica relativista mejora estas soluciones (véase más abajo).
La solución de la ecuación de Schrödinger (ecuación de onda) para el átomo de hidrógeno utiliza el hecho de que el potencial de Coulomb producido por el núcleo es isótropo (es radialmente simétrico en el espacio y solo depende de la distancia al núcleo). Aunque las funciones propias de energía resultantes (los orbitales ) no son necesariamente isótropas en sí mismas, su dependencia de las coordenadas angulares se sigue de manera completamente general de esta isotropía del potencial subyacente: los estados propios del hamiltoniano (es decir, los estados propios de energía) pueden elegirse como estados propios simultáneos del operador de momento angular . Esto corresponde al hecho de que el momento angular se conserva en el movimiento orbital del electrón alrededor del núcleo. Por lo tanto, los estados propios de energía pueden clasificarse por dos números cuánticos de momento angular , y (ambos son números enteros). El número cuántico de momento angular determina la magnitud del momento angular. El número cuántico magnético determina la proyección del momento angular sobre el eje (elegido arbitrariamente) .
Además de las expresiones matemáticas para el momento angular total y la proyección del momento angular de las funciones de onda, se debe encontrar una expresión para la dependencia radial de las funciones de onda. Es sólo aquí donde entran en juego los detalles del potencial de Coulomb (que conduce a los polinomios de Laguerre en ). Esto conduce a un tercer número cuántico, el número cuántico principal . El número cuántico principal en el hidrógeno está relacionado con la energía total del átomo.
Téngase en cuenta que el valor máximo del número cuántico del momento angular está limitado por el número cuántico principal: solo puede alcanzar , es decir, .
Debido a la conservación del momento angular, los estados iguales pero diferentes tienen la misma energía (esto se aplica a todos los problemas con simetría rotacional ). Además, para el átomo de hidrógeno, los estados iguales pero diferentes también son degenerados (es decir, tienen la misma energía). Sin embargo, esta es una propiedad específica del hidrógeno y ya no es cierta para átomos más complejos que tienen un potencial (efectivo) diferente de la forma (debido a la presencia de los electrones internos que protegen el potencial del núcleo).
Teniendo en cuenta el espín del electrón, se añade un último número cuántico, la proyección del momento angular de espín del electrón a lo largo del eje , que puede adoptar dos valores. Por lo tanto, cualquier estado propio del electrón en el átomo de hidrógeno se describe completamente mediante cuatro números cuánticos. De acuerdo con las reglas habituales de la mecánica cuántica, el estado real del electrón puede ser cualquier superposición de estos estados. Esto explica también por qué la elección del eje para la cuantificación direccional del vector de momento angular es irrelevante: un orbital de dado y obtenido para otro eje preferido siempre se puede representar como una superposición adecuada de los diversos estados de diferentes (pero iguales ) que se han obtenido para .
En 1928, Paul Dirac encontró una ecuación que era totalmente compatible con la relatividad especial y (como consecuencia) convirtió la función de onda en un " espinor de Dirac " de 4 componentes que incluía componentes de espín "arriba" y "abajo", con energía tanto positiva como "negativa" (o materia y antimateria). La solución de esta ecuación dio los siguientes resultados, más precisos que la solución de Schrödinger.
Los niveles de energía del hidrógeno, incluyendo la estructura fina (excluyendo el desplazamiento de Lamb y la estructura hiperfina ), se dan mediante la expresión de estructura fina de Sommerfeld : [13] donde es la constante de estructura fina y es el número cuántico de momento angular total , que es igual a , dependiendo de la orientación del espín del electrón en relación con el momento angular orbital. [14] Esta fórmula representa una pequeña corrección a la energía obtenida por Bohr y Schrödinger como se indica anteriormente. El factor entre corchetes en la última expresión es casi uno; el término adicional surge de efectos relativistas (para más detalles, consulte #Características que van más allá de la solución de Schrödinger). Vale la pena señalar que esta expresión fue obtenida por primera vez por A. Sommerfeld en 1916 basándose en la versión relativista de la antigua teoría de Bohr . Sin embargo, Sommerfeld ha utilizado una notación diferente para los números cuánticos.
La imagen de la derecha muestra los primeros orbitales de los átomos de hidrógeno (funciones propias de energía). Se trata de secciones transversales de la densidad de probabilidad que están codificadas por colores (el negro representa la densidad cero y el blanco la densidad más alta). El número cuántico del momento angular (orbital) ℓ se indica en cada columna, utilizando el código de letras espectroscópico habitual ( s significa ℓ = 0, p significa ℓ = 1, d significa ℓ = 2). El número cuántico principal n (= 1, 2, 3, ...) está marcado a la derecha de cada fila. Para todas las imágenes, el número cuántico magnético m se ha establecido en 0 y el plano de la sección transversal es el plano xz ( z es el eje vertical). La densidad de probabilidad en el espacio tridimensional se obtiene rotando la que se muestra aquí alrededor del eje z .
El " estado fundamental ", es decir, el estado de menor energía, en el que habitualmente se encuentra el electrón, es el primero, el estado 1 s ( nivel cuántico principal n = 1, ℓ = 0).
Las líneas negras aparecen en todos los orbitales, excepto en el primero: son los nodos de la función de onda, es decir, donde la densidad de probabilidad es cero. (Más precisamente, los nodos son armónicos esféricos que aparecen como resultado de resolver la ecuación de Schrödinger en coordenadas esféricas).
Los números cuánticos determinan la disposición de estos nodos. Son: [ cita requerida ]

La frecuencia de un estado en el nivel n es , por lo que en caso de una superposición de múltiples orbitales, oscilarían debido a la diferencia de frecuencia. Por ejemplo, dos estados, ψ 1 y ψ 2 : La función de onda está dada por y la función de probabilidad es

El resultado es una función de onda rotatoria. El movimiento de los electrones y el cambio de estados cuánticos irradian luz a una frecuencia del coseno.
Hay varios efectos importantes que la ecuación de Schrödinger no tiene en cuenta y que son responsables de ciertas desviaciones pequeñas pero mensurables de las líneas espectrales reales respecto de las previstas:
Ambas características (y más) están incorporadas en la ecuación relativista de Dirac , con predicciones que se acercan aún más a la experimentación. Nuevamente, la ecuación de Dirac puede resolverse analíticamente en el caso especial de un sistema de dos cuerpos, como el átomo de hidrógeno. Los estados cuánticos de solución resultantes ahora deben clasificarse por el número de momento angular total j (que surge a través del acoplamiento entre el espín del electrón y el momento angular orbital ). Los estados del mismo j y el mismo n todavía están degenerados. Por lo tanto, la solución analítica directa de la ecuación de Dirac predice 2S( 1/2 ) y 2P( 1/2) los niveles de hidrógeno tienen exactamente la misma energía, lo que está en contradicción con las observaciones ( experimento de Lamb–Retherford ).
Para estos avances era esencial que la solución de la ecuación de Dirac para el átomo de hidrógeno pudiera calcularse con exactitud, de modo que cualquier desviación observada experimentalmente debía tomarse seriamente como una señal de fracaso de la teoría.
En el lenguaje de la mecánica matricial de Heisenberg , el átomo de hidrógeno fue resuelto por primera vez por Wolfgang Pauli [15] utilizando una simetría rotacional en cuatro dimensiones [O(4)-simetría] generada por el momento angular y el vector de Laplace–Runge–Lenz . Al extender el grupo de simetría O(4) al grupo dinámico O(4,2), todo el espectro y todas las transiciones se integraron en una única representación de grupo irreducible. [16]
En 1979, el átomo de hidrógeno (no relativista) fue resuelto por primera vez dentro de la formulación integral de trayectorias de Feynman de la mecánica cuántica por Duru y Kleinert. [17] [18] Este trabajo amplió enormemente el rango de aplicabilidad del método de Feynman .
Otros modelos alternativos son la mecánica de Böhm y la compleja formulación de Hamilton-Jacobi de la mecánica cuántica .