
Metaloproteína es un término genérico para una proteína que contiene un cofactor de iones metálicos . [1] [2] Una gran proporción de todas las proteínas forman parte de esta categoría. Por ejemplo, al menos 1000 proteínas humanas (de un total de ~20 000) contienen dominios proteicos de unión al zinc [3], aunque puede haber hasta 3000 metaloproteínas de zinc humanas. [4]
Se estima que aproximadamente la mitad de todas las proteínas contienen un metal . [5] En otra estimación, se propone que aproximadamente entre un cuarto y un tercio de todas las proteínas requieren metales para llevar a cabo sus funciones. [6] Por lo tanto, las metaloproteínas tienen muchas funciones diferentes en las células , como el almacenamiento y transporte de proteínas, enzimas y proteínas de transducción de señales , o enfermedades infecciosas. [7] La abundancia de proteínas de unión a metales puede ser inherente a los aminoácidos que utilizan las proteínas, ya que incluso las proteínas artificiales sin historia evolutiva se unirán fácilmente a los metales. [8]
La mayoría de los metales presentes en el cuerpo humano están ligados a las proteínas. Por ejemplo, la concentración relativamente alta de hierro en el cuerpo humano se debe principalmente al hierro presente en la hemoglobina .
En las metaloproteínas, los iones metálicos suelen estar coordinados por centros de nitrógeno , oxígeno o azufre que pertenecen a los residuos de aminoácidos de la proteína. Estos grupos donantes suelen estar provistos por cadenas laterales en los residuos de aminoácidos. Especialmente importantes son el sustituyente imidazol en los residuos de histidina , los sustituyentes tiolato en los residuos de cisteína y los grupos carboxilato proporcionados por el aspartato . Dada la diversidad del metaloproteoma , se ha demostrado que prácticamente todos los residuos de aminoácidos se unen a centros metálicos. La cadena principal del péptido también proporciona grupos donantes; estos incluyen amidas desprotonadas y los centros de oxígeno carbonílico de amida . Se ha revisado la unión del plomo (II) en proteínas naturales y artificiales. [10]
Además de los grupos donantes que proporcionan los residuos de aminoácidos, muchos cofactores orgánicos funcionan como ligandos. Quizás los más famosos sean los ligandos macrocíclicos tetradentados N 4 incorporados a la proteína hemo . Los ligandos inorgánicos como el sulfuro y el óxido también son comunes.
Estos son el producto de la segunda etapa de la hidrólisis de proteínas, obtenido por tratamiento con ácidos y álcalis ligeramente más fuertes.
La hemoglobina , que es el principal transportador de oxígeno en los seres humanos, tiene cuatro subunidades en las que el ion hierro (II) está coordinado por el ligando macrocíclico planar protoporfirina IX (PIX) y el átomo de nitrógeno imidazol de un residuo de histidina . El sexto sitio de coordinación contiene una molécula de agua o una molécula de dioxígeno . Por el contrario, la proteína mioglobina , que se encuentra en las células musculares , tiene solo una de estas unidades. El sitio activo está ubicado en una bolsa hidrófoba . Esto es importante ya que sin él, el hierro (II) se oxidaría irreversiblemente a hierro (III). La constante de equilibrio para la formación de HbO 2 es tal que el oxígeno se absorbe o se libera dependiendo de la presión parcial de oxígeno en los pulmones o en el músculo. En la hemoglobina, las cuatro subunidades muestran un efecto de cooperatividad que permite una fácil transferencia de oxígeno de la hemoglobina a la mioglobina. [11]
En la hemoglobina y la mioglobina, a veces se afirma incorrectamente que las especies oxigenadas contienen hierro (III). Ahora se sabe que la naturaleza diamagnética de estas especies se debe a que el átomo de hierro (II) está en el estado de espín bajo . En la oxihemoglobina, el átomo de hierro se encuentra en el plano del anillo de porfirina, pero en la desoxihemoglobina paramagnética, el átomo de hierro se encuentra por encima del plano del anillo. [11] Este cambio en el estado de espín es un efecto cooperativo debido a la mayor división del campo cristalino y al menor radio iónico del Fe 2+ en la fracción de oxihemoglobina.
La hemeritrina es otro transportador de oxígeno que contiene hierro. El sitio de unión del oxígeno es un centro de hierro binuclear. Los átomos de hierro se coordinan con la proteína a través de las cadenas laterales de carboxilato de un glutamato y aspartato y cinco residuos de histidina . La captación de O 2 por la hemeritrina va acompañada de una oxidación de dos electrones del centro binuclear reducido para producir peróxido unido (OOH − ). El mecanismo de captación y liberación de oxígeno se ha estudiado en detalle. [12] [13]
Las hemocianinas transportan oxígeno en la sangre de la mayoría de los moluscos y algunos artrópodos como el cangrejo herradura . Ocupan el segundo lugar después de la hemoglobina en popularidad biológica en el transporte de oxígeno. En la oxigenación, los dos átomos de cobre (I) en el sitio activo se oxidan a cobre (II) y las moléculas de dioxígeno se reducen a peróxido, O2−
2. [14] [15]
La clorocruorina (como el transportador más grande, la eritrocruorina ) es una hemoproteína que se une al oxígeno presente en el plasma sanguíneo de muchos anélidos , particularmente ciertos poliquetos marinos .
Las reacciones de oxidación y reducción no son comunes en la química orgánica , ya que pocas moléculas orgánicas pueden actuar como agentes oxidantes o reductores . El hierro (II), por otro lado, puede oxidarse fácilmente a hierro (III). Esta funcionalidad se utiliza en los citocromos , que funcionan como vectores de transferencia de electrones . La presencia del ion metálico permite que las metaloenzimas realicen funciones como reacciones redox que no pueden ser realizadas fácilmente por el conjunto limitado de grupos funcionales que se encuentran en los aminoácidos . [16] El átomo de hierro en la mayoría de los citocromos está contenido en un grupo hemo . Las diferencias entre esos citocromos radican en las diferentes cadenas laterales. Por ejemplo, el citocromo a tiene un grupo prostético hemo a y el citocromo b tiene un grupo prostético hemo b . Estas diferencias dan como resultado diferentes potenciales redox Fe 2+ /Fe 3+ de modo que varios citocromos están involucrados en la cadena de transporte de electrones mitocondrial . [17]
Las enzimas del citocromo P450 realizan la función de insertar un átomo de oxígeno en un enlace C−H, una reacción de oxidación. [18] [19]
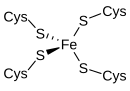
La rubredoxina es un transportador de electrones que se encuentra en bacterias y arqueas que metabolizan azufre . El sitio activo contiene un ion de hierro coordinado por los átomos de azufre de cuatro residuos de cisteína que forman un tetraedro casi regular . Las rubredoxinas realizan procesos de transferencia de un electrón. El estado de oxidación del átomo de hierro varía entre los estados +2 y +3. En ambos estados de oxidación el metal tiene un espín alto , lo que ayuda a minimizar los cambios estructurales.
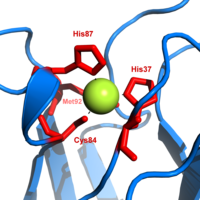
La plastocianina es una de las proteínas azules de cobre que participan en las reacciones de transferencia de electrones . El sitio de unión del cobre se describe como una pirámide trigonal distorsionada . [20] El plano trigonal de la base piramidal está compuesto por dos átomos de nitrógeno (N 1 y N 2 ) de histidinas separadas y un azufre (S 1 ) de una cisteína. El azufre (S 2 ) de una metionina axial forma el ápice. La distorsión se produce en las longitudes de enlace entre los ligandos de cobre y azufre. El contacto Cu−S 1 es más corto (207 pm ) que el Cu−S 2 (282 pm). El enlace Cu−S 2 alargado desestabiliza la forma Cu(II) y aumenta el potencial redox de la proteína. El color azul (pico de absorción de 597 nm ) se debe al enlace Cu−S 1 donde se produce la transferencia de carga de S(pπ) a Cu(d x 2 − y 2 ). [21]
En la forma reducida de plastocianina, la His -87 se protonará con un p K a de 4,4. La protonación evita que actúe como ligando y la geometría del sitio de cobre se vuelve trigonal plana .
El hierro se almacena como hierro(III) en la ferritina . La naturaleza exacta del sitio de unión aún no se ha determinado. El hierro parece estar presente como un producto de hidrólisis como FeO(OH). El hierro es transportado por la transferrina cuyo sitio de unión consiste en dos tirosinas , una de ácido aspártico y una de histidina . [22] El cuerpo humano no tiene un mecanismo controlado para la excreción de hierro. [23] Esto puede conducir a problemas de sobrecarga de hierro en pacientes tratados con transfusiones de sangre , como, por ejemplo, con β- talasemia . El hierro se excreta en la orina [24] y también se concentra en la bilis [25] que se excreta en las heces. [26]
La ceruloplasmina es la principal proteína transportadora de cobre en la sangre. La ceruloplasmina exhibe actividad oxidasa, que está asociada con la posible oxidación de Fe(II) a Fe(III), por lo que ayuda a su transporte en el plasma sanguíneo en asociación con la transferrina, que puede transportar hierro solo en el estado Fe(III).
La osteopontina participa en la mineralización de las matrices extracelulares de los huesos y los dientes.
Todas las metaloenzimas tienen una característica en común: el ion metálico está unido a la proteína mediante un sitio de coordinación lábil . Como ocurre con todas las enzimas , la forma del sitio activo es crucial. El ion metálico suele estar ubicado en una cavidad cuya forma se adapta al sustrato. El ion metálico cataliza reacciones que son difíciles de lograr en la química orgánica .
En solución acuosa , el dióxido de carbono forma ácido carbónico.
Esta reacción es muy lenta en ausencia de un catalizador, pero bastante rápida en presencia del ion hidróxido .
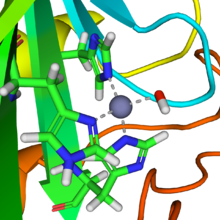
Una reacción similar a ésta es casi instantánea con la anhidrasa carbónica . La estructura del sitio activo en las anhidrasas carbónicas es bien conocida a partir de varias estructuras cristalinas. Consiste en un ion de cinc coordinado por tres átomos de nitrógeno de imidazol de tres unidades de histidina . El cuarto sitio de coordinación está ocupado por una molécula de agua. La esfera de coordinación del ion de cinc es aproximadamente tetraédrica . El ion de cinc cargado positivamente polariza la molécula de agua coordinada, y el ataque nucleofílico por la porción de hidróxido cargada negativamente sobre el dióxido de carbono procede rápidamente. El ciclo catalítico produce el ion de bicarbonato y el ion de hidrógeno [2] como equilibrio :
favoreciendo la disociación del ácido carbónico a valores de pH biológicos . [27]
La vitamina B 12 que contiene cobalto (también conocida como cobalamina) cataliza la transferencia de grupos metilo (−CH 3 ) entre dos moléculas, lo que implica la ruptura de enlaces C−C , un proceso que es energéticamente costoso en reacciones orgánicas. El ion metálico reduce la energía de activación del proceso al formar un enlace transitorio Co−CH 3 . [28] La estructura de la coenzima fue determinada por Dorothy Hodgkin y colaboradores, por lo que recibió un Premio Nobel de Química . [29] Consiste en un ion cobalto (II) coordinado a cuatro átomos de nitrógeno de un anillo de corrina y un quinto átomo de nitrógeno de un grupo imidazol . En el estado de reposo hay un enlace sigma Co−C con el átomo de carbono 5' de la adenosina . [30] Se trata de un compuesto organometálico de origen natural , lo que explica su función en reacciones de transmetilación , como la reacción que lleva a cabo la metionina sintasa .
La fijación del nitrógeno atmosférico es un proceso que consume mucha energía, ya que implica romper el triple enlace muy estable entre los átomos de nitrógeno. Las nitrogenasas catalizan el proceso. Una de estas enzimas se encuentra en la bacteria Rhizobium . Hay tres componentes en su acción: un átomo de molibdeno en el sitio activo, grupos de hierro-azufre que participan en el transporte de los electrones necesarios para reducir el nitrógeno y una abundante fuente de energía en forma de ATP de magnesio . Este último es proporcionado por una simbiosis mutualista entre la bacteria y una planta huésped, a menudo una leguminosa . La reacción puede escribirse simbólicamente como
donde P i representa fosfato inorgánico . La estructura precisa del sitio activo ha sido difícil de determinar. Parece contener un grupo MoFe 7 S 8 que es capaz de unirse a la molécula de dinitrógeno y, presumiblemente, permitir que comience el proceso de reducción. [31] Los electrones son transportados por el grupo "P" asociado, que contiene dos grupos cúbicos Fe 4 S 4 unidos por puentes de azufre. [32]

El ion superóxido , O−
2Se genera en sistemas biológicos por reducción del oxígeno molecular . Tiene un electrón desapareado , por lo que se comporta como un radical libre . Es un poderoso agente oxidante . Estas propiedades hacen que el ion superóxido sea muy tóxico y los fagocitos lo utilizan para matar microorganismos invasores . De lo contrario, el ion superóxido debe destruirse antes de que cause daños no deseados en una célula. Las enzimas superóxido dismutasas realizan esta función de manera muy eficiente. [33]
El estado de oxidación formal de los átomos de oxígeno es − 1 ⁄ 2 . En soluciones a pH neutro , el ion superóxido se desproporciona con el oxígeno molecular y el peróxido de hidrógeno .
En biología, este tipo de reacción se denomina reacción de dismutación e implica tanto la oxidación como la reducción de iones superóxido. El grupo de enzimas superóxido dismutasa (SOD) aumenta la velocidad de reacción hasta cerca de la velocidad limitada por la difusión. [34] La clave de la acción de estas enzimas es un ion metálico con un estado de oxidación variable que puede actuar como agente oxidante o como agente reductor.
En la SOD humana, el metal activo es el cobre , como Cu(II) o Cu(I), coordinado tetraédricamente por cuatro residuos de histidina . Esta enzima también contiene iones de zinc para la estabilización y es activada por la chaperona de cobre para la superóxido dismutasa ( CCS ). Otras isoenzimas pueden contener hierro , manganeso o níquel . La actividad de Ni-SOD involucra níquel(III), un estado de oxidación inusual para este elemento. La geometría del sitio activo del níquel cicla desde Ni(II) plano cuadrado , con ligandos de tiolato (Cys 2 y Cys 6 ) y nitrógeno de la cadena principal (His 1 y Cys 2 ), hasta Ni(III) piramidal cuadrado con un ligando de cadena lateral axial His 1 agregado . [35]

La clorofila desempeña un papel crucial en la fotosíntesis . Contiene magnesio encerrado en un anillo de clorina . Sin embargo, el ion magnesio no participa directamente en la función fotosintética y puede ser reemplazado por otros iones divalentes con poca pérdida de actividad. En cambio, el fotón es absorbido por el anillo de clorina, cuya estructura electrónica está bien adaptada para este propósito.
Inicialmente, la absorción de un fotón hace que un electrón se excite a un estado singlete de la banda Q. El estado excitado sufre un cruce intersistema desde el estado singlete a un estado triplete en el que hay dos electrones con espín paralelo . Esta especie es, en efecto, un radical libre , y es muy reactiva y permite que un electrón se transfiera a aceptores que están adyacentes a la clorofila en el cloroplasto . En el proceso, la clorofila se oxida. Más adelante en el ciclo fotosintético, la clorofila se reduce nuevamente. Esta reducción finalmente extrae electrones del agua, produciendo oxígeno molecular como producto final de la oxidación.
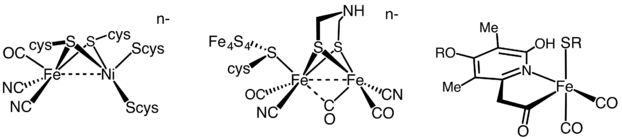
Las hidrogenasas se subclasifican en tres tipos diferentes según el contenido de metal del sitio activo: hidrogenasa de hierro-hierro, hidrogenasa de níquel-hierro e hidrogenasa de hierro. [36] Todas las hidrogenasas catalizan la captación reversible de H 2 , pero mientras que las hidrogenasas [FeFe] y [NiFe] son verdaderos catalizadores redox , que impulsan la oxidación de H 2 y la reducción de H +
Las [Fe] hidrogenasas catalizan la escisión heterolítica reversible de H 2 .
Desde el descubrimiento de las ribozimas por Thomas Cech y Sidney Altman a principios de la década de 1980, se ha demostrado que las ribozimas son una clase distinta de metaloenzimas. [37] Muchas ribozimas requieren iones metálicos en sus sitios activos para la catálisis química; por lo tanto, se las llama metaloenzimas. Además, los iones metálicos son esenciales para la estabilización estructural de las ribozimas. El intrón del grupo I es la ribozima más estudiada que tiene tres metales que participan en la catálisis. [38] Otras ribozimas conocidas incluyen el intrón del grupo II , la ARNasa P y varias ribozimas virales pequeñas (como hammerhead , hairpin , HDV y VS ) y la subunidad grande de los ribosomas. Se han descrito varias clases de ribozimas. [39]
Las desoxirribozimas , también llamadas ADNzimas o ADN catalítico, son catalizadores artificiales basados en ADN que se produjeron por primera vez en 1994. [40] Casi todas las ADNzimas requieren iones metálicos. Aunque las ribozimas catalizan principalmente la escisión de sustratos de ARN, las ADNzimas pueden catalizar una variedad de reacciones, incluida la escisión de ARN/ADN, la ligación de ARN/ADN, la fosforilación y desfosforilación de aminoácidos y la formación de enlaces carbono-carbono. [41] Sin embargo, las ADNzimas que catalizan la reacción de escisión de ARN son las más exploradas. 10-23 La ADNzima, descubierta en 1997, es uno de los ADN catalíticos más estudiados con aplicaciones clínicas como agente terapéutico. [42] Se han informado varias ADNzimas específicas de metales, incluidas la ADNzima GR-5 ( específica del plomo ), [43] las ADNzimas CA1-3 ( específicas del cobre ), la ADNzima 39E ( específica del uranilo ) [44] y la ADNzima NaA43 ( específica del sodio ). [45]

La calmodulina es un ejemplo de proteína de transducción de señales. Es una proteína pequeña que contiene cuatro motivos EF-hand , cada uno de los cuales es capaz de unirse a un ion Ca 2+ .
En un dominio proteico de bucle de mano EF , el ion calcio está coordinado en una configuración bipiramidal pentagonal. Seis residuos de ácido glutámico y ácido aspártico involucrados en la unión están en las posiciones 1, 3, 5, 7 y 9 de la cadena polipeptídica. En la posición 12, hay un ligando de glutamato o aspartato que se comporta como un ligando bidentado , proporcionando dos átomos de oxígeno. El noveno residuo en el bucle es necesariamente glicina debido a los requisitos conformacionales de la cadena principal. La esfera de coordinación del ion calcio contiene solo átomos de oxígeno de carboxilato y ningún átomo de nitrógeno. Esto es consistente con la naturaleza dura del ion calcio.
La proteína tiene dos dominios aproximadamente simétricos, separados por una región "bisagra" flexible. La unión del calcio provoca un cambio conformacional en la proteína. La calmodulina participa en un sistema de señalización intracelular actuando como un segundo mensajero difusible a los estímulos iniciales. [46] [47]
Tanto en los músculos cardíacos como en los esqueléticos , la producción de fuerza muscular está controlada principalmente por cambios en la concentración intracelular de calcio . En general, cuando el calcio aumenta, los músculos se contraen y, cuando el calcio disminuye, los músculos se relajan. La troponina , junto con la actina y la tropomiosina , es el complejo proteico al que se une el calcio para desencadenar la producción de fuerza muscular.
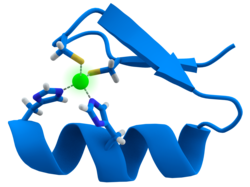
Muchos factores de transcripción contienen una estructura conocida como dedo de zinc , un módulo estructural en el que una región de proteína se pliega alrededor de un ion de zinc. El zinc no entra en contacto directo con el ADN al que se unen estas proteínas. En cambio, el cofactor es esencial para la estabilidad de la cadena proteica fuertemente plegada. [48] En estas proteínas, el ion de zinc suele estar coordinado por pares de cadenas laterales de cisteína e histidina.
Existen dos tipos de deshidrogenasa de monóxido de carbono : una contiene hierro y molibdeno, la otra contiene hierro y níquel. Se han analizado los paralelismos y las diferencias en las estrategias catalíticas. [49]
El Pb 2+ (plomo) puede reemplazar al Ca 2+ (calcio), como por ejemplo con la calmodulina , o al Zn 2+ (zinc), como por ejemplo con las metalocarboxipeptidasas . [50]
En la siguiente tabla se dan algunas otras metaloenzimas, según el metal involucrado.
{{cite book}}: |journal=ignorado ( ayuda ){{cite book}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ){{cite book}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ){{cite book}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ){{cite book}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ){{cite book}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace )