En química inorgánica , el bicarbonato ( nomenclatura recomendada por la IUPAC : hidrogenocarbonato [2] ) es una forma intermedia en la desprotonación del ácido carbónico . Es un anión poliatómico con la fórmula química H C O−
3.
El bicarbonato desempeña un papel bioquímico crucial en el sistema amortiguador del pH fisiológico . [3]
El término "bicarbonato" fue acuñado en 1814 por el químico inglés William Hyde Wollaston . [4] [5] El nombre sigue vivo como un nombre trivial .
El ion bicarbonato (ion hidrogenocarbonato) es un anión con la fórmula empírica HCO−
3y una masa molecular de 61,01 daltons ; Consiste en un átomo de carbono central rodeado por tres átomos de oxígeno en una disposición plana trigonal , con un átomo de hidrógeno unido a uno de los oxígenos. Es isoelectrónico con ácido nítrico HNO
3. El ion bicarbonato lleva una carga formal negativa y es una especie anfiprótica que tiene propiedades tanto ácidas como básicas. Es a la vez la base conjugada del ácido carbónico H.
2CO
3; y el ácido conjugado de CO2-3
, el ion carbonato , como lo muestran estas reacciones de equilibrio :
Una sal de bicarbonato se forma cuando un ion cargado positivamente se une a los átomos de oxígeno cargados negativamente del ion, formando un compuesto iónico . Muchos bicarbonatos son solubles en agua a temperatura y presión estándar ; en particular, el bicarbonato de sodio contribuye al total de sólidos disueltos , un parámetro común para evaluar la calidad del agua . [6]
Bicarbonato ( HCO−
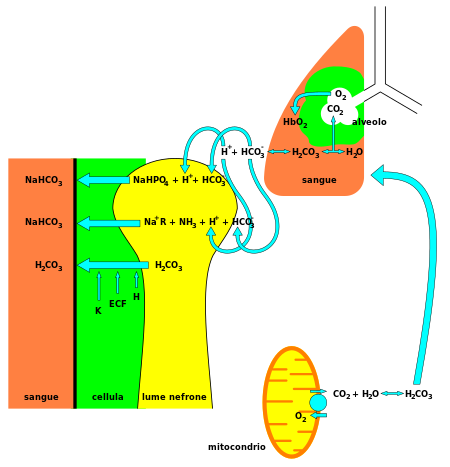
3) es un componente vital del sistema amortiguador del pH [3] del cuerpo humano (manteniendo la homeostasis ácido-base ). Entre el 70% y el 75% del CO 2 del cuerpo se convierte en ácido carbónico (H 2 CO 3 ), que es el ácido conjugado del HCO.−
3y puede convertirse rápidamente en ello. [ cita necesaria ]
Con el ácido carbónico como especie intermedia central , el bicarbonato (junto con agua, iones de hidrógeno y dióxido de carbono ) forma este sistema amortiguador, que se mantiene en el equilibrio volátil [3] necesario para proporcionar una resistencia rápida a los cambios de pH tanto en el medio ácido como en el medio ambiente. y direcciones básicas . Esto es especialmente importante para proteger los tejidos del sistema nervioso central , donde los cambios de pH demasiado fuera del rango normal en cualquier dirección podrían resultar desastrosos (ver acidosis o alcalosis ). Recientemente también se ha demostrado que el metabolismo del bicarbonato celular puede regularse mediante la señalización de mTORC1. [7]
Además, el bicarbonato juega un papel clave en el sistema digestivo. Eleva el pH interno del estómago, una vez que los jugos digestivos altamente ácidos han terminado en la digestión de los alimentos. El bicarbonato también actúa para regular el pH en el intestino delgado. Se libera del páncreas en respuesta a la hormona secretina para neutralizar el quimo ácido que ingresa al duodeno desde el estómago. [8]
El bicarbonato es la forma dominante de carbono inorgánico disuelto en el agua de mar [9] y en la mayoría de las aguas dulces. Como tal, es un sumidero importante en el ciclo del carbono .
Algunas plantas como Chara utilizan carbonato y producen carbonato de calcio (CaCO 3 ) como resultado del metabolismo biológico. [10]
En la ecología de agua dulce, la fuerte actividad fotosintética de las plantas de agua dulce durante el día libera oxígeno gaseoso al agua y al mismo tiempo produce iones de bicarbonato. Estos aumentan el pH hasta que, en determinadas circunstancias, el grado de alcalinidad puede volverse tóxico para algunos organismos o puede hacer que otros componentes químicos, como el amoníaco, sean tóxicos. En la oscuridad, cuando no se produce la fotosíntesis, los procesos respiratorios liberan dióxido de carbono y no se producen nuevos iones de bicarbonato, lo que provoca una rápida caída del pH. [ cita necesaria ]
El flujo de iones de bicarbonato de las rocas erosionadas por el ácido carbónico del agua de lluvia es una parte importante del ciclo del carbono .
La sal más común del ion bicarbonato es el bicarbonato de sodio , NaHCO 3 , que comúnmente se conoce como bicarbonato de sodio . Cuando se calienta o se expone a un ácido como el ácido acético ( vinagre ), el bicarbonato de sodio libera dióxido de carbono . Se utiliza como agente leudante en repostería . [ cita necesaria ]
El bicarbonato de amonio se utiliza en la fabricación de galletas digestivas . [ cita necesaria ]
En medicina de diagnóstico , el valor del bicarbonato en sangre es uno de varios indicadores del estado de la fisiología ácido-base del cuerpo. Se mide, junto con el cloruro , el potasio y el sodio , para evaluar los niveles de electrolitos en una prueba de panel de electrolitos (que tiene Terminología de procedimiento actual , CPT, código 80051). [ cita necesaria ]
El parámetro concentración estándar de bicarbonato (SBC e ) es la concentración de bicarbonato en sangre a una Pa CO 2 de 40 mmHg (5,33 kPa), saturación total de oxígeno y 36 °C. [11]

El indicador más común de la calidad del agua es la concentración de sólidos disueltos totales (TDS)