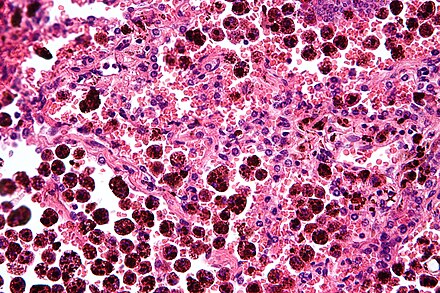
Un macrófago alveolar , macrófago pulmonar , (o célula de polvo ) es un tipo de macrófago , un fagocito profesional , que se encuentra en las vías respiratorias y a nivel de los alvéolos de los pulmones , pero separado de sus paredes. [1]
La actividad de los macrófagos alveolares es relativamente alta, ya que se encuentran en uno de los principales límites entre el cuerpo y el mundo exterior. Son los encargados de eliminar partículas como polvo o microorganismos de las superficies respiratorias.
Con frecuencia se observa que los macrófagos alveolares contienen gránulos de material exógeno, como partículas de carbono , que han recogido de las superficies respiratorias. Estos gránulos negros pueden ser especialmente comunes en los pulmones de los fumadores o de los habitantes de ciudades que viven mucho tiempo en la ciudad.
El macrófago alveolar es el tercer tipo de célula del alvéolo; los otros son los neumocitos tipo I y tipo II .



Los macrófagos alveolares son fagocitos que desempeñan un papel fundamental en la homeostasis , la defensa del huésped y la remodelación tisular. [7] Su densidad de población es decisiva para estos numerosos procesos. Son muy adaptables y pueden liberar muchas secreciones para interactuar con otras células y moléculas utilizando varios receptores de superficie . Los macrófagos alveolares también participan en la fagocitosis de células apoptóticas y necróticas. [8] Deben ser selectivos del material que se fagocita para salvaguardar las células y estructuras normales. [8] Para combatir la infección, los fagocitos facilitan muchos receptores de reconocimiento de patrones (PRR) para ayudar a reconocer patrones moleculares asociados a patógenos (PAMP) en la superficie de los microorganismos patógenos. [9] Todos los PAMP tienen las características comunes de ser exclusivos de un grupo de patógenos pero invariables en su estructura básica; y son esenciales para la patogenicidad (capacidad de un organismo para producir una enfermedad infecciosa en otro organismo). [9] Las proteínas implicadas en el reconocimiento de patrones microbianos incluyen el receptor de manosa, los receptores del complemento, DC-SIGN, los receptores tipo Toll (TLR), el receptor scavenger, CD14 y Mac-1. [9] [10] Los PRR se pueden dividir en tres clases:
El reconocimiento y la eliminación de microorganismos invasores se produce a través de vías dependientes e independientes de la opsonina. Los mecanismos moleculares que facilitan la fagocitosis dependiente de la opsonina son diferentes para pares específicos de opsonina/receptor. Por ejemplo, la fagocitosis de patógenos opsonizados por IgG se produce a través de los receptores Fcγ (FcγR) e implica extensiones de fagocitos alrededor del microbio, lo que da como resultado la producción de mediadores proinflamatorios. Por el contrario, la ingestión de patógenos mediada por el receptor del complemento se produce sin extensiones de membrana observables (las partículas simplemente se hunden en la célula) y generalmente no da como resultado una respuesta de mediador inflamatorio.
Tras la internalización, el microbio queda encerrado en un fagosoma vesicular que luego se fusiona con lisosomas primarios o secundarios , formando un fagolisosoma. [9] Existen varios mecanismos que conducen a la muerte intracelular; hay procesos oxidativos y otros independientes del metabolismo oxidativo. El primero implica la activación de sistemas enzimáticos de membrana que conducen a una estimulación de la captación de oxígeno (conocida como estallido respiratorio) y su reducción a intermediarios reactivos de oxígeno (ROI), especies moleculares que son altamente tóxicas para los microorganismos. [9] La enzima responsable de la provocación del estallido respiratorio se conoce como nicotinamida adenina dinucleótido fosfato (NADPH) oxidasa, que se compone de cinco subunidades. [9] Un componente es un citocromo de membrana formado por dos subunidades proteicas, gp91phox y p22phox; los tres componentes restantes son proteínas derivadas del citosólico: p40phox, p47phox y p67phox. [9] La NADPH oxidasa existe en el citosol del AM cuando está en estado de reposo; pero tras la activación, dos de sus componentes citosólicos, p47phox y p67phox, tienen sus residuos de tirosina y serina fosforilados, que luego pueden mediar la translocación de NADPHox al componente del citocromo, gp91phox/p22phox, en la membrana plasmática a través de elementos del citoesqueleto. [11]
En comparación con otros fagocitos, el estallido respiratorio en AM es de mayor magnitud. [9] Los mecanismos microbicidas independientes del oxígeno se basan en la producción de ácido, en la secreción de lisozimas, en proteínas que se unen al hierro y en la síntesis de polipéptidos catiónicos tóxicos. [9] Los macrófagos poseen un repertorio de moléculas antimicrobianas empaquetadas dentro de sus gránulos y lisosomas. [9] Estos orgánulos contienen una miríada de enzimas degradativas y péptidos antimicrobianos que se liberan en el fagolisosoma, como proteasas, nucleasas, fosfatasas, esterasas, lipasas y péptidos altamente básicos. [9] Además, los macrófagos poseen una serie de mecanismos de privación de nutrientes que se utilizan para privar a los patógenos fagocitados de micronutrientes esenciales. [9] Ciertos microorganismos han desarrollado contramedidas que les permiten evadir ser destruidos por los fagocitos. Aunque la degradación mediada por lisosomas es un medio eficiente para neutralizar una infección y prevenir la colonización, varios patógenos parasitan a los macrófagos, explotándolos como una célula huésped para el crecimiento, el mantenimiento y la replicación. [9] Los parásitos como Toxoplasma gondii y las micobacterias pueden evitar la fusión de los fagosomas con los lisosomas, escapando así a la acción dañina de las hidrolasas lisosomales. Otros evitan los lisosomas abandonando la vacuola fagocítica para llegar a la matriz citosólica donde su desarrollo no se ve obstaculizado. En estos casos, los macrófagos pueden verse inducidos a destruir activamente los microorganismos fagocitados produciendo una serie de moléculas altamente tóxicas e induciendo un mecanismo de privación para matarlos de hambre. [9] Finalmente, algunos microbios tienen enzimas para desintoxicar los metabolitos de oxígeno formados durante el estallido respiratorio. [9]
Cuando no son suficientes para protegerse de la amenaza, los macrófagos alveolares pueden liberar citocinas y quimiocinas proinflamatorias para generar una red altamente desarrollada de células fagocíticas defensivas responsables de la respuesta inmune adaptativa.
Los pulmones son especialmente sensibles y propensos a sufrir daños, por lo que para evitar daños colaterales a los neumocitos tipo I y tipo II, los macrófagos alveolares se mantienen en un estado inactivo, produciendo pocas citocinas inflamatorias y mostrando poca actividad fagocítica, como lo demuestra la expresión regulada a la baja del antígeno del receptor fagocítico Macrófago 1 (Mac-1). [7] [12] Los AM suprimen activamente la inducción de dos de los sistemas de inmunidad del cuerpo: la inmunidad adaptativa y la inmunidad humoral. La inmunidad adaptativa se suprime a través de los efectos de los AM en las células dendríticas intersticiales, las células B y las células T, ya que estas células son menos selectivas de lo que destruyen y, a menudo, causan daños innecesarios a las células normales. Para prevenir la inflamación descontrolada en el tracto respiratorio inferior, los macrófagos alveolares secretan óxido nítrico, prostaglandinas , interleucina-4 y -10 (IL-4, IL-10) y factor de crecimiento transformante -β (TGF-β). [12] [13] [14] [15]
El óxido nítrico (NO) es una fuente importante de inmunomodulación en roedores y es producido por la enzima óxido nítrico sintetasa tipo 2 (NOS2) en el macrófago alveolar. [14] El NO inhibe la fosforilación de tirosina de las quinasas involucradas en la producción del receptor de interleucina-2 (IL-2), cuya expresión es fundamental para la proliferación de células T. [13] En humanos, sin embargo, la actividad de NOS2 ha sido difícil de verificar. [14]
Existen dos explicaciones para la falta de respuesta del promotor de la óxido nítrico sintetasa inducible humana (iNOS) a la activación del NO por lipopolisacáridos (LPS) + interferón gamma (IFNγ). [14] La primera es que existen diversas variaciones de nucleótidos inactivadores en la contraparte humana del elemento potenciador que regula la expresión inducida por LPS/IFNγ del gen NOS2 de ratón. La segunda se debe a la ausencia de un factor nuclear en los macrófagos humanos que se requiere para la expresión óptima del gen NOS2 (complejo factor nuclear inducible por LPS-kappa B/Rel). [14] Se supone que la dificultad para verificar NOS2 se debe a una expresión mucho más controlada en los macrófagos humanos en comparación con la de los macrófagos de roedores. [14] La NOS2 es parte de un circuito de retroalimentación autorregulatoria, en el que un alérgeno o provocador estimula la producción de citocinas inflamatorias, que a su vez estimula la producción de NO, y el NO regula a la baja la producción de citocinas. [14] En ratas, el NO inhibe la maduración de células dendríticas mediada por el factor estimulante de colonias de granulocitos y macrófagos (GM-CSF), y en humanos inhibe la maduración de células dendríticas humanas mediada por TNF-alfa, a través de mecanismos dependientes de GMP cíclico. [14] El NO prolonga la capacidad de las células dendríticas humanas para internalizar antígenos en sitios de inflamación, modulando así los pasos iniciales que conducen a respuestas inmunes específicas de antígeno. [14]
Se ha implicado a la producción de NO como un factor relevante en la patología del asma. Las personas con asma muestran una mayor expresión de iNOS en las células epiteliales de las vías respiratorias y un mayor nivel de óxido nítrico en el aire exhalado. [14]
Se han aislado muchos otros factores inmunomoduladores, de los cuales los más importantes son las prostaglandinas y las citocinas. PGE2 fue el primer inmunomodulador derivado de los macrófagos y descrito. [14] PGE2 funciona en la amplificación de la transcripción de IL-10 de linfocitos de sangre periférica y la producción de proteínas; así como en la desactivación de macrófagos y células T. [14] PGE2 es un eicosanoide inmunomodulador derivado del componente de la membrana celular, ácido araquidónico , y se procesa en la cascada del ácido araquidónico: la oxigenación e isomerización sucesivas del ácido araquidónico por las enzimas ciclooxigenasa y PGE2 sintasa. [16] La regulación de las células diana por PGE2 ocurre a través de la señalización a través de cuatro receptores E-prostanoides (EP) acoplados a proteína G asociados a la membrana celular, llamados EP1, EP2, EP3 y EP4. [16] La PGE2 inhibe la muerte bacteriana y la producción de ROI por AM al afectar la fagocitosis mediada por Fcγ a través de su capacidad para estimular la producción de efectores intracelulares de monofosfato de adenosina cíclico (cAMP) a través de la señalización de los receptores EP2 y EP4. [11] [16] Los receptores EP2 y EP4 envían señales principalmente a través de la proteína G estimuladora (Gs), lo que aumenta la actividad de la adenilil ciclasa (AC) y la posterior formación de cAMP. [11] El cAMP es un segundo mensajero que influye en múltiples funciones celulares a través de la activación de dos moléculas efectoras posteriores, la proteína quinasa A (PKA) y las proteínas de intercambio activadas directamente por cAMP (Epac-1 y -2). [11] Epac-1 y PKA son factores importantes involucrados en la inhibición de la muerte bacteriana de AM. [11] Los efectos de PKA resultan de su capacidad para fosforilar residuos de serina y treonina en muchas proteínas celulares, especialmente la proteína de unión al elemento de respuesta al cAMP del factor de transcripción (CREB). El eje cAMP/PKA/CREB media la inhibición de la liberación de TNF-alfa. [11] La eliminación de bacterias fagocitadas por los AM depende de varios mecanismos microbicidas distintos, como la liberación reducida de ROI mediada por la NADPH oxidasa. [9] [11] La generación de ROI por la NADPH oxidasa es un mecanismo bactericida importante después de la fagocitosis mediada por FcR. [11] La PGE2 activa los receptores EP2 y EP4 acoplados a Gs por ligación, estimulando la producción de cAMP y la posterior activación de los efectores de cAMP descendentes, PKA y Epac-1; ambos a su vez perjudican la fosforilación y la translocación de la membrana fagosómica del componente de la NADPH oxidasa, p47phox, inhibiendo así el estallido respiratorio. [11]
La IL-4 es una citocina pleiotrópica que desempeña un papel clave en el desarrollo de las células T auxiliares de tipo 2 (Th2). La IL-4 es importante para la diferenciación de las células T CD4-naïve en células maduras de tipo Th2; así como para el cambio de clase de inmunoglobulina (Ig) a IgE e IgG4 durante el desarrollo de las respuestas inmunitarias. [17] [18] La Ig es una clase de anticuerpo que se encuentra solo en mamíferos y que desempeña un papel importante en la respuesta alérgica y la defensa contra muchos tipos de patógenos al proteger al cuerpo contra ellos mediante la activación del complemento, la opsonización para la fagocitosis y la neutralización de sus toxinas. [18]
Se ha demostrado que tanto la IL-4 como la IL-10 reducen la producción de metaloproteinasas (endopeptidasas que descomponen el colágeno y otras proteínas extracelulares) por los macrófagos humanos. [14] [15] La IL-4 tiene efectos duales sobre la función biológica de los macrófagos, que pueden ser estimulantes o inhibidores. [15] Mejora la expresión del antígeno MHC de clase II (complejo proteico extracelular que interactúa exclusivamente con las células CD4-T como parte de la vía exógena) y Mac-1 (receptor de superficie como parte del sistema innato del complemento), promoviendo así la fagocitosis. [15] También se ha demostrado que la IL-4 inhibe la producción de PGE2 al reducir la expresión de la enzima, prostaglandina H sintasa -2 (PGHS-2), que es fundamental en la producción de PGE2. [14] Sin embargo, la IL-4 inhibe la producción de TNF-alfa, IL-1 y -6, que son todas citocinas importantes en la respuesta proinflamatoria). [15]
La IL-10 inhibe la secreción de las citocinas proinflamatorias TNF-alfa e INF-gamma, suprimiendo así la proliferación de células T, células NK y AM. [14] La IL-10 comparte mecanismos inmunomoduladores similares a los del TGF-β. [14] Se cree que ambas citocinas reducen la tasa de apoptosis en los macrófagos alveolares humanos, mejorando así indirectamente la inhibición de la proliferación de células T mediada por los macrófagos alveolares. [14] Hay un aumento significativo en la tasa basal de apoptosis tras la activación por productos bacterianos. La apoptosis está particularmente regulada por la presencia de citocinas: el IFNγ aumenta la tasa de apoptosis, mientras que la IL-10 y el TGF-β la disminuyen. [14] Sin embargo, la IL-10 tiene efectos contraproducentes en el sistema inmunológico y se ha demostrado que en realidad promueve la infección por patógenos extraños. Se ha descubierto que la IL-10 desempeña un papel en las infecciones bacterianas y parasitarias como estrategia para evadir el sistema inmunológico del huésped. [19] Hay bacterias que parasitan a los macrófagos alveolares invadiendo sus membranas y prosperan creciendo y replicándose dentro de ellas, explotando a los macrófagos como células huésped. Normalmente, esta infección puede ser eliminada por las células T, que activan enzimas en los macrófagos alveolares que destruyen las bacterias; pero se ha demostrado que estas bacterias alteran la red de señalización de citocinas en su beneficio. Como citocina inhibidora, la IL-10 facilita la infección de los macrófagos alveolares y monocitos humanos al revertir por completo el efecto protector del IFNγ contra la replicación intracelular de Legionella pneumophila. [19] También se ha demostrado que Yersinia enterocolitica libera el antígeno de virulencia LcrV, que induce IL-10 a través del receptor tipo Toll-2 y CD14 (una proteína de superficie accesoria de la señalización de LPS mediada por TLR4), lo que da como resultado la supresión de IFNγ y TNF-alfa. [19]
En condiciones normales, los macrófagos alveolares se adhieren estrechamente a las células epiteliales alveolares, induciendo así la expresión de la integrina αvβ6. Las integrinas son receptores diméricos de la superficie celular compuestos por subunidades alfa y beta, que activan el TGF-β. [20] [21] El TGF-β es una citocina multifuncional que modula una variedad de procesos biológicos como el crecimiento celular, la apoptosis, la síntesis de la matriz extracelular, la inflamación y las respuestas inmunitarias. [22] El TGF-β regula estrechamente la actividad antiinflamatoria al suprimir la producción de citocinas proinflamatorias, inhibiendo así la función de los linfocitos T. [23] Las integrinas avβ6 y avβ8 secuestran el TGF-β latente en la superficie celular, donde la activación puede acoplarse estrechamente a las respuestas celulares al estrés ambiental en el mantenimiento de la homeostasis; las integrinas también localizan el TGFβ activado en las proximidades de los macrófagos. [24] Normalmente, el TGFβ maduro se secreta como un complejo latente con su fragmento N-terminal, el péptido asociado a la latencia (LAP), que inhibe su actividad. [22] El complejo latente está unido covalentemente a la matriz extracelular mediante la unión a las proteínas latentes de unión al TGF-β. [20] El TGF-β se activa por diversos mecanismos en el pulmón, que en última instancia implican la proteólisis o la alteración conformacional del LAP. [24] La integrina αvβ6 puede mediar la activación del TGF-β mediante la unión al LAP del TGF-β1, que sirve como sitio de unión del ligando para la integrina y es un componente esencial del aparato de activación del TGF-β. [22] [25] Una vez activado, el TGFβ conduce a la supresión de la funcionalidad de los macrófagos (producción de citocinas y fagocitosis). [22] La unión del TGF-β activado a sus receptores expresados en los macrófagos alveolares induce una cascada de señalización descendente, que incluye la fosforilación de los homólogos 2 y 3 de Small Mothers Against Decapentaplegic (R-SMAD) regulados por el receptor. [7] [22] [23] Los SMAD-2 y -3 fosforilados forman entonces complejos heteroméricos con el mediador común SMAD 4 (co-SMAD-4). Una vez ensamblados, los complejos se translocan al núcleo a través del poro nuclear con la ayuda de las importinas alfa/beta. Una vez en el núcleo, estos complejos se acumulan y finalmente actúan como factores de transcripción, regulando la expresión de los genes diana del TGF-β. [23] Por lo tanto, la señalización del TGF-β implica una vía directa desde los receptores en la superficie de una célula hasta el núcleo.
Los receptores tipo Toll (TLR) son PRR de señalización , capaces de reconocer varias proteínas bacterianas. [10] Aunque las bacterias han desarrollado medios para evadir los mecanismos de defensa del huésped, expresan PAMP, como lipoglicanos y lipoproteínas que son reconocidos por las células del sistema inmune innato a través de los TLR. [10] Tras la unión de los PAMP a los TLR, el TLR desencadena respuestas inflamatorias y defensivas en la célula huésped, induciendo la polimerización de actina en los macrófagos alveolares (un componente crucial en la endocitosis y la motilidad). [22] La polimerización de actina en los macrófagos alveolares provoca la supresión de la expresión de integrina, que a su vez provoca la desactivación de TGF-β y la regulación negativa del nivel de fosforilación basal de SMAD 2/3; lo que posteriormente conduce a la activación y el desprendimiento de los macrófagos alveolares de las células epiteliales alveolares [22] [15]. Tras la activación, los macrófagos se preparan para la fagocitosis y comienzan a secretar citocinas proinflamatorias (TNF-α e IL-6). [22]
La preparación de los macrófagos implica la mejora de la actividad de la ráfaga respiratoria por parte del IFN-γ y el TNF-α. [9] El IFNγ induce tanto una mayor afinidad de la NADPH oxidasa por el NADPH en los macrófagos, como una mayor tasa de transcripción génica y expresión de mensajes para la proteína gp91phox. [9] El TNF-α actúa como un estímulo autocrino al aumentar la expresión de las transcripciones de p47phox y p67phox. Las ROI producidas durante la respuesta de la ráfaga respiratoria, a su vez, mejoran la producción de TNF-α por los macrófagos. [9]
El intercambio de gases debe restablecerse lo más rápido posible para evitar daños colaterales, por lo que los linfocitos activados secretan IFNγ para estimular la producción de metaloproteinasa de matriz MMP-9 por los macrófagos. [22] Se ha informado que los AM producen MMP-9 en parte a través de las vías de señalización de PKA dependientes de PGE2, que son las vías involucradas en la inhibición de la fagocitosis. [26] La MMP-9 activa el TGF-β latente, reinduciendo la expresión de las integrinas αvβ6 en las células epiteliales alveolares, devolviendo así el macrófago alveolar a un estado de reposo. [7] [22] [26] La activación del TGF-β también es ventajosa porque su producción estimula la síntesis de colágeno en los fibroblastos intersticiales, que es necesaria para restaurar la arquitectura de la pared alveolar. [22]
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )