Los antibióticos β-lactámicos ( antibióticos beta -lactámicos ) son antibióticos que contienen un anillo β-lactámico en su estructura química. Esto incluye derivados de penicilina ( penams ), cefalosporinas y cefamicinas ( cefems ), monobactámicos , carbapenémicos [1] y carbacefems . [2] La mayoría de los antibióticos β-lactámicos funcionan inhibiendo la biosíntesis de la pared celular en el organismo bacteriano y son el grupo de antibióticos más utilizado. Hasta 2003, cuando se midió por ventas, más de la mitad de todos los antibióticos disponibles comercialmente en uso eran compuestos β-lactámicos. [3] El primer antibiótico β-lactámico descubierto, la penicilina , fue aislado de una cepa de Penicillium rubens (nombrada como Penicillium notatum en ese momento). [4] [5]
Las bacterias suelen desarrollar resistencia a los antibióticos β-lactámicos mediante la síntesis de una β-lactamasa , una enzima que ataca el anillo β-lactámico. Para superar esta resistencia, los antibióticos β-lactámicos pueden administrarse con inhibidores de la β-lactamasa , como el ácido clavulánico . [6]
Los antibióticos β-lactámicos están indicados para la prevención y el tratamiento de infecciones bacterianas causadas por organismos susceptibles. Al principio, los antibióticos β-lactámicos eran principalmente activos sólo contra bacterias grampositivas , pero el desarrollo reciente de antibióticos β-lactámicos de amplio espectro activos contra varios organismos gramnegativos ha aumentado su utilidad. [ cita requerida ]
En las meninges cerebrales no inflamadas (normales), la penetración de los antibióticos betalactámicos es baja, con una relación AUC LCR /AUC S de 0,15 (la relación del área bajo la curva del líquido cefalorraquídeo frente al área bajo la curva del suero). [7]
Las reacciones adversas más comunes a los antibióticos β-lactámicos incluyen diarrea, náuseas, sarpullido, urticaria y superinfección (incluida candidiasis ). [8]
Los efectos adversos poco frecuentes incluyen fiebre, vómitos, eritema , dermatitis, angioedema y colitis pseudomembranosa . [8]
El dolor y la inflamación en el lugar de la inyección también son comunes en el caso de los antibióticos β-lactámicos administrados por vía parenteral . [ cita requerida ]
Las reacciones adversas inmunológicamente mediadas a cualquier antibiótico β-lactámico pueden ocurrir en hasta el 10% de los pacientes que reciben ese agente (una pequeña fracción de las cuales son verdaderamente reacciones alérgicas mediadas por IgE , ver erupción por amoxicilina ). La anafilaxia ocurrirá en aproximadamente el 0,01% de los pacientes. [8] [9] Quizás haya una sensibilidad cruzada del 5 al 10% entre los derivados de la penicilina, las cefalosporinas y los carbapenémicos; [ cita requerida ] pero esta cifra ha sido cuestionada por varios investigadores. [ ¿quién? ] [ cita requerida ]
Sin embargo, el riesgo de reactividad cruzada es suficiente para justificar la contraindicación de todos los antibióticos β-lactámicos en pacientes con antecedentes de reacciones alérgicas graves ( urticaria , anafilaxia, nefritis intersticial ) a cualquier antibiótico β-lactámico. En raras ocasiones, las reacciones alérgicas se han desencadenado por la exposición a través de besos y contacto sexual con una pareja que esté tomando estos antibióticos. [10]
Puede producirse una reacción de Jarisch-Herxheimer después del tratamiento inicial de una infección por espiroquetas , como la sífilis, con un antibiótico β-lactámico. [ cita requerida ]

Los antibióticos β-lactámicos son bactericidas y actúan inhibiendo la síntesis de la capa de peptidoglicano de las paredes celulares bacterianas . La capa de peptidoglicano es importante para la integridad estructural de la pared celular, [6] especialmente en organismos grampositivos , siendo el componente más externo y primario de la pared. El paso final de transpeptidación en la síntesis del peptidoglicano es facilitado por las DD -transpeptidasas , también conocidas como proteínas de unión a penicilina (PBP). Las PBP varían en su afinidad por la penicilina y otros antibióticos β-lactámicos. El número de PBP varía entre las especies bacterianas. [11]
Los antibióticos β-lactámicos son análogos de la d -alanil- d - alanina , los residuos de aminoácidos terminales de las subunidades precursoras del péptido NAM/NAG de la capa naciente de peptidoglicano. La similitud estructural entre los antibióticos β-lactámicos y la d -alanil- d -alanina facilita su unión al sitio activo de las PBP. El núcleo β-lactámico de la molécula se une irreversiblemente al residuo Ser 403 del sitio activo de las PBP ( acila ). Esta inhibición irreversible de las PBP impide la reticulación final (transpeptidación) de la capa naciente de peptidoglicano, lo que altera la síntesis de la pared celular. [13] Los antibióticos β-lactámicos bloquean no sólo la división de bacterias, incluidas las cianobacterias , sino también la división de las cianelas, los orgánulos fotosintéticos de las glaucófitas , y la división de los cloroplastos de las briofitas . Por el contrario, no tienen efecto sobre los plástidos de las plantas vasculares altamente desarrolladas . Esto apoya la teoría endosimbiótica e indica una evolución de la división de plástidos en plantas terrestres. [14]
En circunstancias normales, los precursores de peptidoglicanos indican una reorganización de la pared celular bacteriana y, como consecuencia, desencadenan la activación de las hidrolasas autolíticas de la pared celular . La inhibición de la reticulación por las β-lactámicas provoca una acumulación de precursores de peptidoglicanos, lo que desencadena la digestión del peptidoglicano existente por las hidrolasas autolíticas sin la producción de nuevo peptidoglicano. Como resultado, la acción bactericida de los antibióticos β-lactámicos se potencia aún más. [ cita requerida ]
Otra posibilidad que se ha propuesto para explicar gran parte de la citotoxicidad de las β-lactáminas se centra en la oxidación del nucleótido de guanina en el conjunto de nucleótidos bacterianos. [15] La incorporación del nucleótido de guanina oxidado al ADN podría causar citotoxicidad. La citotoxicidad bacteriana podría surgir de la reparación incompleta de lesiones de 8-oxo-2'-desoxiguanosina muy espaciadas en el ADN, lo que da lugar a roturas de doble cadena. [15]
Dos características estructurales de los antibióticos β-lactámicos se han correlacionado con su potencia antibiótica. [16] La primera se conoce como "parámetro de Woodward", h , y es la altura (en angstroms ) de la pirámide formada por el átomo de nitrógeno de la β-lactama como vértice y los tres átomos de carbono adyacentes como base. [17] El segundo se llama "parámetro de Cohen", c , y es la distancia entre el átomo de carbono del carboxilato y el átomo de oxígeno del carbonilo de la β-lactama . [18] Se cree que esta distancia corresponde a la distancia entre el sitio de unión del carboxilato y el agujero de oxianión de la enzima PBP. Los mejores antibióticos son aquellos con valores h más altos (más reactivos a la hidrólisis) y valores c más bajos (mejor unión a las PBP). [16]
Por definición, todos los antibióticos β-lactámicos tienen un anillo β-lactámico en su estructura. La eficacia de estos antibióticos depende de su capacidad para alcanzar la PBP intacta y de su capacidad para unirse a ella. Por lo tanto, existen dos modos principales de resistencia bacteriana a los β-lactámicos: la hidrólisis enzimática del anillo β-lactámico y la posesión de proteínas de unión a la penicilina alteradas. [ cita requerida ]
Si la bacteria produce la enzima β-lactamasa o la enzima penicilinasa , la enzima hidrolizará el anillo β-lactámico del antibiótico, volviéndolo ineficaz. [19] (Un ejemplo de dicha enzima es la metalo-beta-lactamasa 1 de Nueva Delhi , descubierta en 2009). Los genes que codifican estas enzimas pueden estar presentes de manera inherente en el cromosoma bacteriano o pueden adquirirse mediante transferencia de plásmidos ( resistencia mediada por plásmidos ), y la expresión del gen β-lactamasa puede ser inducida por la exposición a β-lactáminas. [ cita requerida ]


La producción de una β-lactamasa por una bacteria no descarta necesariamente todas las opciones de tratamiento con antibióticos β-lactámicos. En algunos casos, los antibióticos β-lactámicos pueden administrarse conjuntamente con un inhibidor de la β-lactamasa . Por ejemplo, Augmentin (FGP) está hecho de amoxicilina (un antibiótico β-lactámico) y ácido clavulánico (un inhibidor de la β-lactamasa). El ácido clavulánico está diseñado para abrumar a todas las enzimas β-lactamasa y servir eficazmente como antagonista para que la amoxicilina no se vea afectada por las enzimas β-lactamasa. Otra combinación de β-lactámico/inhibidor de la β-lactamasa es piperacilina/tazobactam con un amplio espectro de actividad antibacteriana que incluye bacterias aeróbicas y anaeróbicas grampositivas y gramnegativas. La adición de tazobactam a la piperacilina ha mejorado su estabilidad frente a una amplia gama de enzimas β-lactamasas, incluidas algunas β-lactamasas de espectro extendido. [20]
Se están estudiando otros inhibidores de las β-lactamasas, como los ácidos borónicos, que se unen de forma irreversible al sitio activo de las β-lactamasas. Esto supone una ventaja con respecto al ácido clavulánico y a otros β-lactámas competidores similares, ya que no se pueden hidrolizar y, por lo tanto, se vuelven inútiles. Actualmente se están realizando investigaciones exhaustivas para desarrollar ácidos borónicos personalizados que actúen sobre diferentes isoenzimas de las β-lactamasas. [21]
Sin embargo, en todos los casos en los que se sospecha una infección por bacterias productoras de β-lactamasa, se debe considerar cuidadosamente la elección de un antibiótico β-lactámico adecuado antes del tratamiento. En particular, la elección de la terapia antibiótica β-lactámica adecuada es de suma importancia contra los organismos que albergan algún nivel de expresión de β-lactamasa. En este caso, no utilizar la terapia antibiótica β-lactámica más adecuada al inicio del tratamiento podría dar como resultado la selección de bacterias con niveles más altos de expresión de β-lactamasa, lo que dificultaría los esfuerzos posteriores con otros antibióticos β-lactámicos. [22]
En el contexto de la farmacología médica, las penicilinas, las cefalosporinas y los carbapenémicos, si bien todos tienen el anillo β-lactámico que sirve como estructura fundamental, también tienen un anillo auxiliar que lleva un grupo carboxilato que está ubicado en el mismo lado que el grupo carbonilo dentro del anillo β-lactámico y, como tal, esta configuración estructural es fundamental para su actividad antimicrobiana. [23] La resistencia bacteriana a estos antibióticos ocurre principalmente a través de la producción de β-lactamasas, enzimas que hidrolizan el enlace amida del anillo β-lactámico, eliminando así la actividad antimicrobiana de estos antibióticos. Este mecanismo de resistencia subraya la importancia de la integridad estructural del anillo β-lactámico para la función del antibiótico. [24] El cambio de color de incoloro o amarillo claro a ámbar o incluso rojo en una solución acuosa de un antibiótico β-lactámico puede denotar la hidrólisis de los enlaces amida en el anillo β-lactámico por parte de la β-lactamasa. [25] [26] Esto se observa a menudo con un sustrato cromogénico de β-lactamasa como ceftriaxona, merapenem o nitrocefina, [27] que sufre un cambio de color distintivo de amarillo a rojo a medida que la β-lactamasa hidroliza el enlace amida en el anillo β-lactámico. [27] [28] Este cambio de color es un indicador visual de la presencia y actividad de las enzimas β-lactamasas, que son responsables de conferir resistencia a los antibióticos β-lactámicos en muchas especies bacterianas. La hidrólisis del anillo β-lactámico por las enzimas β-lactamasa hace que el antibiótico sea ineficaz, lo que permite que las bacterias sobrevivan en presencia del antibiótico. [28] Se sabe que algunos antibióticos β-lactámicos como la ceftriaxona y el meropenem son relativamente inestables en solución, especialmente cuando se almacenan durante períodos prolongados, y se degradan en una solución acuosa incluso sin la presencia de β-lactamasa. [29] En el caso de la ceftriaxona, el color de las soluciones puede variar de amarillo claro a ámbar, dependiendo del tiempo de almacenamiento, la concentración y el diluyente utilizado. [30] [31] Un estudio encontró que las concentraciones de meropenem cayeron al 90% de la concentración inicial a las 7,4 horas a 22 °C y a las 5,7 horas a 33 °C, lo que indica una degradación con el tiempo. [29]
Como respuesta al uso de β-lactáminas para controlar las infecciones bacterianas, algunas bacterias han desarrollado proteínas de unión a penicilina con estructuras novedosas. Los antibióticos β-lactáminas no pueden unirse de manera tan efectiva a estas PBP alteradas y, como resultado, las β-lactáminas son menos efectivas para alterar la síntesis de la pared celular. Ejemplos notables de este modo de resistencia incluyen Staphylococcus aureus resistente a la meticilina ( MRSA ) [32] y Streptococcus pneumoniae resistente a la penicilina . Las PBP alteradas no descartan necesariamente todas las opciones de tratamiento con antibióticos β-lactáminas. [ cita médica necesaria ]

Las β-lactamas se clasifican según sus estructuras de anillo central. [33]
Por convención, las β-lactámas bicíclicas se numeran comenzando con la posición que ocupa el azufre en las penamas y cefemas, independientemente de qué átomo se encuentre en una clase dada. Es decir, la posición 1 siempre está adyacente al carbono β del anillo de la β-lactáma. La numeración continúa en el sentido de las agujas del reloj desde la posición uno hasta que se alcanza el carbono β de la β-lactáma, momento en el que la numeración continúa en sentido contrario a las agujas del reloj alrededor del anillo de la lactama para numerar los carbonos restantes. Por ejemplo, el átomo de nitrógeno de todas las β-lactámas bicíclicas fusionadas a anillos de cinco miembros se etiqueta como la posición 4, como en las penamas, mientras que en las cefemas, el nitrógeno es la posición 5. [ cita médica necesaria ]
La numeración de las monobactamas sigue la de la IUPAC : el átomo de nitrógeno está en la posición 1, el carbono carbonílico en la 2, el carbono α en la 3 y el carbono β en la 4. [ cita médica necesaria ]
Hasta la fecha, se han descubierto dos métodos distintos de biosíntesis del núcleo β-lactámico de esta familia de antibióticos. La primera vía descubierta fue la de los penams y los cefems. Esta vía comienza con una sintetasa de péptidos no ribosómicos (NRPS), la sintetasa ACV (ACVS), que genera el tripéptido lineal δ-( L -α-aminoadipyl) -L -cisteína- D -valina (ACV). La isopenicilina N sintasa (IPNS) cicla oxidativamente el ACV (dos ciclaciones por una sola enzima) al intermediario bicíclico isopenicilina N para formar la estructura del núcleo del penam. [34] Varias transamidaciones conducen a las diferentes penicilinas naturales.
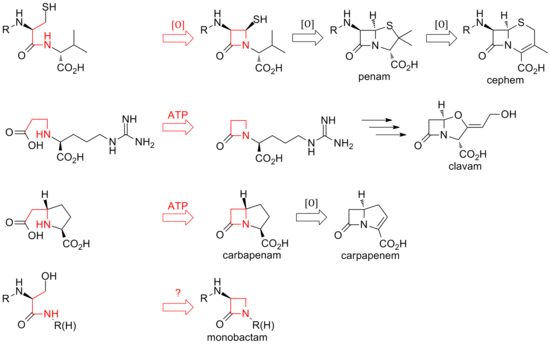
La biosíntesis de los cefemas se ramifica en la isopenicilina N mediante una expansión del anillo oxidativo hasta el núcleo del cefema. Al igual que con los penams, la variedad de cefalosporinas y cefamicinas proviene de diferentes transamidaciones, como es el caso de las penicilinas. [ cita requerida ]
Mientras que el cierre del anillo en los penams y cefems está entre las posiciones 1 y 4 de la β-lactama y es oxidativo, los clavams y carbapenems tienen sus anillos cerrados entre las posiciones 1 y 2 del anillo. Las β-lactama sintetasas son responsables de estas ciclizaciones, y el carboxilato de los sustratos de anillo abierto es activado por ATP . [35] En los clavams, la β-lactama se forma antes del segundo anillo; en los carbapenems, el anillo de β-lactama se cierra en segundo lugar en secuencia. [ cita requerida ]
La biosíntesis del anillo β-lactámico de la tabtoxina refleja la de los clavams y los carbapenémicos. El cierre del anillo lactámico en los otros monobactámicos, como la sulfazecina y las nocardicinas, puede implicar un tercer mecanismo que implica la inversión de la configuración en el carbono β. [36]
{{cite web}}: CS1 maint: copia archivada como título ( enlace ){{cite web}}: CS1 maint: copia archivada como título ( enlace )