
La técnica de patch clamp es una técnica de laboratorio en electrofisiología que se utiliza para estudiar corrientes iónicas en células vivas aisladas individuales , secciones de tejido o parches de membrana celular. La técnica es especialmente útil en el estudio de células excitables como neuronas , cardiomiocitos , fibras musculares y células beta pancreáticas , y también puede aplicarse al estudio de canales iónicos bacterianos en esferoplastos gigantes especialmente preparados .
La fijación del parche se puede realizar utilizando la técnica de fijación de voltaje . En este caso, el experimentador controla el voltaje a través de la membrana celular y se registran las corrientes resultantes. Alternativamente, se puede utilizar la técnica de pinza actual . En este caso, el experimentador controla la corriente que pasa a través de la membrana y los cambios de voltaje resultantes se registran, generalmente en forma de potenciales de acción .
Erwin Neher y Bert Sakmann desarrollaron la abrazadera de parche a finales de los años 1970 y principios de los 1980. Este descubrimiento hizo posible registrar por primera vez las corrientes de moléculas de canales iónicos individuales, lo que mejoró la comprensión de la participación de los canales en procesos celulares fundamentales, como los potenciales de acción y la actividad nerviosa. Neher y Sakmann recibieron el Premio Nobel de Fisiología o Medicina en 1991 por este trabajo. [1]
Durante una grabación con pinza de parche, un tubo de vidrio hueco conocido como micropipeta o pipeta de parche lleno de una solución electrolítica y un electrodo de grabación conectado a un amplificador se pone en contacto con la membrana de una celda aislada . Se coloca otro electrodo en un baño que rodea la célula o tejido como electrodo de tierra de referencia . Se puede formar un circuito eléctrico entre el electrodo de registro y el de referencia con la celda de interés en el medio.


La solución que llena la pipeta del parche puede coincidir con la composición iónica de la solución del baño, como en el caso del registro adherido a células, o coincidir con el citoplasma , para el registro de células completas. La solución del baño puede coincidir con la solución extracelular fisiológica, el citoplasma, o ser completamente no fisiológica, según el experimento a realizar. El investigador también puede cambiar el contenido de la solución del baño (o menos comúnmente la solución de la pipeta) agregando iones o medicamentos para estudiar los canales iónicos en diferentes condiciones.
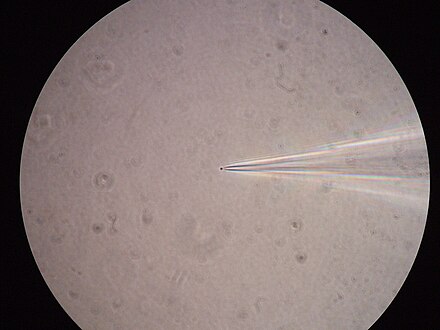
Dependiendo de lo que el investigador esté tratando de medir, el diámetro de la punta de la pipeta utilizada puede variar, pero generalmente está en el rango micrométrico . [2] Este tamaño pequeño se utiliza para encerrar un área de superficie de membrana celular o "parche" que a menudo contiene sólo una o unas pocas moléculas de canal iónico. [3] Este tipo de electrodo se diferencia del "microelectrodo afilado" utilizado para perforar células en grabaciones intracelulares tradicionales , en que se sella en la superficie de la membrana celular, en lugar de insertarse a través de ella.

En algunos experimentos, la punta de la micropipeta se calienta en una microforja para producir una superficie lisa que ayuda a formar un sello de alta resistencia con la membrana celular. Para obtener este sellado de alta resistencia, se presiona la micropipeta contra una membrana celular y se aplica succión. Una porción de la membrana celular se succiona hacia la pipeta, creando un área de membrana en forma de omega que, si se forma correctamente, crea una resistencia en el rango de 10 a 100 gigaohmios , llamada "sello de gigaohmios" o "gigaseal". [3] La alta resistencia de este sello permite aislar electrónicamente las corrientes medidas a través del parche de membrana con poco ruido competitivo , además de proporcionar cierta estabilidad mecánica a la grabación. [4]

Muchos amplificadores de pinza de conexión no utilizan circuitos de pinza de voltaje real , sino que son amplificadores diferenciales que utilizan el electrodo de baño para establecer el nivel de corriente cero (tierra). Esto permite al investigador mantener el voltaje constante mientras observa cambios en la corriente . Para realizar estos registros, se compara la pipeta de parche con el electrodo de tierra. Luego se inyecta corriente en el sistema para mantener un voltaje establecido constante. La corriente que se necesita para fijar el voltaje tiene signo opuesto e igual en magnitud a la corriente a través de la membrana. [3]
Alternativamente, la celda se puede sujetar con corriente en modo de celda completa, manteniendo la corriente constante mientras se observan cambios en el voltaje de la membrana . [5]
La sección precisa del tejido con vibratomo o micrótomo comprestomo es esencial, además de los métodos de pinzamiento con parche. Al suministrar cortes de tejido finos y uniformes, estos dispositivos proporcionan una implantación óptima de los electrodos. Para preparar tejidos para estudios de pinzamiento de parche de una manera que garantice registros precisos y confiables, los investigadores pueden seleccionar entre el uso de vibratomos para tejidos más blandos y micrótomos para estructuras más resistentes. [6] Leica Biosystems y Carl Zeiss AG son los productores destacados de estos dispositivos.

Se pueden aplicar varias variaciones de la técnica básica, dependiendo de lo que el investigador quiera estudiar. Las técnicas de adentro hacia afuera y de afuera hacia afuera se denominan técnicas de "parche extirpado", porque el parche se extirpa (elimina) del cuerpo principal de la célula. Se utilizan técnicas de parche adherido a células y de parche extirpado para estudiar el comportamiento de canales iónicos individuales en la sección de membrana unida al electrodo.
El parche de célula completa y el parche perforado permiten al investigador estudiar el comportamiento eléctrico de toda la célula, en lugar de las corrientes de un solo canal. El parche de célula completa, que permite el acceso eléctrico de baja resistencia al interior de una célula, ha reemplazado en gran medida a las técnicas de registro de microelectrodos de alta resistencia para registrar corrientes a través de toda la membrana celular.

Para este método, la pipeta se sella sobre la membrana celular para obtener un gigaseal (un sello con resistencia eléctrica del orden de un gigaohmio), asegurando al mismo tiempo que la membrana celular permanezca intacta. Esto permite el registro de corrientes a través de uno o varios canales iónicos contenidos en el parche de membrana capturado por la pipeta. Al unirse únicamente al exterior de la membrana celular, hay muy poca alteración de la estructura celular. [3] Además, al no alterar el interior de la célula, cualquier mecanismo intracelular que normalmente influya en el canal podrá funcionar como lo haría fisiológicamente. [7] Con este método también es relativamente fácil obtener la configuración correcta y, una vez obtenida, es bastante estable. [8]
Para los canales iónicos activados por ligando o los canales que están modulados por receptores metabotrópicos , el neurotransmisor o fármaco en estudio suele incluirse en la solución de la pipeta, donde puede interactuar con lo que solía ser la superficie externa de la membrana. La actividad resultante del canal se puede atribuir al fármaco que se está utilizando, aunque normalmente no es posible cambiar la concentración del fármaco dentro de la pipeta. Por tanto, la técnica se limita a un punto de una curva dosis-respuesta por parche. Por lo tanto, la respuesta a la dosis se logra utilizando varias células y parches. Sin embargo, los canales iónicos dependientes de voltaje se pueden fijar sucesivamente a diferentes potenciales de membrana en un solo parche. Esto da como resultado la activación del canal en función del voltaje, y se puede establecer una curva IV (corriente-voltaje) completa en un solo parche. Otro posible inconveniente de esta técnica es que, así como las vías intracelulares de la célula no se alteran, tampoco se pueden modificar directamente. [8]

En el método de adentro hacia afuera, se une un parche de la membrana a la pipeta del parche, se separa del resto de la célula, y la superficie citosólica de la membrana se expone a los medios externos o al baño. [9] Una ventaja de este método es que el experimentador tiene acceso a la superficie intracelular de la membrana a través del baño y puede cambiar la composición química a la que está expuesta la superficie interior de la membrana. Esto es útil cuando un experimentador desea manipular el entorno en la superficie intracelular de canales iónicos individuales. Por ejemplo, los canales que se activan mediante ligandos intracelulares se pueden estudiar a través de una variedad de concentraciones de ligando.
Para lograr la configuración de adentro hacia afuera, la pipeta se une a la membrana celular como en el modo de unión a células, formando un gigasello, y luego se retrae para separar un parche de membrana del resto de la célula. Al retirar un parche de membrana, a menudo se forma inicialmente una vesícula de membrana en la punta de la pipeta, porque los extremos del parche de membrana se fusionan rápidamente después de la escisión. Luego se debe romper la cara exterior de la vesícula para entrar en modo de adentro hacia afuera; Esto se puede hacer llevando brevemente la membrana a través de la interfaz solución de baño/aire, exponiéndola a una solución baja en Ca 2+ o haciendo contacto momentáneamente con una gota de parafina o un trozo de polímero de silicona curado . [10]

Los registros de células completas implican registrar corrientes a través de múltiples canales simultáneamente, en una gran región de la membrana celular. El electrodo se deja en su lugar sobre la célula, como en los registros adheridos a la célula, pero se aplica más succión para romper el parche de membrana, proporcionando así acceso desde el interior de la pipeta al espacio intracelular de la célula. Esto proporciona un medio para administrar y estudiar cómo los tratamientos (por ejemplo, medicamentos) pueden afectar a las células en tiempo real. [11] Una vez que la pipeta está unida a la membrana celular, existen dos métodos para romper el parche. La primera es aplicando más succión. La cantidad y duración de esta succión depende del tipo de celda y del tamaño de la pipeta. El otro método requiere enviar un gran impulso de corriente a través de la pipeta. La cantidad de corriente que se aplica y la duración del pulso también dependen del tipo de celda. [8] Para algunos tipos de células, es conveniente aplicar ambos métodos simultáneamente para romper el parche.
La ventaja de la grabación con pinza de parche de celda completa sobre la grabación con la técnica de electrodo afilado es que la abertura más grande en la punta del electrodo de pinza de parche proporciona una menor resistencia y, por lo tanto, un mejor acceso eléctrico al interior de la celda. [12] [11] Una desventaja de esta técnica es que debido a que el volumen del electrodo es mayor que el volumen de la celda, el contenido soluble del interior de la celda será reemplazado lentamente por el contenido del electrodo. Esto se conoce como electrodo que "dializa" el contenido de la celda. [8] Después de un tiempo, cualquier propiedad de la célula que dependa del contenido intracelular soluble se verá alterada. La solución de pipeta utilizada generalmente se aproxima al ambiente rico en potasio del interior de la célula para minimizar cualquier cambio que esto pueda causar. A menudo hay un período al comienzo de un registro de células completas en el que se pueden tomar mediciones antes de que la célula haya sido dializada. [8]

El nombre "de afuera hacia afuera" enfatiza tanto la complementariedad de esta técnica con la técnica de adentro hacia afuera como el hecho de que coloca la superficie externa, en lugar de la intracelular, de la membrana celular en el exterior del parche de membrana, en relación con el electrodo del parche. . [7]
La formación de un parche de afuera hacia afuera comienza con una configuración de grabación de celda completa. Una vez formada la configuración de celda completa, el electrodo se retira lentamente de la celda, permitiendo que un bulbo de membrana salga de la celda. Cuando el electrodo se aleja lo suficiente, esta ampolla se desprenderá de la celda y se reformará como una membrana convexa en el extremo del electrodo (como una bola abierta en la punta del electrodo), con el exterior original de la membrana mirando hacia afuera desde el electrodo. [7] Como muestra la imagen de la derecha, esto significa que el líquido dentro de la pipeta simulará el líquido intracelular, mientras que un investigador es libre de mover la pipeta y la ampolla con sus canales a otro baño de solución. Si bien pueden existir múltiples canales en una ampolla de membrana, también son posibles grabaciones de un solo canal en esta conformación si la ampolla de membrana desprendida es pequeña y solo contiene un canal. [13]
Los parches de afuera hacia afuera brindan al experimentador la oportunidad de examinar las propiedades de un canal iónico cuando se aísla de la célula y se expone sucesivamente a diferentes soluciones en la superficie extracelular de la membrana. El experimentador puede perfundir el mismo parche con una variedad de soluciones en un período de tiempo relativamente corto, y si el canal es activado por un neurotransmisor o fármaco de la cara extracelular, entonces se puede obtener una curva dosis-respuesta . [14] Esta capacidad de medir la corriente a través de exactamente el mismo trozo de membrana en diferentes soluciones es la clara ventaja del parche de afuera hacia afuera en relación con el método de fijación de células. Por otro lado, es más difícil de lograr. El proceso de formación más largo implica más pasos que podrían fallar y da como resultado una menor frecuencia de parches utilizables.

Esta variación del método de abrazadera de parche es muy similar a la configuración de celda completa. La principal diferencia radica en el hecho de que cuando el experimentador forma el sello de gigaohmios, no se utiliza succión para romper la membrana del parche. En cambio, la solución del electrodo contiene pequeñas cantidades de un agente antifúngico o antibiótico , como anfotericina B , nistatina o gramicidina , que se difunde en el parche de membrana y forma pequeños poros en la membrana, proporcionando acceso eléctrico al interior de la célula. [15] Al comparar los métodos de células enteras y de parche perforado, se puede pensar en el parche de células enteras como una puerta abierta, en la que hay un intercambio completo entre las moléculas de la solución de la pipeta y el citoplasma. El parche perforado se puede comparar con una puerta mosquitera que sólo permite el intercambio de determinadas moléculas de la solución de la pipeta al citoplasma de la célula.
Las ventajas del método del parche perforado, en relación con los registros de células enteras, incluyen las propiedades de los poros de los antibióticos, que permiten el equilibrio sólo de pequeños iones monovalentes entre la pipeta del parche y el citosol, pero no de moléculas más grandes que no pueden atravesar los poros. Esta propiedad mantiene niveles endógenos de iones divalentes como Ca 2+ y moléculas de señalización como AMPc . En consecuencia, se pueden tener registros de toda la célula, como en el pinzamiento de parches de células completas, conservando al mismo tiempo la mayoría de los mecanismos de señalización intracelular, como en los registros adheridos a células. Como resultado, se reduce el consumo de corriente y las grabaciones estables de parches perforados pueden durar más de una hora. [15] Las desventajas incluyen una mayor resistencia de acceso, en relación con la célula completa, debido a la membrana parcial que ocupa la punta del electrodo. Esto puede disminuir la resolución actual y aumentar el ruido de grabación. El antibiótico también puede tardar un tiempo considerable en perforar la membrana (unos 15 minutos para la anfotericina B, e incluso más para la gramicidina y la nistatina). La membrana debajo de la punta del electrodo se debilita debido a las perforaciones formadas por el antibiótico y puede romperse. Si el parche se rompe, la grabación se realiza en modo de célula completa, con el antibiótico contaminando el interior de la célula. [15]

Una abrazadera de parche suelta se diferencia de las otras técnicas analizadas aquí en que emplea un sello suelto (baja resistencia eléctrica) en lugar del gigaseal apretado utilizado en la técnica convencional. Esta técnica se utilizó ya en el año 1961, como se describe en un artículo de Strickholm sobre la impedancia de la superficie de una célula muscular, [16] pero recibió poca atención hasta que Almers, Stanfield y Stühmer la mencionaron nuevamente y le dieron un nombre. en 1982, [17] después de que el parche abrazadera se estableciera como una herramienta importante de la electrofisiología.
Para lograr una abrazadera de parche suelta en una membrana celular, la pipeta se mueve lentamente hacia la celda, hasta que la resistencia eléctrica del contacto entre la celda y la pipeta aumenta a una resistencia algunas veces mayor que la del electrodo solo. Cuanto más se acerca la pipeta a la membrana, mayor es la resistencia de la punta de la pipeta, pero si se forma un sello demasiado cerca, podría resultar difícil retirar la pipeta sin dañar la célula. En la técnica del parche suelto, la pipeta no se acerca lo suficiente a la membrana para formar un gigasello o una conexión permanente, ni para perforar la membrana celular. [18] La membrana celular permanece intacta y la falta de un sello hermético crea un pequeño espacio a través del cual los iones pueden pasar fuera de la célula sin entrar en la pipeta.
Una ventaja significativa del sello suelto es que la pipeta utilizada se puede retirar repetidamente de la membrana después del registro, y la membrana permanecerá intacta. Esto permite mediciones repetidas en una variedad de ubicaciones en la misma celda sin destruir la integridad de la membrana. Esta flexibilidad ha sido especialmente útil para los investigadores a la hora de estudiar las células musculares a medida que se contraen en condiciones fisiológicas reales, obteniendo registros rápidamente y sin recurrir a medidas drásticas para detener la contracción de las fibras musculares. [17] Una desventaja importante es que la resistencia entre la pipeta y la membrana se reduce considerablemente, lo que permite que la corriente se escape a través del sello y reduce significativamente la resolución de pequeñas corrientes. Sin embargo, esta fuga se puede corregir parcialmente, lo que ofrece la oportunidad de comparar y contrastar grabaciones realizadas en diferentes áreas de la celda de interés. Ante esto, se ha estimado que la técnica del parche suelto puede resolver corrientes menores a 1 mA/cm 2 . [18]
Este método utiliza una combinación de imágenes celulares, secuenciación de ARN y pinzamiento de parche para caracterizar completamente las neuronas en múltiples modalidades. [19] Como los tejidos neurales son una de las poblaciones de células con mayor diversidad transcriptómica , clasificar las neuronas en tipos de células para comprender los circuitos que forman es un desafío importante para los neurocientíficos. La combinación de métodos de clasificación clásicos con la secuenciación post-hoc de ARN unicelular ha demostrado ser difícil y lenta. Al combinar múltiples modalidades de datos, como electrofisiología , secuenciación y microscopía , Patch-seq permite caracterizar las neuronas de múltiples maneras simultáneamente. Actualmente adolece de un bajo rendimiento en comparación con otros métodos de secuenciación, principalmente debido al trabajo manual que implica lograr una grabación exitosa con parche en una neurona. Actualmente se están realizando investigaciones para automatizar la tecnología de fijación de parches, lo que también mejorará el rendimiento de patch-seq. [20]
Se han desarrollado sistemas automatizados de abrazadera de parche para recopilar grandes cantidades de datos de forma económica en un período de tiempo más corto. Dichos sistemas suelen incluir un dispositivo de microfluidos de un solo uso , ya sea un chip moldeado por inyección o un chip fundido de polidimetilsiloxano (PDMS), para capturar una célula o células, y un electrodo integrado.
En una forma de dicho sistema automatizado, se utiliza un diferencial de presión para forzar que las células que se están estudiando sean atraídas hacia la abertura de la pipeta hasta que formen un gigasello. Luego, al exponer brevemente la punta de la pipeta a la atmósfera, la porción de la membrana que sobresale de la pipeta estalla y la membrana ahora está en la conformación de adentro hacia afuera, en la punta de la pipeta. En un sistema completamente automatizado, la pipeta y el parche de membrana se pueden mover rápidamente a través de una serie de diferentes soluciones de prueba, lo que permite aplicar diferentes compuestos de prueba al lado intracelular de la membrana durante el registro. [20]
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )