La paracoccidioidomicosis (PCM) , también conocida como blastomicosis sudamericana , es una infección fúngica que puede presentarse como un tipo de tipo boca-piel, tipo linfangítico , tipo de afectación multiorgánica (particularmente pulmones) o tipo mixto. [1] [6] Si hay úlceras en la boca o lesiones en la piel, es probable que la enfermedad esté diseminada. [1] Puede no haber síntomas, o puede presentarse con fiebre , sepsis, pérdida de peso , glándulas agrandadas o un hígado y bazo grandes . [4] [7]
La causa son hongos del género Paracoccidioides , incluidos Paracoccidioides brasiliensis y Paracoccidioides lutzii , [8] adquiridos al inhalar esporas de hongos. [6]
El diagnóstico se realiza mediante una muestra de sangre , esputo o piel . [4] La enfermedad puede parecerse a la tuberculosis , la leucemia y el linfoma . [4] El tratamiento es con antimicóticos ; itraconazol . [1] [7] Para la enfermedad grave, el tratamiento es con anfotericina B seguida de itraconazol o trimetoprima/sulfametoxazol como alternativa. [1] [7]
Es endémica de América Central y del Sur, [9] y se considera un tipo de enfermedad tropical desatendida . [8] En Brasil, la enfermedad causa alrededor de 200 muertes al año. [1]
La infección pulmonar asintomática es común y menos del 5% de los individuos infectados desarrollan enfermedad clínica. [10]
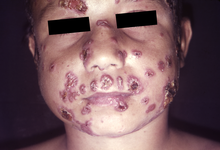
Puede presentarse como un tipo de afectación de boca y piel, tipo linfangítico , tipo de afectación de múltiples órganos (particularmente pulmones) o tipo mixto. [1] [6] Si hay úlceras en la boca o lesiones en la piel, es probable que la enfermedad esté diseminada. [1] Puede no haber síntomas, o puede presentarse con fiebre , sepsis, pérdida de peso , glándulas agrandadas o un hígado y bazo grandes . [4] [7]
Se conocen dos presentaciones: la forma aguda o subaguda, que afecta predominantemente a niños y adultos jóvenes, [11] y la forma crónica , que afecta predominantemente a hombres adultos. [12] La mayoría de los casos se infectan antes de los 20 años, aunque los síntomas pueden presentarse muchos años después. [13]
La forma juvenil aguda se caracteriza por síntomas como fiebre, pérdida de peso y malestar, junto con agrandamiento de los ganglios linfáticos y agrandamiento del hígado y el bazo . [14] [15] [16] Esta forma suele estar diseminada y los síntomas se manifiestan según los órganos afectados. [14] Suelen presentarse lesiones en la piel y las mucosas , [17] y en casos graves puede producirse afectación ósea. [14] Esta presentación aguda y grave puede imitar la tuberculosis , el linfoma o la leucemia . [17]
La forma crónica se presenta meses o años después de que ocurre la infección inicial y con mayor frecuencia se presenta con tos seca y dificultad para respirar. [10] Otros síntomas incluyen exceso de salivación , dificultad para tragar y dificultades con el control de la voz . [14] Pueden estar presentes lesiones en la mucosa del tracto respiratorio superior, así como aumento de la producción de moco y tos con sangre . [18] Es común la afectación pulmonar y extrapulmonar. [14]
Hasta el 70% de los casos tienen afectación de las mucosas, con lesiones que suelen encontrarse en la boca, orofaringe , laringe y paladar. Las lesiones clásicas son úlceras granulares dolorosas superficiales , con pequeñas manchas de sangrado. [15]
La paracoccidioidomicosis es causada por dos especies de hongos que pueden existir como moho o levadura dependiendo de la temperatura , P. brasiliensis y P. lutzii . [19] En ambientes de suelo protegido, cerca de fuentes de agua, que son perturbados ya sea de manera natural o por la actividad humana, se ha observado epidemiológicamente P. brasiliensis (aunque no aislado). [20] Un portador animal conocido es el armadillo . [13] En el ambiente natural, los hongos se encuentran como estructuras filamentosas y desarrollan esporas infecciosas conocidas como conidios . [13]
Nunca se ha demostrado la transmisión entre humanos. [21]
Se cree que la infección primaria, aunque poco conocida debido a la falta de datos, ocurre a través de la inhalación de conidios a través del tracto respiratorio, después de inhalar conidios fúngicos producidos por la forma micelial de P. brasiliensis . [14] [21] Esto ocurre predominantemente en la infancia y la adultez temprana, después de la exposición a la actividad agrícola. [13] La infección puede ocurrir a través de la inoculación directa de la piel, aunque esto es poco común. [15]
Después de la inhalación en los alvéolos , se produce una rápida multiplicación del organismo en el tejido pulmonar, propagándose a veces a través de los sistemas venoso y linfático. [14] Aproximadamente el 2% de las personas desarrollan características clínicas después de la infección asintomática inicial. [15]
El tipo de respuesta inmunitaria determina la manifestación clínica de la infección, siendo los niños y los individuos coinfectados con VIH los que más comúnmente desarrollan la enfermedad diseminada aguda/subaguda. [14] La mayoría de los infectados desarrollan una respuesta inmunitaria mediada por células T tipo 1 ( Th1 ), que resulta en alveolitis fibrosante y formación de granulomas compactos que controlan la replicación fúngica y una infección latente o asintomática. [13] [14] Luego se cree que permanece latente en las lesiones pulmonares residuales y los ganglios linfáticos mediastínicos . [21] Una respuesta deficiente de células Th1 resulta en las formas graves de la enfermedad. En estos individuos, no se forman granulomas y la persona afectada desarrolla respuestas Th2 y Th9, lo que resulta en la activación de los linfocitos B , altos niveles de anticuerpos circulantes, eosinofilia e hipergammaglobulinemia . [13]
La afectación pulmonar ocurre posteriormente después de una fase latente, manifestándose en síntomas del tracto respiratorio superior e infiltrados pulmonares en las imágenes. [15] La forma crónica más común es casi con certeza una reactivación de la enfermedad, [15] y puede evolucionar hacia una cicatrización progresiva de los pulmones (fibrosis pulmonar) . [22]
Puede causar enfermedad en personas con función inmunológica normal, aunque la inmunosupresión aumenta la agresividad del hongo. Rara vez causa enfermedad en mujeres en edad fértil, probablemente debido a un efecto protector del estradiol . [23]
Más del 90% de los casos pueden diagnosticarse con examen histológico directo de tejidos, como esputo, líquido de lavado bronquial, exudados y biopsias . El estudio histopatológico con tinción de plata metenamina de Gomori (GMS) o tinción de hematoxilina y eosina ( H&E ) revela células de levadura grandes con paredes celulares translúcidas con múltiples brotes. [14]
En la forma juvenil, las anomalías pulmonares se muestran en tomografías computarizadas de alta resolución de los pulmones, mientras que en la forma crónica las radiografías simples pueden mostrar infiltrados intersticiales y alveolares en los campos pulmonares centrales e inferiores. [14]
El cultivo de P. brasiliensis demora entre 20 y 30 días y requiere múltiples muestras y medios de cultivo. El cultivo inicial puede realizarse a temperatura ambiente, sin embargo, una vez que se observa el crecimiento, se confirma incubando a 36-37 grados para transformar el hongo en células de levadura. [14]
La detección de anticuerpos es útil tanto para el diagnóstico agudo como para el seguimiento. La inmunodifusión en gel se utiliza habitualmente en zonas endémicas y diagnostica el 95% de los casos con una alta especificidad . [14] La fijación del complemento permite medir la gravedad de los casos cuantificando el nivel de anticuerpos y, por tanto, es útil para controlar la respuesta al tratamiento. Sin embargo, solo es sensible en el 85% de los casos y reacciona de forma cruzada con H. capsulatum . [14]
La enfermedad puede parecerse a la tuberculosis , la leucemia y el linfoma [4].
Tanto P. brasiliensis como P. lutzii son susceptibles in vitro a la mayoría de los agentes antimicóticos, a diferencia de otras infecciones fúngicas sistémicas . Las formas leves y moderadas se tratan con itraconazol durante 9 a 18 meses, ya que se ha demostrado que es más eficaz, tiene una duración de tratamiento más corta y es más tolerado. [ cita requerida ] Se ha demostrado que las bebidas ácidas reducen la absorción de itraconazol. [13] El cotrimoxazol es un agente de segunda línea y se prefiere para aquellos con afectación cerebral y durante el embarazo. [13] Para los casos graves, está indicado el tratamiento intravenoso con anfotericina B , durante un promedio de 2 a 4 semanas. [13] La prednisolona prescrita al mismo tiempo puede reducir la inflamación durante el tratamiento. [13] Los pacientes deben ser tratados hasta la estabilización de los síntomas y el aumento del peso corporal. Se debe proporcionar asesoramiento sobre el apoyo nutricional, así como el tabaquismo y la ingesta de alcohol. La insuficiencia suprarrenal , si se encuentra, se trata con corticosteroides. [24] Los criterios clínicos de curación incluyen la ausencia o curación de lesiones, estabilización del peso corporal y pruebas de autoanticuerpos negativas y negativas. [13] No hay datos suficientes para respaldar los beneficios de los medicamentos mencionados anteriormente para tratar la enfermedad. [25]
La paracoccidioidomicosis es endémica en las zonas rurales de América Latina, desde el sur de México hasta Argentina, y también se encuentra en Brasil, Colombia, Venezuela, Ecuador y Paraguay. [13] [15] Nunca se ha observado un brote epidémico. [13] Tiene la prevalencia más alta de todas las micosis sistémicas (infecciones fúngicas) en el área. [12] Se ha estimado que hasta el 75% de las personas en áreas endémicas están infectadas con la forma asintomática (hasta 10 millones de personas), y el 2% desarrolla una enfermedad clínicamente significativa. [12] La morbilidad y la mortalidad están fuertemente asociadas con el entorno socioeconómico del paciente, [12] y la mayoría de los pacientes adultos son trabajadores agrícolas varones. [26] Otros factores de riesgo incluyen el tabaquismo, el consumo de alcohol, la coinfección por VIH u otra inmunosupresión. [21] El 80% de los casos notificados se encuentran en Brasil, en el sureste, medio oeste y sur, y se extendieron en la década de 1990 al área amazónica. La mayoría de las infecciones restantes se encuentran en Argentina, Colombia y Venezuela. [21] La mayoría de los informes epidemiológicos se han centrado en P. brasliensis , y hasta 2015 la epidemiología de P. lutzii era poco conocida. [21]
El aumento de casos se ha relacionado con la agriculturización y la deforestación en Brasil, la urbanización en áreas periféricas de las ciudades con infraestructura deficiente, así como el aumento de la humedad del suelo y del aire. [13] [21] Una tribu indígena brasileña, los suruí, después de cambiar de la agricultura de subsistencia al cultivo de café, mostró tasas de infección más altas que las tribus circundantes. [21]
También se han registrado casos en zonas no endémicas con el auge del ecoturismo, en Estados Unidos, Europa y Japón. [15] Todos los casos notificados fueron viajeros que regresaron de regiones endémicas. [21]
La enfermedad de Lutz-Splendore-de Almeida [3] recibe su nombre de los médicos Adolfo Lutz , [27] Alfonso Splendore (1871-1953), un parasitólogo italobrasileño [28] y Floriano Paulo de Almeida (1898-1977), un patólogo brasileño especializado en Micología Patológica (Estudio de Hongos Infecciosos), [29] [30] quienes caracterizaron por primera vez la enfermedad en Brasil a principios del siglo XX.
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )