
La fotoquímica es la rama de la química que se ocupa de los efectos químicos de la luz. Generalmente, este término se utiliza para describir una reacción química causada por la absorción de radiación ultravioleta ( longitud de onda de 100 a 400 nm ), visible (400 a 750 nm) o infrarroja (750 a 2500 nm). [1]
En la naturaleza, la fotoquímica es de inmensa importancia ya que es la base de la fotosíntesis, la visión y la formación de vitamina D con la luz solar. [2] También es responsable de la aparición de mutaciones en el ADN que conducen a cánceres de piel. [3]
Las reacciones fotoquímicas se desarrollan de manera diferente a las reacciones impulsadas por la temperatura. Las rutas fotoquímicas acceden a intermediarios de alta energía que no pueden generarse térmicamente, superando así grandes barreras de activación en un corto período de tiempo y permitiendo reacciones que de otro modo serían inaccesibles mediante procesos térmicos. La fotoquímica también puede ser destructiva, como lo ilustra la fotodegradación de los plásticos.
La fotoexcitación es el primer paso de un proceso fotoquímico en el que el reactivo se eleva a un estado de mayor energía, un estado excitado . La primera ley de la fotoquímica, conocida como ley de Grotthuss-Draper (por los químicos Theodor Grotthuss y John W. Draper ), establece que la luz debe ser absorbida por una sustancia química para que se produzca una reacción fotoquímica . Según la segunda ley de la fotoquímica, conocida como ley de Stark-Einstein (por los físicos Johannes Stark y Albert Einstein ), por cada fotón de luz absorbido por un sistema químico, no se activa más de una molécula para una reacción fotoquímica, tal como se define por el rendimiento cuántico . [4] [5]
Cuando una molécula o átomo en el estado fundamental (S 0 ) absorbe luz, un electrón se excita a un nivel orbital más alto. Este electrón mantiene su espín según la regla de selección de espín; otras transiciones violarían la ley de conservación del momento angular . La excitación a un estado singlete superior puede ser de HOMO a LUMO o a un orbital superior, de modo que son posibles estados de excitación singlete S 1 , S 2 , S 3 ... con diferentes energías.
La regla de Kasha estipula que los estados singlete superiores se relajarían rápidamente mediante desintegración sin radiación o conversión interna (IC) a S 1 . Por tanto, S 1 suele ser, aunque no siempre, el único estado excitado singlete relevante. Este estado excitado S 1 puede relajarse aún más a S 0 mediante IC, pero también mediante una transición radiativa permitida de S 1 a S 0 que emite un fotón; este proceso se llama fluorescencia .
Alternativamente, es posible que el estado excitado S1 experimente una inversión de espín y genere un estado excitado triplete T1 que tenga dos electrones desapareados con el mismo espín. Esta violación de la regla de selección de espín es posible mediante el cruce entre sistemas (ISC) de los niveles vibratorios y electrónicos de S 1 y T 1 . Según la regla de máxima multiplicidad de Hund , este estado T 1 sería algo más estable que S 1 .
Este estado triplete puede relajarse hasta el estado fundamental S 0 mediante ISC sin radiación o mediante una vía de radiación llamada fosforescencia . Este proceso implica un cambio de espín electrónico, que está prohibido por las reglas de selección de espín, lo que hace que la fosforescencia (de T 1 a S 0 ) sea mucho más lenta que la fluorescencia (de S 1 a S 0 ). Por lo tanto, los estados tripletes generalmente tienen vidas más largas que los estados singletes. Estas transiciones suelen resumirse en un diagrama de energía de estado o diagrama de Jablonski , el paradigma de la fotoquímica molecular.
Estas especies excitadas, ya sea S 1 o T 1 , tienen un orbital de baja energía medio vacío y, en consecuencia, son más oxidantes que el estado fundamental. Pero al mismo tiempo, tienen un electrón en un orbital de alta energía y, por tanto, son más reductores . En general, las especies excitadas son propensas a participar en procesos de transferencia de electrones. [6]

Las reacciones fotoquímicas requieren una fuente de luz que emita longitudes de onda correspondientes a una transición electrónica en el reactivo. En los primeros experimentos (y en la vida cotidiana), la fuente de luz era la luz del sol, aunque es policromática. [7] Las lámparas de vapor de mercurio son más comunes en el laboratorio. Las lámparas de vapor de mercurio de baja presión emiten principalmente a 254 nm. Para fuentes policromáticas, los rangos de longitud de onda se pueden seleccionar mediante filtros. Alternativamente, los rayos láser suelen ser monocromáticos (aunque se pueden obtener dos o más longitudes de onda utilizando ópticas no lineales ), y los LED tienen una banda relativamente estrecha que puede usarse de manera eficiente, así como las lámparas Rayonet, para obtener haces aproximadamente monocromáticos.

La luz emitida debe llegar al grupo funcional objetivo sin ser bloqueada por el reactor, el medio u otros grupos funcionales presentes. En muchas aplicaciones, el cuarzo se utiliza tanto para los reactores como para contener la lámpara. Pyrex absorbe en longitudes de onda inferiores a 275 nm. El disolvente es un parámetro experimental importante. Los disolventes son reactivos potenciales y, por esta razón, se evitan los disolventes clorados porque el enlace C-Cl puede provocar la cloración del sustrato. Los disolventes de fuerte absorción impiden que los fotones lleguen al sustrato. Los disolventes de hidrocarburos absorben sólo en longitudes de onda cortas y, por tanto, se prefieren para experimentos fotoquímicos que requieren fotones de alta energía. Los disolventes que contienen insaturación absorben en longitudes de onda más largas y pueden filtrar de forma útil longitudes de onda cortas. Por ejemplo, el ciclohexano y la acetona se "cortan" (se absorben fuertemente) en longitudes de onda inferiores a 215 y 330 nm, respectivamente.
Normalmente, la longitud de onda empleada para inducir un proceso fotoquímico se selecciona en función del espectro de absorción de las especies reactivas, normalmente el máximo de absorción. En los últimos años [ ¿cuándo? ] , sin embargo, se ha demostrado que, en la mayoría de las reacciones de formación de enlaces, el espectro de absorción no permite seleccionar la longitud de onda óptima para lograr el mayor rendimiento de la reacción en función de la absortividad. Este desajuste fundamental entre absortividad y reactividad se ha dilucidado con los llamados gráficos de acción fotoquímica . [8] [9]
La fotoquímica de flujo continuo ofrece múltiples ventajas sobre la fotoquímica por lotes. Las reacciones fotoquímicas están impulsadas por la cantidad de fotones que pueden activar las moléculas que causan la reacción deseada. La gran relación superficie-volumen de un microrreactor maximiza la iluminación y, al mismo tiempo, permite un enfriamiento eficiente, lo que disminuye los productos térmicos secundarios. [10]
En el caso de reacciones fotoquímicas, la luz proporciona la energía de activación . De manera simplista, la luz es un mecanismo para proporcionar la energía de activación necesaria para muchas reacciones. Si se emplea luz láser , es posible excitar selectivamente una molécula para producir un estado electrónico y vibratorio deseado. [11] Del mismo modo, las emisiones de un estado particular pueden ser monitoreadas selectivamente, proporcionando una medida de la población de ese estado. Si el sistema químico está a baja presión, esto permite a los científicos observar la distribución de energía de los productos de una reacción química antes de que las diferencias de energía hayan sido borradas y promediadas por repetidas colisiones.
La absorción de un fotón por una molécula reactiva también puede permitir que se produzca una reacción no sólo llevando la molécula a la energía de activación necesaria, sino también cambiando la simetría de la configuración electrónica de la molécula, permitiendo una ruta de reacción que de otro modo sería inaccesible, como se describe por las reglas de selección de Woodward-Hoffmann . Una reacción de cicloadición [2+2] es un ejemplo de reacción pericíclica que puede analizarse utilizando estas reglas o mediante la teoría de orbitales moleculares de frontera relacionada .
Algunas reacciones fotoquímicas son varios órdenes de magnitud más rápidas que las reacciones térmicas; A menudo se observan reacciones de hasta 10 −9 segundos y procesos asociados de hasta 10 −15 segundos.
El fotón puede ser absorbido directamente por el reactivo o por un fotosensibilizador , que absorbe el fotón y transfiere la energía al reactivo. El proceso opuesto, cuando un reactivo químico desactiva un estado fotoexcitado, se llama extinción .
La mayoría de las transformaciones fotoquímicas ocurren mediante una serie de pasos simples conocidos como procesos fotoquímicos primarios. Un ejemplo común de estos procesos es la transferencia de protones en estado excitado.
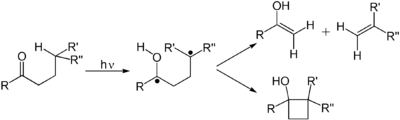
Ejemplos de reacciones orgánicas fotoquímicas son reacciones electrocíclicas , reacciones radicalarias , fotoisomerización y reacciones de Norrish . [20] [21]
Los alquenos experimentan muchas reacciones importantes que se desarrollan a través de una transición de π a π* inducida por fotones. El primer estado excitado electrónico de un alqueno carece del enlace π , de modo que la rotación alrededor del enlace C-C es rápida y la molécula participa en reacciones que no se observan térmicamente. Estas reacciones incluyen isomerización cis-trans y cicloadición a otro alqueno (estado fundamental) para dar derivados de ciclobutano . La isomerización cis-trans de un (poli)alqueno está implicada en la retina , un componente de la maquinaria de la visión . La dimerización de alquenos es relevante para el fotodaño del ADN , donde se observan dímeros de timina al iluminar el ADN con radiación UV. Estos dímeros interfieren con la transcripción . Los efectos beneficiosos de la luz solar están asociados con la reacción de retrociclación (desciclización) del ergosterol inducida fotoquímicamente para producir vitamina D. En la reacción de DeMayo , un alqueno reacciona con una 1,3-dicetona a través de su enol para producir una 1,5-dicetona. Otra reacción fotoquímica común es el reordenamiento de di-π-metano de Howard Zimmerman .
En una aplicación industrial, se preparan anualmente alrededor de 100.000 toneladas de cloruro de bencilo mediante la reacción fotoquímica en fase gaseosa de tolueno con cloro . [22] La luz es absorbida por las moléculas de cloro; la baja energía de esta transición queda indicada por el color amarillento del gas. El fotón induce la homólisis del enlace Cl-Cl y el radical cloro resultante convierte el tolueno en radical bencilo:
Los mercaptanos se pueden producir mediante la adición fotoquímica de sulfuro de hidrógeno (H 2 S) a alfa olefinas .
Los complejos de coordinación y los compuestos organometálicos también son fotorreactivos. Estas reacciones pueden implicar una isomerización cis-trans. Más comúnmente, las fotorreacciones dan como resultado la disociación de ligandos, ya que el fotón excita un electrón del metal a un orbital que es antienlazante con respecto a los ligandos. Por tanto, los carbonilos metálicos que resisten la sustitución térmica sufren descarbonilación tras la irradiación con luz ultravioleta. La irradiación UV de una solución de hexacarbonilo de molibdeno en THF produce el complejo de THF, que es sintéticamente útil:
En una reacción relacionada, la fotólisis del pentacarbonilo de hierro produce nonacarbonilo de hierro (ver figura):
Algunos complejos de coordinación fotorreactivos pueden sufrir procesos de oxidación-reducción mediante transferencia de un solo electrón. Esta transferencia de electrones puede ocurrir dentro de la esfera de coordinación interna o externa del metal. [23]
Aquí hay algunos tipos diferentes de reacciones fotoquímicas.
Aunque el blanqueo se practica desde hace mucho tiempo, la primera reacción fotoquímica fue descrita por Trommsdorff en 1834. [24] Observó que los cristales del compuesto α-santonina cuando se exponían a la luz solar se volvían amarillos y estallaban. En un estudio de 2007, la reacción se describió como una sucesión de tres pasos que tienen lugar dentro de un solo cristal. [25]
El primer paso es una reacción de reordenamiento a un intermedio de ciclopentadienona ( 2 ), el segundo una dimerización en una reacción de Diels-Alder ( 3 ) y el tercero una cicloadición intramolecular [2+2] ( 4 ). El efecto de estallido se atribuye a un gran cambio en el volumen del cristal durante la dimerización.
La organización de estas conferencias está facilitada por la Fundación Internacional de Fotoquímica. [26]