
Los iluros de azometina son 1,3-dipolos a base de nitrógeno , que consisten en un ion iminio junto a un carbanión . Se utilizan en reacciones de cicloadición 1,3-dipolares para formar heterociclos de cinco miembros , incluidas pirrolidinas y pirrolinas . [1] [2] [3] Estas reacciones son altamente estereo y regioselectivas y tienen el potencial de formar cuatro nuevos estereocentros contiguos. Por lo tanto, los iluros de azometina tienen una gran utilidad en la síntesis total y en la formación de ligandos quirales y productos farmacéuticos . Los iluros de azometina se pueden generar a partir de muchas fuentes, incluidas aziridinas, iminas e iminios. A menudo se generan in situ y reaccionan inmediatamente con dipolarófilos.
Las estructuras de resonancia a continuación muestran la contribución del 1,3-dipolo , en el que los dos átomos de carbono adyacentes al nitrógeno tienen una carga negativa o positiva. [1] La representación más común de iluros de azometino es aquella en la que el nitrógeno está cargado positivamente y la carga negativa se comparte entre los dos átomos de carbono. Las contribuciones relativas de las diferentes estructuras de resonancia dependen de los sustituyentes de cada átomo. El carbono que contiene sustituyentes aceptores de electrones tendrá una carga negativa más parcial, debido a la capacidad del grupo aceptor de electrones cercano para estabilizar la carga negativa.
Son posibles tres formas de iluro diferentes, cada una de las cuales conduce a una estereoquímica diferente en los productos de reacciones de cicloadición 1,3-dipolares . Son posibles ilusiones en forma de W, U y S. [1] Los iluros en forma de W y U, en los que los sustituyentes R están en el mismo lado, dan como resultado productos de cicloadición sin , mientras que los iluros en forma de S dan como resultado productos anti . En los ejemplos siguientes, el lugar donde el sustituyente R 3 termina en el producto depende de la naturaleza estérica y electrónica del sustituyente (ver regioselectividad de las cicloadiciones 1,3 dipolares ). La estereoquímica de R 1 y R 2 en el producto de cicloadición se deriva del dipolo. La estereoquímica de R 3 se deriva del dipolarófilo: si el dipolarófilo está más que monosustituido (y es proquiral ), pueden resultar en el producto hasta cuatro nuevos estereocentros.

Los iluros de azometina se pueden generar a partir de la apertura del anillo de aziridinas . [4] [5] De acuerdo con las reglas de Woodward-Hoffmann , la apertura térmica del anillo de cuatro electrones se produce mediante un proceso conrotatorio , mientras que la reacción fotoquímica es disrotatoria.

En esta reacción de apertura del anillo, existe un problema de torquoselectividad . Los sustituyentes electronegativos prefieren rotar hacia afuera, hacia el mismo lado que el sustituyente R en el nitrógeno, mientras que los sustituyentes electropositivos prefieren rotar hacia adentro. [6]
Tenga en cuenta que con las aziridinas, la apertura del anillo puede dar como resultado un dipolo 1,3 diferente , en el que se rompe un enlace C-N (en lugar del enlace C-C). [7]

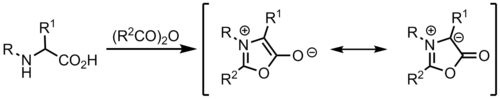
Uno de los métodos más sencillos para formar iluros de azometino es mediante la condensación de un aldehído con una amina . Si la amina contiene un grupo aceptor de electrones en el carbono alfa, como un éster , la desprotonación se produce fácilmente. Una posible desventaja de utilizar este método es que el éster termina en el producto de cicloadición. Una alternativa es utilizar un ácido carboxílico , que puede eliminarse fácilmente durante el proceso de cicloadición mediante descarboxilación . [8]

Los iluros de azometina también se pueden formar directamente por desprotonación de iminios.

Los reactivos metálicos utilizados en esta reacción incluyen bromuro de litio y acetato de plata . [1] En este método, el metal se coordina con el nitrógeno para activar el sustrato para la desprotonación. Otra forma de formar iluros de azometino a partir de iminas es mediante prototropía y alquilación .
Los iluros se pueden formar a partir de münchnonas , que son heterociclos mesoiónicos y actúan como iluros de azometino cíclicos. [9]

Al igual que con otras reacciones de cicloadición de un 1,3-dipolo con un sistema π, la cicloadición 1,3-dipolar utilizando un iluro de azometina es un proceso de seis electrones. Según las reglas de Woodward-Hoffmann , esta adición es suprafacial respecto tanto del dipolo como del dipolarófilo . La reacción generalmente se considera concertada , en la que los dos enlaces carbono-carbono se forman al mismo tiempo, pero de forma asincrónica. Sin embargo, dependiendo de la naturaleza del dipolo y del dipolarófilo, son posibles intermedios dirradicales o zwitteriónicos . [10] Generalmente se favorece el producto endo , como en la reacción isoelectrónica de Diels-Alder . En estas reacciones, el iluro de azometina es típicamente el HOMO , y el dipolarófilo con deficiencia de electrones el LUMO, aunque se sabe que ocurren reacciones de cicloadición con sistemas π inactivados, especialmente cuando la ciclación es intramolecular. [11] Para una discusión sobre la teoría de orbitales moleculares de frontera de las cicloadiciones 1,3-dipolares, consulte Cicloadición 1,3-dipolar # Teoría de orbitales moleculares de frontera .

Las reacciones de cicloadición 1,3-dipolar de iluros de azometino comúnmente utilizan alquenos o alquinos como dipolarófilos, para formar pirrolidinas o pirrolinas , respectivamente. Arriba se muestra una reacción de un iluro de azometina con un alqueno y da como resultado una pirrolidina. [12] Este tipo de reacciones se pueden utilizar para sintetizar Ullazina. [13] Si bien los dipolarófilos son típicamente compuestos carbonílicos α, β-insaturados , ha habido muchos avances recientes en el desarrollo de nuevos tipos de dipolarófilos. [14]
Cuando el dipolo y el dipolarófilo forman parte de la misma molécula, una reacción de ciclación intramolecular puede dar lugar a un producto policíclico de considerable complejidad. [1] Si el dipolarófilo está atado a un carbono del dipolo, se forma una bicicleta fusionada. Si está unido al nitrógeno, se produce una estructura puenteada. La naturaleza intramolecular de la reacción también puede resultar útil porque la regioselectividad suele estar limitada. Otra ventaja de las reacciones intramoleculares es que el dipolarófilo no necesita tener deficiencia de electrones; se han informado muchos ejemplos de reacciones de ciclación con dipolarófilos sustituidos con alquilo, ricos en electrones, incluida la síntesis de ácido martinélico que se muestra a continuación.
A diferencia de la mayoría de las reacciones de cicloadición 1,3-dipolares, en las que la estereoquímica del dipolo se pierde o es inexistente, los iluros de azometina pueden conservar su estereoquímica. Esto generalmente se hace mediante la apertura del anillo de una aziridina y el posterior atrapamiento por un dipolarófilo antes de que la estereoquímica pueda alterarse.
Al igual que otras reacciones de cicloadición 1,3-dipolar, las cicloadiciones de iluro de azometina pueden formar productos endo o exo. Esta selectividad se puede ajustar mediante catálisis de metales. [15] [16]
La cicloadición enantioselectiva de iluros de azometina utilizando catalizadores quirales se describió por primera vez en un trabajo fundamental de Allway y Grigg en 1991. [17] Este poderoso método fue desarrollado aún más por Jørgensen y Zhang. Estas reacciones generalmente utilizan complejos de zinc , plata , cobre , níquel y calcio .
Utilizando catalizadores de fosfina quirales , se pueden sintetizar espiroindolinonas enantioméricamente puras. El método descrito por Gong, et al. conduce a un resultado regioquímico inesperado que no sigue a los efectos electrónicos. Esto se atribuye al apilamiento favorable de pi con el catalizador. [18]
Los iluros de azometino conjugados son capaces de realizar electrociclaciones [1,5] y [1,7] . [19] A continuación se muestra un ejemplo de una [1,7]-electrociclación de un iluro de azometino sustituido con difeniletenilo. Este cierre conrotatorio del anillo es seguido por un desplazamiento suprafacial de [1,5]-hidruro, que produce el producto rearomatizado. La estérica y la geometría del anillo de fenilo que reacciona juegan un papel importante en el éxito de la reacción. [20]

Los compuestos resultantes de este tipo de electrociclación se han utilizado como dienos en reacciones de Diels-Alder para unir compuestos a fullerenos . [21]

Se utilizó una cicloadición de un iluro de azometino con un alqueno inactivado en la síntesis total de ácido martinélico. El paso de cicloadición formó dos anillos, incluida una pirrolidina , y dos estereocentros. [22]

En la síntesis de espirotriprostatina B , se forma un iluro de azometina a partir de la condensación de una amina con un aldehído . Luego, el iluro reacciona con un alqueno deficiente en electrones en una indolinona, lo que resulta en la formación de una pirrolidina espirocíclica y cuatro estereocentros contiguos. [23]
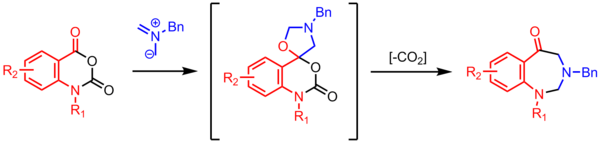
La ciclación de un iluro de azometino con un carbonilo produce una oxazolidina espirocíclica , que pierde CO 2 para formar un anillo de siete miembros. Estas reacciones descarboxilativas de múltiples pasos de alta utilidad son comunes en la química del iluro de azometina. [24]