El glucagón es una hormona peptídica producida por las células alfa del páncreas . Aumenta la concentración de glucosa y ácidos grasos en el torrente sanguíneo y se considera la principal hormona catabólica del cuerpo. [1] También se utiliza como medicamento para tratar una serie de condiciones de salud. Su efecto es opuesto al de la insulina , que reduce la glucosa extracelular. [2] Se produce a partir del proglucagón , codificado por el gen GCG .
El páncreas libera glucagón cuando la cantidad de glucosa en el torrente sanguíneo es demasiado baja. El glucagón hace que el hígado participe en la glucogenólisis : convertir el glucógeno almacenado en glucosa , que se libera al torrente sanguíneo. [3] Los niveles elevados de glucosa en sangre, por otro lado, estimulan la liberación de insulina. La insulina permite que los tejidos dependientes de insulina absorban y utilicen la glucosa. Así, el glucagón y la insulina forman parte de un sistema de retroalimentación que mantiene estables los niveles de glucosa en sangre. El glucagón aumenta el gasto energético y se eleva en condiciones de estrés. [4] El glucagón pertenece a la familia de hormonas secretinas .
El glucagón es un polipéptido de 29 aminoácidos . Su estructura primaria en humanos es: NH 2 - His - Ser - Gln - Gly - Thr - Phe - Thr - Ser - Asp - Tyr - Ser - Lys - Tyr - Leu - Asp - Ser - Arg - Arg - Ala - Gln - Asp - Phe - Val - Gln - Trp - Leu - Met - Asn - Thr - COOH (HSQGTFTSDYSKYLDSRRAQDFVQWLMNT).
El polipéptido tiene una masa molecular de 3485 daltons . [5] El glucagón es una hormona peptídica (no esteroide ).

La hormona se sintetiza y secreta a partir de las células alfa (células α) de los islotes de Langerhans , que se encuentran en la porción endocrina del páncreas. El glucagón se produce a partir del gen preproglucagón Gcg . Primero, la peptidasa señal elimina el péptido señal del preproglucagón , formando la proteína proglucagón de 160 aminoácidos . [6] Luego, el proglucagón es escindido por la proproteína convertasa 2 en glucagón (aminoácidos 33-61) en las células α de los islotes pancreáticos. En las células L intestinales , el proglucagón se escinde en los productos alternativos glicentina (1–69), polipéptido pancreático relacionado con la glicentina (1–30), oxintomodulina (33–69), péptido similar al glucagón 1 (72–107 o 108), y el péptido 2 similar al glucagón (126-158). [6]
En los roedores, las células alfa se encuentran en el borde exterior del islote. La estructura de los islotes humanos está mucho menos segregada y las células alfa se distribuyen por todo el islote muy cerca de las células beta. El glucagón también es producido por las células alfa del estómago. [7]
Investigaciones recientes han demostrado que la producción de glucagón también puede tener lugar fuera del páncreas, siendo el intestino el sitio más probable de síntesis extrapancreática de glucagón. [8]
La producción, que de otro modo funciona libremente, es suprimida/regulada por la amilina , una hormona peptídica cosecretada con la insulina de las células β pancreáticas. [9] A medida que los niveles de glucosa en plasma disminuyen, la reducción posterior en la secreción de amilina alivia la supresión de las células α, lo que permite la secreción de glucagón.
La secreción de glucagón es estimulada por:
La secreción de glucagón se inhibe por:
El glucagón generalmente eleva la concentración de glucosa en la sangre al promover la gluconeogénesis y la glucogenólisis . [17] El glucagón también disminuye la síntesis de ácidos grasos en el tejido adiposo y el hígado, además de promover la lipólisis en estos tejidos, lo que hace que liberen ácidos grasos a la circulación, donde pueden catabolizarse para generar energía en tejidos como el músculo esquelético cuando sea necesario. . [18]
La glucosa se almacena en el hígado en forma de glucógeno polisacárido , que es un glucano (un polímero formado por moléculas de glucosa). Las células del hígado ( hepatocitos ) tienen receptores de glucagón . Cuando el glucagón se une a los receptores de glucagón, las células del hígado convierten el glucógeno en moléculas de glucosa individuales y las liberan al torrente sanguíneo, en un proceso conocido como glucogenólisis . A medida que estas reservas se agotan, el glucagón estimula al hígado y al riñón a sintetizar glucosa adicional mediante gluconeogénesis . El glucagón desactiva la glucólisis en el hígado, lo que provoca que los intermediarios glucolíticos sean transportados a la gluconeogénesis.
El glucagón también regula la tasa de producción de glucosa mediante lipólisis. El glucagón induce la lipólisis en humanos en condiciones de supresión de insulina (como la diabetes mellitus tipo 1 ). [19]
La producción de glucagón parece depender del sistema nervioso central a través de vías aún por definir. En animales invertebrados , se ha informado que la eliminación del pedúnculo afecta la producción de glucagón. "La extirpación del pedúnculo ocular en cangrejos jóvenes produce hiperglucemia inducida por glucagón ". [20]
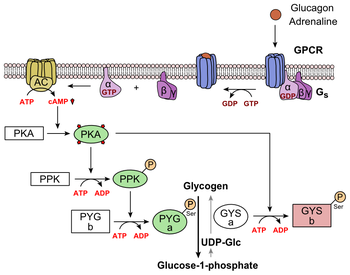
El glucagón se une al receptor de glucagón , un receptor acoplado a proteína G , ubicado en la membrana plasmática de la célula. El cambio de conformación en el receptor activa una proteína G , una proteína heterotrimérica con subunidades αs , β y γ. Cuando la proteína G interactúa con el receptor, sufre un cambio conformacional que resulta en el reemplazo de la molécula de GDP que estaba unida a la subunidad α por una molécula de GTP . [21] Esta sustitución da como resultado la liberación de la subunidad α de las subunidades β y γ. La subunidad alfa activa específicamente la siguiente enzima de la cascada, la adenilato ciclasa .
La adenilato ciclasa fabrica monofosfato de adenosina cíclico (AMP cíclico o AMPc), que activa la proteína quinasa A (proteína quinasa dependiente de AMPc). Esta enzima, a su vez, activa la fosforilasa quinasa , que luego fosforila la glucógeno fosforilasa b (PYG b), convirtiéndola en la forma activa llamada fosforilasa a (PYG a). La fosforilasa a es la enzima responsable de la liberación de glucosa 1-fosfato de los polímeros de glucógeno. Un ejemplo de esta vía sería cuando el glucagón se une a una proteína transmembrana. Las proteínas transmembrana interactúan con Gɑβ𝛾. Gαs se separa de Gβ𝛾 e interactúa con la proteína transmembrana adenilil ciclasa. La adenilil ciclasa cataliza la conversión de ATP en AMPc. El AMPc se une a la proteína quinasa A y el complejo fosforila la glucógeno fosforilasa quinasa. [22] La glucógeno fosforilasa quinasa fosforilada fosforila la glucógeno fosforilasa . La glucógeno fosforilasa fosforilada separa las unidades de glucosa del glucógeno como glucosa 1-fosfato.
Además, el control coordinado de la glucólisis y la gluconeogénesis en el hígado se ajusta mediante el estado de fosforilación de las enzimas que catalizan la formación de un potente activador de la glucólisis llamado fructosa 2,6-bifosfato. [23] La enzima proteína quinasa A (PKA) que fue estimulada por la cascada iniciada por el glucagón también fosforilará un único residuo de serina de la cadena polipeptídica bifuncional que contiene las enzimas fructosa 2,6-bisfosfatasa y fosfofructoquinasa-2. Esta fosforilación covalente iniciada por el glucagón activa el primero e inhibe el segundo. Esto regula la reacción que cataliza la fructosa 2,6-bifosfato (un potente activador de la fosfofructoquinasa-1, la enzima que es el principal paso regulador de la glucólisis) [24] al disminuir la velocidad de su formación, inhibiendo así el flujo de la vía de la glucólisis. y permitiendo que predomine la gluconeogénesis. Este proceso es reversible en ausencia de glucagón (y, por tanto, en presencia de insulina).
La estimulación con glucagón de la PKA inactiva la enzima glucolítica piruvato quinasa , [25] inactiva la glucógeno sintasa , [26] y activa la lipasa sensible a hormonas , [27] que cataboliza los glicéridos en glicerol y ácidos grasos libres en los hepatocitos.
El glucagón también inactiva la acetil-CoA carboxilasa , que crea malonil-CoA a partir de acetil-CoA, a través de quinasas dependientes y/o independientes de AMPc. [28]
La malonil-CoA es un subproducto del ciclo de Krebs (después de la glucólisis) y un inhibidor alostérico de la carnitina palmitoiltransferasa I (CPT1) , una enzima mitocondrial importante para llevar ácidos grasos al espacio intermembrana de las mitocondrias para la β-oxidación. [29] El glucagón disminuye la malonil-CoA mediante la inhibición de la acetil-CoA carboxilasa y mediante la reducción de la glucólisis mediante la reducción antes mencionada de la fructosa 2,6-bisfosfato. Por tanto, la reducción de malonil-CoA es un regulador común de los efectos del aumento del metabolismo de los ácidos grasos del glucagón.
Los niveles anormalmente elevados de glucagón pueden ser causados por tumores pancreáticos , como el glucagonoma , cuyos síntomas incluyen eritema migratorio necrolítico , [30] reducción de aminoácidos e hiperglucemia. Puede ocurrir sola o en el contexto de una neoplasia endocrina múltiple tipo 1 . [31]
El nivel elevado de glucagón es el principal contribuyente a la cetoacidosis hiperglucémica en la diabetes tipo 1 no diagnosticada o mal tratada. A medida que las células beta dejan de funcionar, la insulina y el GABA pancreático ya no están presentes para suprimir la producción libre de glucagón. Como resultado, las células alfa liberan glucagón al máximo, lo que provoca una rápida descomposición del glucógeno en glucosa y una cetogénesis rápida . [32] Se descubrió que un subconjunto de adultos con diabetes tipo 1 tardó 4 veces más en promedio para acercarse a la cetoacidosis cuando se les administró somatostatina (inhibe la producción de glucagón) sin insulina. [ cita necesaria ] Inhibir el glucagón ha sido una idea popular en el tratamiento de la diabetes; sin embargo, algunos han advertido que hacerlo dará lugar a una diabetes frágil en pacientes con glucosa en sangre adecuadamente estable. [ cita necesaria ]
Se cree que la ausencia de células alfa (y por tanto de glucagón) es una de las principales influencias en la extrema volatilidad de la glucosa en sangre en el contexto de una pancreatectomía total .
A principios de la década de 1920, varios grupos notaron que los extractos pancreáticos inyectados en animales diabéticos darían como resultado un breve aumento del azúcar en sangre antes de la disminución del azúcar en sangre impulsada por la insulina. [6] En 1922, C. Kimball y John R. Murlin identificaron un componente de los extractos pancreáticos responsable de este aumento de azúcar en la sangre, denominándolo "glucagón", un acrónimo de " glucosa agonista ". [6] [33] En la década de 1950, los científicos de Eli Lilly aislaron glucagón puro, lo cristalizaron y determinaron su secuencia de aminoácidos. [6] [34] [35] Esto condujo al desarrollo del primer radioinmunoensayo para detectar glucagón, descrito por el grupo de Roger Unger en 1959. [6]
No se logró una comprensión más completa de su papel en la fisiología y la enfermedad hasta la década de 1970, cuando se desarrolló un radioinmunoensayo específico . [36]