El ferroceno es un compuesto organometálico con la fórmula Fe(C 5 H 5 ) 2 . La molécula es un complejo que consta de dos anillos de ciclopentadienilo intercalados con un átomo de hierro central . Es un sólido de color naranja con un olor parecido al alcanfor que se sublima por encima de la temperatura ambiente y es soluble en la mayoría de los disolventes orgánicos. Destaca por su estabilidad: no se ve afectado por el aire, el agua ni las bases fuertes y puede calentarse hasta 400 °C sin descomponerse. En condiciones oxidantes puede reaccionar reversiblemente con ácidos fuertes para formar el catión ferrocenio Fe(C 5 H 5 ).+2. [7] El ferroceno y el catión ferrocenio a veces se abrevian como Fc y Fc + respectivamente.
La primera síntesis de ferroceno de la que se tiene noticia fue en 1951. Su inusual estabilidad desconcertó a los químicos y requirió el desarrollo de una nueva teoría para explicar su formación y enlace. El descubrimiento del ferroceno y sus numerosos análogos , conocidos como metalocenos , generó entusiasmo y condujo a un rápido crecimiento en la disciplina de la química organometálica . Geoffrey Wilkinson y Ernst Otto Fischer , quienes trabajaron en el esclarecimiento de la estructura del ferroceno, compartieron más tarde el Premio Nobel de Química en 1973 por su trabajo sobre compuestos organometálicos tipo sándwich. El ferroceno en sí no tiene aplicaciones a gran escala, pero ha encontrado usos más especializados en catálisis, como aditivo para combustible y como herramienta en la educación universitaria.
El ferroceno fue descubierto por accidente dos veces. La primera síntesis conocida pudo haber sido realizada a finales de la década de 1940 por investigadores desconocidos de Union Carbide , que intentaron hacer pasar vapor caliente de ciclopentadieno a través de un tubo de hierro. El vapor reaccionó con la pared de la tubería, creando un "lodo amarillo" que obstruyó la tubería. Años más tarde, Eugene O. Brimm obtuvo y analizó una muestra del lodo que se había guardado, poco después de leer el artículo de Kealy y Pauson, y se descubrió que consistía en ferroceno. [7] [8]
La segunda vez fue alrededor de 1950, cuando Samuel A. Miller, John A. Tebboth y John F. Tremaine, investigadores de British Oxygen , intentaban sintetizar aminas a partir de hidrocarburos y nitrógeno en una modificación del proceso de Haber . Cuando intentaron hacer reaccionar ciclopentadieno con nitrógeno a 300 °C, a presión atmosférica, se decepcionaron al ver que el hidrocarburo reaccionaba con alguna fuente de hierro, produciendo ferroceno. Si bien ellos también observaron su notable estabilidad, dejaron la observación a un lado y no la publicaron hasta que Pauson informó sus hallazgos. [7] [9] [10] Kealy y Pauson recibieron más tarde una muestra de Miller et al. , quien confirmó que los productos eran el mismo compuesto. [8]
En 1951, Peter L. Pauson y Thomas J. Kealy de la Universidad de Duquesne intentaron preparar fuvaleno ( (C 5 H 4 ) 2 ) mediante dimerización oxidativa de ciclopentadieno ( C 5 H 6 ). Para ello, hicieron reaccionar el compuesto de Grignard, bromuro de ciclopentadienil magnesio en éter dietílico, con cloruro férrico como oxidante. [7] Sin embargo, en lugar del fulvaleno esperado, obtuvieron un polvo de color naranja claro de "notable estabilidad", con la fórmula C 10 H 10 Fe . [8] [11]

Pauson y Kealy conjeturaron que el compuesto tenía dos grupos ciclopentadienilo, cada uno con un único enlace covalente del átomo de carbono saturado al átomo de hierro. [7] Sin embargo, esa estructura era inconsistente con los modelos de enlace existentes en ese momento y no explicaba la estabilidad inesperada del compuesto, y los químicos lucharon por encontrar la estructura correcta. [10] [12]
La estructura fue deducida e informada de forma independiente por tres grupos en 1952. [13] Robert Burns Woodward y Geoffrey Wilkinson la dedujeron observando que el ferroceno experimentaba reacciones típicas de compuestos aromáticos como el benceno . [14] Ernst Otto Fischer y Wolfgang Pfab notaron que el compuesto era diamagnético y centrosimétrico, sintetizando también níqueloceno y cobaltoceno y confirmando que tenían la misma estructura. [15] Fischer describió la estructura como Doppelkegelstruktur ("estructura de doble cono"), aunque los químicos británicos y estadounidenses prefirieron el término "sándwich". [16] Philip Frank Eiland y Raymond Pepinsky confirmaron la estructura mediante cristalografía de rayos X y posteriormente mediante RMN . [10] [17] [18] [19]
La estructura "sándwich" del ferroceno era sorprendentemente novedosa y requería una nueva teoría para explicarla. Aplicación de la teoría de los orbitales moleculares con el supuesto de un centro Fe 2+ entre dos aniones ciclopentadienuro C 5 H−5dio como resultado el exitoso modelo de Dewar-Chatt-Duncanson , que permite la predicción correcta de la geometría de la molécula y explica su notable estabilidad. [20] [21]
El ferroceno no fue el primer compuesto organometálico descubierto. La sal de Zeise K[PtCl 3 (C 2 H 4 )]·H 2 O se informó en 1831, [22] [23] Edward Frankland sintetizó dietilzinc y otros compuestos similares en 1848, el descubrimiento de Mond de Ni(CO) 4 ocurrió en 1888 , [24] y los compuestos de organolitio se desarrollaron en la década de 1930. [25] Sin embargo, se puede argumentar que fue el descubrimiento del ferroceno el que inició la química organometálica como un área separada de la química. También provocó una explosión de interés en los compuestos de metales del bloque D con hidrocarburos. El descubrimiento fue considerado tan significativo que Wilkinson y Fischer compartieron el Premio Nobel de Química de 1973 "por su trabajo pionero, realizado de forma independiente, sobre la química de los compuestos organometálicos, llamados compuestos sándwich ". [26]
La espectroscopia de Mössbauer indica que al centro de hierro en el ferroceno se le debe asignar el estado de oxidación +2. A cada anillo de ciclopentadienilo (Cp) se le debe asignar una única carga negativa. Por tanto, el ferroceno podría describirse como bis ( ciclopentadienuro ) de hierro (II), Fe 2+ [C 5 H−5] 2 .
Cada anillo tiene seis electrones π, lo que los hace aromáticos según la regla de Hückel . Estos electrones π luego se comparten con el metal mediante enlaces covalentes. Dado que el Fe 2+ tiene seis electrones d , el complejo alcanza una configuración de 18 electrones , lo que explica su estabilidad. En notación moderna, este modelo estructural tipo sándwich de la molécula de ferroceno se denota como Fe( η 5 -C 5 H 5 ) 2 , donde η denota hapticidad , el número de átomos a través de los cuales se une cada anillo.
Las distancias de los enlaces carbono-carbono alrededor de cada anillo de cinco miembros son todas de 1,40 Å, y todas las distancias de los enlaces Fe-C son de 2,04 Å. Desde temperatura ambiente hasta 164 K, la cristalografía de rayos X produce el grupo espacial monoclínico; los anillos de ciclopentadienuro tienen una conformación escalonada, lo que da como resultado una molécula centrosimétrica, con grupo de simetría D 5d . [17] Sin embargo, por debajo de 110 K, el ferroceno cristaliza en una red cristalina ortorrómbica en la que los anillos Cp están ordenados y eclipsados, de modo que la molécula tiene un grupo de simetría D 5h . [27] En la fase gaseosa, la difracción de electrones [28] y los estudios computacionales [29] muestran que los anillos de Cp están eclipsados. Mientras que el ferroceno no tiene momento dipolar permanente a temperatura ambiente, entre 172,8 y 163,5 K la molécula exhibe una "modulación inconmensurable", rompiendo la simetría D 5 y adquiriendo un dipolo eléctrico. [30]
Los anillos de Cp giran con una barrera baja alrededor del eje Cp (centroide) –Fe-Cp (centroide) , como se observa mediante mediciones en derivados sustituidos de ferroceno utilizando espectroscopia de resonancia magnética nuclear de 1 H y 13 C. Por ejemplo, el metilferroceno (CH 3 C 5 H 4 FeC 5 H 5 ) presenta un singlete para el anillo C 5 H 5 . [31]
En solución, y a temperatura ambiente, se determinó que el ferroceno D 5h eclipsado dominaba sobre el confórmero D 5d escalonado , como lo sugieren tanto la espectroscopía infrarroja por transformada de Fourier como los cálculos de DFT . [32]
Industrialmente, el ferroceno se sintetiza mediante la reacción de etóxido de hierro (II) con ciclopentadieno; [33] el etóxido de hierro (II) necesario se produce mediante la oxidación electroquímica del hierro metálico en etanol anhidro . Dado que la reacción entre el etóxido de hierro (II) y el ciclopentadieno produce etanol como subproducto, el etanol sirve efectivamente como catalizador para la reacción general, siendo la reacción neta Fe + 2C 5 H 6 → H 2 + Fe(C 5 H 5 ) 2 (ver también más abajo)
Las primeras síntesis de ferroceno de las que se informó fueron casi simultáneas. Pauson y Kealy sintetizaron ferroceno utilizando cloruro de hierro (III) y un reactivo de Grignard, bromuro de ciclopentadienil magnesio. Se suspende cloruro de hierro (III) en éter dietílico anhidro y se añade al reactivo de Grignard. [11] Se produce una reacción redox , que forma el radical ciclopentadienilo y los iones hierro (II). El dihidrofulvaleno se produce mediante recombinación radical-radical mientras que el hierro (II) reacciona con el reactivo de Grignard para formar ferroceno. La oxidación de dihidrofulvaleno a fulvaleno con hierro (III), el resultado buscado por Kealy y Pauson, no ocurre. [8]

La otra síntesis temprana del ferroceno fue la de Miller et al. , [9] quienes hicieron reaccionar hierro metálico directamente con ciclopentadieno en fase gaseosa a temperatura elevada. [34] También se informó sobre un enfoque que utiliza hierro pentacarbonilo . [35]
Los métodos preparativos más eficientes son generalmente una modificación de la secuencia de transmetalación original utilizando ciclopentadienuro de sodio disponible comercialmente [36] o ciclopentadieno recién craqueado desprotonado con hidróxido de potasio [37] y hecho reaccionar con cloruro de hierro (II) anhidro en solventes etéreos.
Se conocen modificaciones modernas del enfoque original de Grignard de Pauson y Kealy:
Incluso algunas bases amínicas (como la dietilamina ) se pueden utilizar para la desprotonación, aunque la reacción avanza más lentamente que cuando se utilizan bases más fuertes: [36]
La transmetalación directa también se puede utilizar para preparar ferroceno a partir de otros metalocenos, como el manganoceno : [38]

El ferroceno es un sólido anaranjado estable al aire con olor a alcanfor. Como se esperaba de una especie simétrica y sin carga, el ferroceno es soluble en disolventes orgánicos normales, como el benceno, pero es insoluble en agua. Es estable a temperaturas de hasta 400 °C. [39]
El ferroceno se sublima fácilmente , especialmente al calentarlo al vacío. Su presión de vapor es de aproximadamente 1 Pa a 25 °C, 10 Pa a 50 °C, 100 Pa a 80 °C, 1000 Pa a 116 °C y 10 000 Pa (casi 0,1 atm ) a 162 °C. [40] [41]
El ferroceno sufre muchas reacciones características de los compuestos aromáticos, lo que permite la preparación de derivados sustituidos. Un experimento común de pregrado es la reacción de Friedel-Crafts de ferroceno con anhídrido acético (o cloruro de acetilo ) en presencia de ácido fosfórico como catalizador. En condiciones de reacción de Mannich , el ferroceno da N,N-dimetilaminometilferroceno .
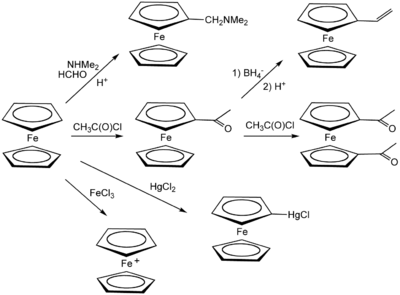
El propio ferroceno se puede utilizar como columna vertebral de un ligando, por ejemplo, 1,1'-bis(difenilfosfino)ferroceno (dppf). El propio ferroceno puede oxidarse al catión ferrocenio (Fc + ); El par ferroceno/ferrocenio se utiliza a menudo como referencia en electroquímica. [12]
Es una sustancia aromática y sufre reacciones de sustitución en lugar de reacciones de adición en los ligandos de ciclopentadienilo. Por ejemplo, la acilación de Friedel-Crafts de ferroceno con anhídrido acético produce acetilferroceno [42] al igual que la acilación de benceno produce acetofenona en condiciones similares.
La protonación del ferroceno permite el aislamiento de [Cp 2 FeH]PF 6 . [43]
En presencia de cloruro de aluminio , Me 2 NPCl 2 y ferroceno reaccionan para dar ferrocenil diclorofosfina, [44] mientras que el tratamiento con fenildiclorofosfina en condiciones similares forma P , P -diferrocenil - P -fenilfosfina. [45]
El ferroceno reacciona con P 4 S 10 forma un disulfuro de diferrocenil-ditiadifosfetano. [46]
El ferroceno reacciona con butillitio para dar 1,1′-dilitioferroceno , que es un nucleófilo versátil . En combinación con butillitio, el terc -butillitio produce monolitioferroceno. [47]
El ferroceno sufre una oxidación de un electrón a alrededor de 0,4 V frente a un electrodo de calomelanos saturado (SCE), convirtiéndose en ferrocenio . Esta oxidación reversible se ha utilizado como estándar en electroquímica como Fc + /Fc = 0,64 V frente al electrodo de hidrógeno estándar , [48] sin embargo, se han informado otros valores. [49] El tetrafluoroborato de ferrocenio es un reactivo común. [50] El comportamiento de oxidación-reducción notablemente reversible se ha utilizado ampliamente para controlar procesos de transferencia de electrones en sistemas electroquímicos [51] [52] y fotoquímicos [53] [54] .
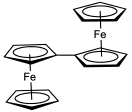
Los sustituyentes en los ligandos de ciclopentadienilo alteran el potencial redox de la manera esperada: los grupos aceptores de electrones, como el ácido carboxílico, desplazan el potencial en la dirección anódica ( es decir, se vuelven más positivos), mientras que los grupos liberadores de electrones, como los grupos metilo , desplazan el potencial en la dirección anódica. la dirección catódica (más negativa). Por lo tanto, el decametilferroceno se oxida mucho más fácilmente que el ferroceno e incluso puede oxidarse al correspondiente dicado. [55] El ferroceno se utiliza a menudo como estándar interno para calibrar potenciales redox en electroquímica no acuosa .
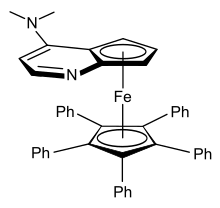
Los ferrocenos disustituidos pueden existir como isómeros 1,2, 1,3 o 1,1', ninguno de los cuales es interconvertible. Los ferrocenos que están disustituidos asimétricamente en un anillo son quirales, por ejemplo [CpFe(EtC 5 H 3 Me)]. Esta quiralidad plana surge a pesar de que ningún átomo es un centro estereogénico . Se ha demostrado que el ferroceno sustituido que se muestra a la derecha (un derivado de 4-(dimetilamino)piridina) es eficaz cuando se utiliza para la resolución cinética de alcoholes secundarios racémicos . [56] Se han desarrollado varios enfoques para funcionalizar asimétricamente el ferroceno en 1,1′. [57]
El ferroceno y sus numerosos derivados no tienen aplicaciones a gran escala, pero tienen muchos usos especializados que explotan su estructura inusual ( estructuras de ligandos , candidatos farmacéuticos ), robustez ( formulaciones antidetonantes , precursores de materiales) y redox (reactivos y estándares redox). .
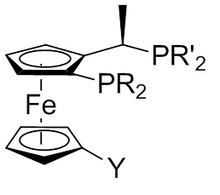
Las ferrocenilfosfinas quirales se emplean como ligandos para reacciones catalizadas por metales de transición. Algunos de ellos han encontrado aplicaciones industriales en la síntesis de productos farmacéuticos y agroquímicos. Por ejemplo, la difosfina 1,1′-bis(difenilfosfino)ferroceno (dppf) es un ligando valioso para reacciones de acoplamiento de paladio y el ligando de Josiphos es útil para la catálisis de hidrogenación. [58] Llevan el nombre del técnico que realizó el primero, Josi Puleo. [59] [60]
El ferroceno y sus derivados son agentes antidetonantes utilizados en el combustible de los motores de gasolina . Son más seguros que el tetraetilo de plomo utilizado anteriormente . [61] Se pueden añadir soluciones de aditivos de gasolina que contienen ferroceno a la gasolina sin plomo para permitir su uso en coches antiguos diseñados para funcionar con gasolina con plomo. [62] Los depósitos que contienen hierro formados a partir del ferroceno pueden formar una capa conductora en las superficies de las bujías . Los copolímeros de poliglicol de ferroceno, preparados mediante una reacción de policondensación entre un derivado de ferroceno y un alcohol dihidroxi sustituido, son prometedores como componente de los propulsores de cohetes. Estos copolímeros proporcionan a los propulsores de cohetes estabilidad térmica, sirviendo como aglutinante del propulsor y controlando la velocidad de combustión del propulsor. [63]
Se ha descubierto que el ferroceno es eficaz para reducir el humo y el trióxido de azufre que se producen al quemar carbón. La adición por cualquier medio práctico, impregnando el carbón o añadiendo ferroceno a la cámara de combustión, puede reducir significativamente la cantidad de estos subproductos indeseables, incluso con una pequeña cantidad del compuesto de ciclopentadienilo metálico. [64]
Los derivados del ferroceno se han investigado como fármacos, [65] y en la década de 1970 se aprobó un compuesto de ferrocerona para su uso en la URSS, aunque ya no se comercializa en la actualidad. [66] Sólo un fármaco ha entrado en ensayos clínicos en los últimos años, la ferroquina (7-cloro-N-(2-((dimetilamino)metil)ferrocenil)quinolin-4-amina), un antipalúdico , [67] [68] [ 69] que ha alcanzado los ensayos de Fase IIb. [70] Se han investigado sistemas de administración de fármacos basados en polímeros que contienen ferroceno. [71]

La actividad anticancerígena de los derivados del ferroceno se investigó por primera vez a finales de la década de 1970, cuando se probaron derivados que portaban grupos amina o amida contra la leucemia linfocítica . [72] Algunas sales de ferrocenio exhiben actividad anticancerígena, pero ningún compuesto ha sido evaluado en la clínica. [73] Los derivados del ferroceno tienen una fuerte actividad inhibidora contra la línea celular de cáncer de pulmón humano A549, la línea celular de cáncer colorrectal HCT116 y la línea celular de cáncer de mama MCF-7. [74] Se informó sobre un fármaco experimental que es una versión ferrocenil del tamoxifeno . [75] La idea es que el tamoxifeno se unirá a los sitios de unión de estrógeno , lo que provocará citotoxicidad. [75] [76]
Los ferrocifenos son explotados para aplicaciones contra el cáncer por una biotecnología francesa, Feroscan, fundada por el Pr. Gerard Jaouen.
El ferroceno y sus derivados se utilizan como potentes catalizadores de velocidad de combustión en propulsores compuestos de perclorato de amonio . [77]
Los análogos del ferroceno se pueden preparar con variantes de ciclopentadienilo. Por ejemplo, bis indeniliron y bisfluoreniliron. [60]

Los átomos de carbono pueden ser reemplazados por heteroátomos como lo ilustra Fe( η 5 -C 5 Me 5 )( η 5 -P 5 ) y Fe( η 5 -C 5 H 5 )( η 5 -C 4 H 4 N) (" azaferroceno"). El azaferroceno surge de la descarbonilación de Fe( η 5 -C 5 H 5 )(CO) 2 ( η 1 -pirrol) en ciclohexano . [78] Este compuesto, al hervir a reflujo en benceno, se convierte en ferroceno. [79]
Debido a la facilidad de sustitución, se han preparado muchos derivados de ferroceno estructuralmente inusuales. Por ejemplo, el ligando penta(ferrocenil)ciclopentadienilo [80] presenta un anión ciclopentadienilo derivatizado con cinco sustituyentes de ferroceno.


En el hexaferrocenilbenceno , C 6 [( η 5 -C 5 H 4 )Fe ( η 5 -C 5 H 5 )] 6 , las seis posiciones en una molécula de benceno tienen sustituyentes ferrocenilo ( R ). [81] El análisis de difracción de rayos X de este compuesto confirma que los ligandos de ciclopentadienilo no son coplanares con el núcleo de benceno, sino que tienen ángulos diédricos alternos de +30° y −80°. Debido al hacinamiento estérico, los ferrocenilos están ligeramente curvados con ángulos de 177° y tienen enlaces C-Fe alargados. Los átomos de carbono cuaternarios del ciclopentadienilo también están piramidalizados . Además, el núcleo de benceno tiene una conformación de silla con ángulos diédricos de 14° y muestra una alternancia de longitud de enlace entre 142,7 pm y 141,1 pm, ambas indicaciones de apiñamiento estérico de los sustituyentes.
Se ha informado sobre la síntesis de hexaferrocenilbenceno utilizando el acoplamiento Negishi de hexayodidobenceno y diferrocenilzinc, utilizando tris (dibencilidenacetona) dipaladio (0) como catalizador , en tetrahidrofurano : [81]
El rendimiento es sólo del 4%, lo que es una prueba más consistente con un apiñamiento estérico sustancial alrededor del núcleo areno.

El ferroceno, un precursor de las nanopartículas de hierro, puede utilizarse como catalizador para la producción de nanotubos de carbono. [83] El vinilferroceno se puede obtener mediante una reacción de Wittig del aldehído , una sal de fosfonio y hidróxido de sodio . [84] El vinilferroceno se puede convertir en un polímero (polivinilferroceno, PVFc), una versión ferrocenilo del poliestireno (los grupos fenilo se reemplazan por grupos ferrocenilo). Otro poliferroceno que puede formarse es poli(ferrocenocarboxilato de 2-(metacriloiloxi)etilo), PFcMA. Además de utilizar cadenas principales de polímeros orgánicos, estas unidades colgantes de ferroceno se han unido a cadenas principales inorgánicas como polisiloxanos , polifosfacenos y polifosfinoboranos (–PH(R)–BH 2 –) n , y los materiales resultantes exhiben propiedades físicas y electrónicas inusuales. relativo a la pareja redox ferroceno/ferrocinio. [82] Tanto el PVFc como el PFcMA se han unido a obleas de sílice y se ha medido la humectabilidad cuando las cadenas de polímero no están cargadas y cuando los restos de ferroceno se oxidan para producir grupos cargados positivamente. El ángulo de contacto con el agua en las obleas recubiertas de PFcMA fue 70° menor después de la oxidación, mientras que en el caso de PVFc la disminución fue de 30° y el cambio de la humectabilidad es reversible. En el caso de PFcMA, el efecto de alargar las cadenas y, por tanto, introducir más grupos ferroceno es una reducción significativamente mayor en el ángulo de contacto tras la oxidación. [82] [85]