Los modelos matemáticos pueden proyectar cómo progresan las enfermedades infecciosas para mostrar el resultado probable de una epidemia (incluso en las plantas ) y ayudar a informar las intervenciones de salud pública y sanidad vegetal. Los modelos utilizan suposiciones básicas o estadísticas recopiladas junto con matemáticas para encontrar parámetros para diversas enfermedades infecciosas y utilizan esos parámetros para calcular los efectos de diferentes intervenciones, como programas de vacunación masiva . El modelado puede ayudar a decidir qué intervención(es) evitar y cuál probar, o puede predecir patrones de crecimiento futuros, etc.
La modelización de enfermedades infecciosas es una herramienta que se ha utilizado para estudiar los mecanismos por los que se propagan las enfermedades, predecir el curso futuro de un brote y evaluar estrategias para controlar una epidemia. [1]
El primer científico que intentó cuantificar sistemáticamente las causas de muerte fue John Graunt en su libro Natural and Political Observations made upon the Bills of Mortality , en 1662. Los proyectos de ley que estudió eran listados de números y causas de muerte publicados semanalmente. El análisis de Graunt sobre las causas de muerte se considera el comienzo de la "teoría de los riesgos competitivos" que, según Daley y Gani [1], es "una teoría que ahora está bien establecida entre los epidemiólogos modernos".
El primer relato de modelización matemática de la propagación de enfermedades fue realizado en 1760 por Daniel Bernoulli . Bernoulli, de formación médica, creó un modelo matemático para defender la práctica de la inoculación contra la viruela . [2] Los cálculos de este modelo mostraron que la inoculación universal contra la viruela aumentaría la esperanza de vida de 26 años 7 meses a 29 años 9 meses. [3] El trabajo de Daniel Bernoulli precedió a la comprensión moderna de la teoría de los gérmenes . [4]
A principios del siglo XX, William Hamer [5] y Ronald Ross [6] aplicaron la ley de acción de masas para explicar el comportamiento epidémico.
En la década de 1920 surgieron los modelos compartimentales. El modelo epidémico de Kermack-McKendrick (1927) y el modelo epidémico de Reed-Frost (1928) describen la relación entre individuos susceptibles , infectados e inmunes en una población. El modelo epidémico de Kermack-McKendrick logró predecir el comportamiento de los brotes de manera muy similar al observado en muchas epidemias registradas. [7]
Recientemente, se han utilizado modelos basados en agentes (ABM) en lugar de modelos compartimentales más simples . [8] Por ejemplo, los ABM epidemiológicos se han utilizado para informar intervenciones de salud pública (no farmacéuticas) contra la propagación del SARS-CoV-2 . [9] Los ABM epidemiológicos, a pesar de su complejidad y de requerir un alto poder computacional, han sido criticados por supuestos simplificadores y poco realistas. [10] [11] Aún así, pueden ser útiles para informar decisiones sobre medidas de mitigación y supresión en los casos en que los ABM están calibrados con precisión. [12]
Los modelos son tan buenos como los supuestos en los que se basan. Si un modelo hace predicciones que no están en línea con los resultados observados y las matemáticas son correctas, los supuestos iniciales deben cambiar para que el modelo sea útil. [13]
"Estocástico" significa ser o tener una variable aleatoria. Un modelo estocástico es una herramienta para estimar distribuciones de probabilidad de resultados potenciales al permitir variaciones aleatorias en una o más entradas a lo largo del tiempo. Los modelos estocásticos dependen de las variaciones aleatorias en el riesgo de exposición, enfermedad y otras dinámicas de enfermedad. La diseminación estadística de la enfermedad a nivel de agente en poblaciones pequeñas o grandes se puede determinar mediante métodos estocásticos. [14] [15] [16]
Cuando se trata de poblaciones grandes, como en el caso de la tuberculosis, se suelen utilizar modelos matemáticos deterministas o compartimentales. En un modelo determinista, los individuos de la población se asignan a diferentes subgrupos o compartimentos, cada uno de los cuales representa una etapa específica de la epidemia. [17]
Las tasas de transición de una clase a otra se expresan matemáticamente como derivadas, por lo que el modelo se formula mediante ecuaciones diferenciales. Al construir tales modelos, se debe suponer que el tamaño de la población en un compartimento es diferenciable con respecto al tiempo y que el proceso epidémico es determinista. En otras palabras, los cambios en la población de un compartimento se pueden calcular utilizando únicamente la historia que se utilizó para desarrollar el modelo. [7]
Una explicación común para el crecimiento de las epidemias sostiene que 1 persona infecta a 2, esas 2 infectan a 4 y así sucesivamente, duplicándose el número de infectados en cada generación. Es análogo a un juego de etiqueta donde 1 persona etiqueta a 2, esas 2 etiquetan a otras 4 que nunca han sido etiquetadas y así sucesivamente. A medida que este juego avanza, se vuelve cada vez más frenético a medida que los etiquetados pasan corriendo junto a los previamente etiquetados para cazar a aquellos que nunca han sido etiquetados. Así, este modelo de epidemia conduce a una curva que crece exponencialmente hasta llegar a cero, ya que toda la población ha sido infectada. es decir, no hay inmunidad colectiva ni un pico y un declive gradual como se ve en la realidad. [18]
Las epidemias pueden modelarse como enfermedades que se propagan a través de redes de contacto entre personas. Una red de este tipo se puede representar matemáticamente mediante un gráfico y se denomina red de contactos. [19] Cada nodo en una red de contactos es una representación de un individuo y cada enlace (borde) entre un par de nodos representa el contacto entre ellos. Los vínculos en las redes de contactos pueden usarse para transmitir la enfermedad entre los individuos y cada enfermedad tiene su propia dinámica además de su red de contactos. La combinación de dinámicas de enfermedades bajo la influencia de intervenciones, si las hubiera, en una red de contactos puede modelarse con otra red, conocida como red de transmisión. En una red de transmisión, todos los eslabones son responsables de transmitir la enfermedad. Si dicha red es una red local similar a un árbol, lo que significa que cualquier vecindad local en dicha red toma la forma de un árbol , entonces la reproducción básica se puede escribir en términos del grado excesivo promedio de la red de transmisión de manera que:
donde es el grado medio (grado promedio) de la red y es el segundo momento de la distribución de grados de la red de transmisión . Sin embargo, no siempre es sencillo encontrar la red de transmisión a partir de la red de contactos y la dinámica de la enfermedad. [20] Por ejemplo, si una red de contactos se puede aproximar con un gráfico Erdős-Rényi con una distribución de grados Poissonianos , y los parámetros de propagación de enfermedades son como se definen en el ejemplo anterior, es decir, la tasa de transmisión por persona y la enfermedad ha un período infeccioso medio de , entonces el número de reproducción básico es [21] [22] ya que para una distribución de Poisson.
El número de reproducción básico (indicado por R 0 ) es una medida de cuán transferible es una enfermedad. Es el número promedio de personas que una sola persona infecciosa infectará durante el transcurso de su infección. Esta cantidad determina si la infección aumentará subexponencialmente , desaparecerá o permanecerá constante: si R 0 > 1, entonces cada persona infecta en promedio a más de una persona, por lo que la enfermedad se propagará; si R 0 < 1, entonces cada persona infecta a menos de una en promedio, por lo que la enfermedad desaparecerá; y si R 0 = 1, entonces cada persona infectará en promedio exactamente a otra persona, por lo que la enfermedad se volverá endémica: se moverá por toda la población pero no aumentará ni disminuirá. [23]
Se dice que una enfermedad infecciosa es endémica cuando puede mantenerse en una población sin necesidad de insumos externos. Esto significa que, en promedio, cada persona infectada está infectando exactamente a otra persona (más y el número de personas infectadas crecerá subexponencialmente y habrá una epidemia ; menos y la enfermedad desaparecerá). En términos matemáticos, eso es:
El número de reproducción básico ( R 0 ) de la enfermedad, suponiendo que todos sean susceptibles, multiplicado por la proporción de la población que es realmente susceptible ( S ) debe ser uno (ya que aquellos que no son susceptibles no figuran en nuestros cálculos porque no pueden contraer la enfermedad). Obsérvese que esta relación significa que para que una enfermedad se encuentre en el estado estacionario endémico , cuanto mayor sea el número de reproducción básico, menor debe ser la proporción de la población susceptible, y viceversa. Esta expresión tiene limitaciones en cuanto a la proporción de susceptibilidad, por ejemplo, R 0 es igual a 0,5 implica que S tiene que ser 2, sin embargo, esta proporción excede el tamaño de la población. [ cita necesaria ]
Supongamos la distribución de edades estacionaria rectangular y consideremos también que las edades de infección tienen la misma distribución para cada año de nacimiento. Sea A la edad promedio de infección , por ejemplo cuando los individuos más jóvenes que A son susceptibles y los mayores que A son inmunes (o infecciosos). Entonces se puede demostrar mediante un argumento sencillo que la proporción de la población que es susceptible viene dada por:
Reiteramos que L es la edad a la que en este modelo se supone que muere cada individuo. Pero la definición matemática del estado estacionario endémico se puede reordenar para dar:
Por tanto, debido a la propiedad transitiva :
Esto proporciona una forma sencilla de estimar el parámetro R 0 utilizando datos fácilmente disponibles.
Para una población con una distribución de edades exponencial ,
Esto permite calcular el número de reproducción básico de una enfermedad dados A y L en cualquier tipo de distribución poblacional.
Los modelos compartimentales se formulan como cadenas de Markov . [24] Un modelo compartimental clásico en epidemiología es el modelo SIR, que puede usarse como un modelo simple para modelar epidemias. También se emplean muchos otros tipos de modelos compartimentales.


En 1927, WO Kermack y AG McKendrick crearon un modelo en el que consideraban una población fija con sólo tres compartimentos: susceptible, ; infectado, ; y recuperado, . Los compartimentos utilizados para este modelo constan de tres clases: [25]
Hay muchas modificaciones del modelo SIR, incluidas aquellas que incluyen nacimientos y muertes, donde al recuperarse no hay inmunidad (modelo SIS), donde la inmunidad dura solo un corto período de tiempo (SIRS), donde hay un período latente de la enfermedad donde la persona no es infecciosa ( SEIS y SEIR ), y donde los bebés pueden nacer con inmunidad (MSIR). [ cita necesaria ]
Los modelos matemáticos deben integrar el creciente volumen de datos que se generan sobre las interacciones entre el huésped y el patógeno . Muchos estudios teóricos sobre la dinámica demográfica , la estructura y la evolución de las enfermedades infecciosas de plantas y animales, incluido el hombre, se ocupan de este problema. [26]
Los temas de investigación incluyen:
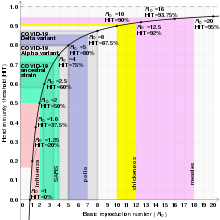
Si la proporción de la población que es inmune excede el nivel de inmunidad colectiva para la enfermedad, entonces la enfermedad ya no puede persistir en la población y su transmisión desaparece. [27] Por lo tanto, una enfermedad puede eliminarse de una población si suficientes individuos son inmunes debido a la vacunación o a la recuperación de una exposición previa a la enfermedad. Por ejemplo, la erradicación de la viruela , con el último caso salvaje en 1977, y la certificación de la erradicación de la transmisión autóctona de 2 de los 3 tipos de poliovirus salvaje (el tipo 2 en 2015, tras el último caso notificado en 1999, y el tipo 3 en 2019). , después del último caso reportado en 2012). [28]
El nivel de inmunidad colectiva se denominará q . Recuerde que, para un estado estable: [ cita necesaria ]
Sucesivamente,
que es aproximadamente: [ cita necesaria ]
S será (1 − q ), ya que q es la proporción de la población que es inmune y q + S debe ser igual a uno (ya que en este modelo simplificado, todos son susceptibles o inmunes). Entonces:
Recuerde que este es el nivel umbral. La desaparición de la transmisión sólo se producirá si la proporción de individuos inmunes supera este nivel debido a un programa de vacunación masiva.
Acabamos de calcular el umbral crítico de inmunización (denotado qc ) . Es la proporción mínima de la población que debe ser inmunizada al nacer (o cerca del nacimiento) para que la infección desaparezca en la población.
Porque la fracción del tamaño final de la población p que nunca se infecta se puede definir como:
Por eso,
Resolviendo para , obtenemos:
Si la vacuna utilizada no es suficientemente eficaz o no se puede alcanzar la cobertura requerida, es posible que el programa no supere q c . Un programa de este tipo protegerá a las personas vacunadas de las enfermedades, pero puede cambiar la dinámica de transmisión. [ cita necesaria ]
Supongamos que una proporción de la población q (donde q < q c ) está inmunizada al nacer contra una infección con R 0 > 1. El programa de vacunación cambia R 0 a R q donde
Este cambio se produce simplemente porque ahora hay menos personas susceptibles en la población que pueden infectarse. R q es simplemente R 0 menos aquellos que normalmente estarían infectados pero que no pueden estarlo ahora ya que son inmunes.
Como consecuencia de este número de reproducción básico más bajo , la edad promedio de infección A también cambiará a algún nuevo valor A q en aquellos que no han sido vacunados.
Recuerde la relación que unía R 0 , A y L . Suponiendo que la esperanza de vida no haya cambiado, ahora: [ cita necesaria ]
Pero R 0 = L / A entonces:
Por lo tanto, el programa de vacunación puede aumentar la edad promedio de infección y las personas no vacunadas experimentarán una fuerza de infección reducida debido a la presencia del grupo vacunado. En el caso de una enfermedad que provoca una mayor gravedad clínica en las poblaciones de mayor edad, la proporción de la población no vacunada puede experimentar la enfermedad relativamente más tarde en la vida de lo que ocurriría sin la vacuna.
Si un programa de vacunación hace que la proporción de individuos inmunes en una población supere el umbral crítico durante un período de tiempo significativo, se detendrá la transmisión de la enfermedad infecciosa en esa población. Si la eliminación se produce en todas partes al mismo tiempo, esto puede conducir a la erradicación . [ cita necesaria ]
Los modelos tienen la ventaja de examinar múltiples resultados simultáneamente, en lugar de hacer un único pronóstico. Los modelos han mostrado amplios grados de confiabilidad en pandemias pasadas, como el SARS , el SARS-CoV-2 , [29] la gripe porcina , el MERS y el Ébola . [30]
{{cite journal}}: Citar diario requiere |journal=( ayuda ){{cite book}}: Mantenimiento CS1: ubicación ( enlace )