El diborano (6) , comúnmente conocido como diborano , es el compuesto químico de fórmula B 2 H 6 . Es un gas altamente tóxico , incoloro y pirofórico con un olor repulsivamente dulce. Dada su sencilla fórmula, el borano es un compuesto de boro fundamental . Ha atraído gran atención por su estructura electrónica. Varios de sus derivados son reactivos útiles .
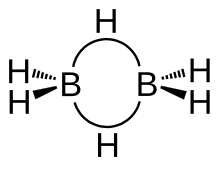
La estructura del diborano tiene simetría D 2h . Cuatro hidruros son terminales, mientras que dos forman puentes entre los centros de boro. Las longitudes de los enlaces puente B-H y de los enlaces terminales B-H son 1,33 y 1,19 Å respectivamente. Esta diferencia en las longitudes de los enlaces refleja la diferencia en sus resistencias, siendo los enlaces del puente B-H relativamente más débiles. La debilidad del puente B – H en comparación con los enlaces terminales B – H está indicada por sus firmas vibratorias en el espectro infrarrojo , siendo ≈2100 y 2500 cm −1 respectivamente. [7]
El modelo determinado por la teoría de los orbitales moleculares describe los enlaces entre el boro y los átomos terminales de hidrógeno como enlaces covalentes convencionales de 2 centros y 2 electrones . Sin embargo, el enlace entre los átomos de boro y los átomos de hidrógeno puente es diferente al de moléculas como los hidrocarburos. Cada boro utiliza dos electrones para unirse a los átomos de hidrógeno terminales y le queda un electrón de valencia para enlaces adicionales. Los átomos de hidrógeno puente proporcionan un electrón cada uno. El anillo B 2 H 2 se mantiene unido mediante cuatro electrones que forman dos enlaces de 2 electrones de 3 centros . Este tipo de bono a veces se denomina "bono banana".
B 2 H 6 es isoelectrónico con C 2 H 6 2+ , lo que surgiría de la diprotonación de la molécula plana etileno . [8] El diborano es uno de los muchos compuestos con enlaces tan inusuales. [9]
De los otros elementos del grupo IIIA , se sabe que el galio forma un compuesto similar digallano , Ga 2 H 6 . El aluminio forma un hidruro polimérico, (AlH 3 ) n ; aunque inestable, Al 2 H 6 se ha aislado en hidrógeno sólido y es isoestructural con diborano. [10]
Amplios estudios sobre el diborano han llevado al desarrollo de múltiples rutas de síntesis. La mayoría de las preparaciones implican reacciones de donantes de hidruros con haluros o alcóxidos de boro . La síntesis industrial de diborano implica la reducción de BF 3 mediante hidruro de sodio (NaH), hidruro de litio (LiH) o hidruro de litio y aluminio (LiAlH 4 ): [11]
El hidruro de litio utilizado para este fin debe estar pulverizado muy finamente para evitar la formación de una capa pasivante de tetrafluoroborato de litio sobre el reactivo. Alternativamente, se puede agregar una pequeña cantidad de producto diborano para formar borohidruro de litio , que descompondrá el fluoroborato y hará que la reacción sea autocatalítica . [12]
Dos métodos de laboratorio parten de tricloruro de boro con hidruro de litio y aluminio o de una solución de éter de trifluoruro de boro con borohidruro de sodio . Ambos métodos dan como resultado un rendimiento de hasta el 30%:
Cuando se calienta con NaBH 4 , el cloruro de estaño (II) se reduce a estaño elemental, formando diborano en el proceso:
Los métodos más antiguos implican la reacción directa de sales de borohidruro con un ácido no oxidante , como el ácido fosfórico o el ácido sulfúrico diluido .
De manera similar, se ha demostrado la oxidación de sales de borohidruro y sigue siendo conveniente para preparaciones a pequeña escala. Por ejemplo, usando yodo como oxidante: [13]
Otra síntesis a pequeña escala utiliza borohidruro de potasio y ácido fosfórico como materiales de partida. [14]

El diborano es un reactivo altamente reactivo y versátil. [dieciséis]
Como sustancia pirofórica , el diborano reacciona exotérmicamente con el oxígeno para formar trióxido de boro y agua:
El diborano reacciona violentamente con el agua para formar hidrógeno y ácido bórico :
El diborano también reacciona de manera similar con los alcoholes. El metanol, por ejemplo, proporciona hidrógeno y trimetilborato : [17]
Un patrón de reacción dominante implica la formación de aductos con bases de Lewis . A menudo, estos aductos iniciales proceden rápidamente para dar otros productos. Por ejemplo, el borano-tetrahidrofurano, que a menudo se comporta de manera equivalente al diborano, se degrada a ésteres de borato. Su aducto con sulfuro de dimetilo es un reactivo importante en la síntesis orgánica .
Con amoníaco, el diborano forma el diamoniato de diborano, DADB, con pequeñas cantidades de amoníaco borano como subproducto. La proporción depende de las condiciones.
En la reacción de hidroboración , el diborano también reacciona fácilmente con alquenos para formar trialquilboranos . Este patrón de reacción es bastante general y los boratos de alquilo resultantes pueden derivatizarse fácilmente, por ejemplo, a alcoholes. Aunque los primeros trabajos sobre hidroboración se basaron en diborano, este ha sido reemplazado por dimetilsulfuro de borano, que se maneja de manera más segura.
La pirólisis del diborano produce hidrógeno y diversos grupos de hidruro de boro. Por ejemplo, el pentaborano se preparó por primera vez mediante pirólisis de diborano a aproximadamente 200 °C. [18] [19] Aunque esta ruta de pirólisis rara vez se emplea, marcó el comienzo de un gran tema de investigación sobre la química de los racimos de borano.
El tratamiento del diborano con amalgama de sodio da NaBH 4 y Na[B 3 H 8 ] [17] Cuando el diborano se trata con hidruro de litio en éter dietílico , se forma borohidruro de litio: [17]
El diborano reacciona con cloruro de hidrógeno anhidro o bromuro de hidrógeno gaseoso para dar un halohidruro de boro: [17]
Al tratar diborano con monóxido de carbono a 470 K y 20 bar se obtiene H3BCO . [17]
El diborano y sus variantes son reactivos de síntesis orgánica centrales para la hidroboración . Los alquenos se añaden a través de los enlaces B-H para dar trialquilboranos, que pueden elaborarse más a fondo. [20] El diborano se utiliza como agente reductor aproximadamente complementario a la reactividad del hidruro de litio y aluminio . El compuesto reduce fácilmente los ácidos carboxílicos a los alcoholes correspondientes , mientras que las cetonas reaccionan sólo con lentitud.
El diborano se sintetizó por primera vez en el siglo XIX mediante hidrólisis de boruros metálicos, pero nunca fue analizado. De 1912 a 1936, Alfred Stock , el principal pionero en la química de los hidruros de boro, emprendió su investigación que condujo a los métodos para la síntesis y manipulación de los hidruros de boro altamente reactivos, volátiles y a menudo tóxicos. Propuso la primera estructura de diborano similar al etano . [21] Las mediciones de difracción de electrones realizadas por S. H. Bauer inicialmente parecieron respaldar su estructura propuesta. [22] [23]
Debido a una comunicación personal con L. Pauling (quien apoyó la estructura similar al etano), H. I. Schlessinger y A. B. Burg no discutieron específicamente el enlace de 3 centros y 2 electrones en su entonces clásica revisión a principios de la década de 1940. [24] Sin embargo, la revisión analiza con cierta profundidad la estructura puenteada del D 2h : "Se debe reconocer que esta formulación explica fácilmente muchas de las propiedades químicas del diborano..."
En 1943, H. Christopher Longuet-Higgins , siendo todavía estudiante en Oxford, fue el primero en explicar la estructura y el enlace de los hidruros de boro. El artículo que informa sobre el trabajo, escrito con su tutor R. P. Bell , [25] también revisa la historia del tema comenzando con el trabajo de Dilthey. [26] Poco después, el trabajo teórico de Longuet-Higgins fue confirmado en un estudio infrarrojo del diborano realizado por Price. [27] La estructura fue reconfirmada mediante medición de difracción de electrones en 1951 por K. Hedberg y V. Schomaker, con la confirmación de la estructura que se muestra en los esquemas de esta página. [28]
William Nunn Lipscomb Jr. confirmó además la estructura molecular de los boranos mediante cristalografía de rayos X en la década de 1950 y desarrolló teorías para explicar su enlace. Posteriormente, aplicó los mismos métodos a problemas relacionados, incluida la estructura de los carboranos, sobre los que dirigió la investigación del futuro premio Nobel de 1981 , Roald Hoffmann . El Premio Nobel de Química de 1976 fue otorgado a Lipscomb "por sus estudios sobre la estructura de los boranos, que iluminan los problemas de los enlaces químicos". [29]
Tradicionalmente, el diborano se ha descrito a menudo como deficiente en electrones , porque los 12 electrones de valencia sólo pueden formar 6 enlaces convencionales de 2 centros y 2 electrones, que son insuficientes para unir los 8 átomos. [30] [31] Sin embargo, la descripción más correcta que utiliza enlaces de 3 centros muestra que el diborano es realmente preciso en electrones, ya que hay suficientes electrones de valencia para llenar los 6 orbitales moleculares de enlace . [32] Sin embargo, algunos libros de texto importantes todavía utilizan el término "deficiente en electrones". [33]
Debido a la exotermia de su reacción con el oxígeno, el diborano ha sido probado como propulsor de cohetes . [34] La combustión completa es fuertemente exotérmica. Sin embargo, la combustión no es completa en el motor del cohete, ya que se produce algo de monóxido de boro , B 2 O. Esta conversión refleja la combustión incompleta de hidrocarburos para producir monóxido de carbono (CO). El diborano también resultó difícil de manejar. [35] [36] [37]
El diborano ha sido investigado como precursor de películas de boruro metálico [38] y para el dopaje p de semiconductores de silicio. [39]
El diborano es un gas pirofórico. En su lugar, normalmente se utilizan aductos disponibles comercialmente , al menos para aplicaciones en química orgánica. Estos aductos incluyen borano-tetrahidrofurano (borano-THF) y borano-dimetilsulfuro . [16] Los efectos tóxicos del diborano se mitigan porque el compuesto es muy inestable en el aire. Se ha investigado la toxicidad en ratas de laboratorio. [40]
{{cite book}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )Una de las consecuencias simples de estos estudios fue que las moléculas con deficiencia de electrones, definidas como aquellas que tienen más orbitales de valencia que electrones, no son realmente deficientes en electrones.
Una especie con deficiencia de electrones posee menos electrones de valencia de los necesarios para un esquema de enlace localizado.
{{cite web}}: Mantenimiento CS1: ubicación ( enlace )