
Un anestésico general (o anestésico ) es un fármaco que produce una pérdida reversible de la conciencia . [2] Estos fármacos generalmente son administrados por un anestesista/ anestesiólogo para inducir o mantener la anestesia general para facilitar la cirugía .
Los anestésicos generales se han utilizado ampliamente en cirugía desde 1842, cuando Crawford Long administró por primera vez éter dietílico a un paciente y realizó una operación indolora. Durante mucho tiempo se ha creído que los anestésicos generales ejercen sus efectos (analgesia, inconsciencia, inmovilidad) [3] a través de un mecanismo mediado por membrana o modulando directamente la actividad de las proteínas de membrana en la membrana neuronal. En general, los diferentes anestésicos exhiben diferentes mecanismos de acción, de modo que existen numerosos objetivos moleculares no excluyentes en todos los niveles de integración dentro del sistema nervioso central . [4] Sin embargo, para ciertos anestésicos intravenosos, como el propofol y el etomidato , se cree que el principal objetivo molecular es el receptor GABA A , con subunidades β particulares que juegan un papel crucial. [5] [6] [7]
El concepto de interacciones específicas entre receptores y fármacos, introducido por primera vez por Paul Ehrlich en 1897 [8], establece que los fármacos actúan únicamente cuando están unidos a sus dianas (receptores). [1] La identificación de dianas moleculares concretas para los anestésicos generales fue posible únicamente gracias al desarrollo moderno de técnicas de biología molecular para mutaciones de aminoácidos individuales en proteínas de ratones modificados genéticamente . [1] [5] [6] [7]

En 1847, Emil Harless y Ernst von Bibra propusieron por primera vez un mecanismo inespecífico de acción de los anestésicos generales. [9] Sugirieron que los anestésicos generales pueden actuar disolviéndose en la fracción grasa de las células cerebrales y eliminando los componentes grasos de ellas, modificando así la actividad de las células cerebrales e induciendo la anestesia. En 1899, Hans Horst Meyer publicó la primera evidencia experimental de que la potencia anestésica está relacionada con la solubilidad en lípidos. [10] [11] Dos años después, Charles Ernest Overton publicó de forma independiente una teoría similar . [12]
Meyer comparó la potencia de muchos agentes, definida como el recíproco de la concentración molar requerida para inducir la anestesia en renacuajos, con su coeficiente de partición aceite de oliva/agua . Encontró una relación casi lineal entre la potencia y el coeficiente de partición para muchos tipos de moléculas anestésicas como alcoholes , aldehídos , cetonas , éteres y ésteres . La concentración de anestésico requerida para inducir la anestesia en el 50% de una población de animales (CE50 ) era independiente del medio por el cual se administraba el anestésico, es decir, la fase gaseosa o acuosa. [10] [11] [13]
Meyer y Overton habían descubierto la sorprendente correlación entre las propiedades físicas de las moléculas de los anestésicos generales y su potencia: cuanto mayor es la solubilidad lipídica de un compuesto en aceite de oliva, mayor es su potencia anestésica. [13] Esta correlación es válida para una amplia gama de anestésicos con solubilidades lipídicas que oscilan entre 4 y 5 órdenes de magnitud si se utiliza aceite de oliva como fase oleosa. Esta correlación se puede mejorar considerablemente en términos tanto de la calidad de la correlación como de la mayor variedad de anestésicos si se utiliza octanol en masa [14] o una bicapa lipídica líquida completamente hidratada [15] [16] [17] [18] como fase "oleosa". También se observó que los anestésicos volátiles tienen efectos aditivos. (Una mezcla de media dosis de dos anestésicos volátiles diferentes produjo el mismo efecto anestésico que una dosis completa de cualquiera de los fármacos solos).
El sitio de anestésicos mejor caracterizado que explica la correlación de Meyer-Overton reside en los dominios lipídicos ordenados. Los anestésicos se adhieren de manera no específica a la superficie de un sitio de unión específico de palmitato dentro de la membrana lipídica, desplazando el palmitato de los lípidos GM1 ordenados. El proceso da lugar a un componente de anestesia mediada por membrana . [19] Se demostró un mecanismo similar para la luciferasa. [20] Los anestésicos se unieron de manera no específica a una superficie hidrófoba y superaron la unión específica de la luciferina. Sin embargo, la luciferasa no es fisiológicamente relevante para los vertebrados, ya que no se expresa endógenamente en ellos.

A partir de la correlación entre la solubilidad lipídica y la potencia anestésica, Meyer y Overton habían supuesto un mecanismo unitario de la anestesia general. Supusieron que la solubilización del anestésico general lipófilo en la bicapa lipídica de la neurona provoca su mal funcionamiento y el efecto anestésico cuando se alcanza la concentración crítica de anestésico. Más tarde, en 1973, Miller y Smith sugirieron la hipótesis del volumen crítico, también llamada hipótesis de expansión de la bicapa lipídica. [21] Supusieron que las moléculas anestésicas voluminosas e hidrófobas se acumulan dentro de las regiones hidrófobas (o lipófilas) de la membrana lipídica neuronal, lo que provoca su distorsión y expansión (engrosamiento) debido al desplazamiento de volumen. La acumulación de cantidades críticas de anestésico provoca un engrosamiento de la membrana suficiente para alterar reversiblemente la función de los canales iónicos de la membrana, proporcionando así un efecto anestésico. La estructura química real del agente anestésico en sí no es importante, pero su volumen molecular desempeña el papel principal: cuanto más espacio dentro de la membrana esté ocupado por el anestésico, mayor será el efecto anestésico. Basándose en esta teoría, en 1954 Mullins sugirió que la correlación de Meyer-Overton con la potencia se puede mejorar si se tienen en cuenta los volúmenes moleculares de las moléculas anestésicas. [22] Esta teoría existió durante más de 60 años y fue apoyada por el hecho experimental de que los aumentos en la presión atmosférica revierten el efecto anestésico ( efecto de inversión de presión ). [21] [23] [24]
Luego surgieron otras teorías fisicoquímicas de la acción anestésica que tenían en cuenta la diversa naturaleza química de los anestésicos generales y sugerían que el efecto anestésico se ejerce a través de alguna perturbación de la bicapa lipídica. [25] Se propusieron varios tipos de perturbaciones de la bicapa para causar un efecto anestésico, incluidos (1) cambios en la separación de fases, (2) cambios en el espesor de la bicapa, (3) cambios en los parámetros de orden o (4) cambios en la elasticidad de la curvatura. [26] [27] [28]
Según la teoría de la separación de fases lateral [28], los anestésicos ejercen su acción fluidizando las membranas nerviosas hasta un punto en el que desaparecen las separaciones de fases en las regiones lipídicas críticas. Esta fluidización inducida por los anestésicos hace que las membranas sean menos capaces de facilitar los cambios conformacionales en las proteínas que pueden ser la base de eventos de membrana como la activación de la compuerta iónica, la liberación del transmisor sináptico y la unión del transmisor a los receptores. Las técnicas más recientes con imágenes de súper resolución muestran que los anestésicos no superan la separación de fases; la separación de fases persiste. Más bien, los lípidos saturados dentro de la separación de fases pueden experimentar una transición de ordenados a desordenados que se ve afectada dramáticamente por los anestésicos. No obstante, ahora se ha demostrado que el concepto de proteínas que se mueven entre lípidos separados en fases en respuesta a los anestésicos es correcto. [29]
En general, se pensaba que todas estas primeras teorías sobre los lípidos adolecían de cuatro debilidades [1] (la descripción completa con refutaciones se encuentra en las secciones siguientes):
Se pensaba que la correlación entre la solubilidad lipídica y la potencia de los anestésicos generales era una condición necesaria pero no suficiente para inferir un sitio diana lipídica. Los anestésicos generales también podrían unirse a sitios diana hidrófobos en las proteínas del cerebro, pero dada la diversidad química de los anestésicos, esto probablemente necesitaría incluir más de un sitio y esos sitios no excluirían inherentemente un sitio en la membrana. En el caso de las proteínas, una razón por la que los anestésicos generales más polares podrían ser menos potentes es que tienen que cruzar la barrera hematoencefálica para ejercer su efecto sobre las neuronas del cerebro.

Existen dos hipótesis modernas sobre los lípidos que no excluyen la unión directa a proteínas. La hipótesis más reciente postula que los lípidos ordenados en la membrana plasmática contienen un sitio de unión estructurado para el palmitato lipídico . Se trata de un sitio de unión lipídica dentro de una estructura lipídica, no de una estructura proteica. Las proteínas que contienen un palmitato unido covalentemente ( palmitoilación ) se dirigen a los lípidos ordenados a través de una interacción lípido-lípido específica. La unión del palmitato al dominio lipídico depende del colesterol y la célula regula la proteína mediante localización nanoscópica.
Los anestésicos actúan uniéndose de forma no específica al sitio de unión del palmitato, lo que altera la capacidad del colesterol de unirse a la proteína y secuestrarla hasta dejarla en un estado inactivo. Pavel y sus colegas demostraron experimentalmente este mecanismo mediado por la membrana en 2020. Demostraron que la enzima fosfolipasa D2 (PLD2) es sensible a los anestésicos y activa el canal de potasio TREK-1 a través de un mecanismo mediado por la membrana . Los anestésicos desplazaron a la PLD2 de los dominios lipídicos ordenados, lo que permitió que la enzima se activara mediante la presentación del sustrato y activara el canal. [29] [30]
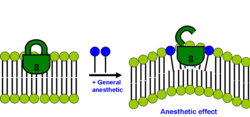
La segunda hipótesis lipídica establece que el efecto anestésico ocurre si la solubilización del anestésico general en la bicapa provoca una redistribución de las presiones laterales de la membrana. [31] [32]
Cada membrana bicapa tiene un perfil distinto de distribución de las presiones laterales en su interior. La mayoría de las proteínas de membrana (especialmente los canales iónicos) son sensibles a los cambios en este perfil de distribución de la presión lateral. Estas tensiones laterales son bastante grandes y varían con la profundidad dentro de la membrana. Según la hipótesis moderna de los lípidos, un cambio en el perfil de presión lateral de la membrana modifica el equilibrio conformacional de ciertas proteínas de membrana que se sabe que se ven afectadas por las concentraciones clínicas de anestésicos, como los canales iónicos regulados por ligando. Este mecanismo también es inespecífico porque la potencia del anestésico no está determinada por su estructura química real, sino por la distribución posicional y orientacional de sus segmentos y enlaces dentro de la bicapa.
En 1997, Cantor sugirió un mecanismo detallado de la anestesia general basado en la termodinámica estadística reticular. [32] Se propuso que la incorporación de solutos anfifílicos y otros solutos activos en la interfaz (por ejemplo, anestésicos generales) en la bicapa aumenta la presión lateral de forma selectiva cerca de las interfaces acuosas, lo que se compensa con una disminución de la presión lateral hacia el centro de la bicapa. Los cálculos mostraron que la anestesia general probablemente implica la inhibición de la apertura del canal iónico en una proteína de membrana dependiente de ligando postsináptico [32] mediante el siguiente mecanismo:
Esta es la primera hipótesis que proporcionó no sólo correlaciones de potencia con propiedades estructurales o termodinámicas, sino una comprensión mecanicista y termodinámica detallada de la anestesia.

Así, según la hipótesis moderna de los lípidos, los anestésicos no actúan directamente sobre sus proteínas de membrana diana, sino que más bien perturban matrices lipídicas especializadas en la interfaz proteína-lípido, que actúan como mediadores. Se trata de un nuevo tipo de mecanismo de transducción, diferente de la interacción llave-cerradura habitual entre ligando y receptor, en la que el anestésico (ligando) afecta a la función de las proteínas de membrana uniéndose al sitio específico de la proteína. Por ello, se propone que algunas proteínas de membrana son sensibles a su entorno lipídico.
En el mismo año se propuso un mecanismo molecular ligeramente diferente y detallado de cómo la perturbación de la bicapa puede influir en el canal iónico. La oleamida (amida de ácido graso del ácido oleico) es un anestésico endógeno que se encuentra in vivo (en el cerebro del gato) y se sabe que potencia el sueño y reduce la temperatura del cuerpo al cerrar la conexión del canal de unión en hendidura. [33] El mecanismo detallado se muestra en la imagen: el anillo de lípidos (verde)/colesterol (amarillo) bien ordenado que existe alrededor del conexón (magenta) se desordena durante el tratamiento con anestésico (triángulos rojos), lo que promueve el cierre del canal iónico del conexón. Esto disminuye la actividad cerebral e induce letargo y efecto anestésico.
Recientemente, las imágenes de súper resolución mostraron evidencia experimental directa de que los anestésicos volátiles alteran los dominios lipídicos ordenados como se predijo. [34] En el mismo estudio, surgió un mecanismo relacionado en el que los anestésicos liberaron la enzima fosfolipasa D (PLD) de los dominios lipídicos y la enzima se unió a los canales TREK-1 y los activó mediante la producción de ácido fosfatídico. Estos resultados mostraron experimentalmente que la membrana es un objetivo fisiológicamente relevante de los anestésicos generales.

A principios de los años 1980, Nicholas P. Franks y William R. Lieb [35] demostraron que la correlación Meyer-Overton se puede reproducir utilizando una proteína soluble. Encontraron que dos clases de proteínas se inactivan mediante dosis clínicas de anestésico en ausencia total de lípidos. Estas son las luciferasas , que son utilizadas por animales y bacterias bioluminiscentes para producir luz, [36] y el citocromo P450 [37] , que es un grupo de proteínas hemo que hidroxilan un grupo diverso de compuestos, incluidos los ácidos grasos , los esteroides y los xenobióticos como el fenobarbital . Sorprendentemente, la inhibición de estas proteínas por anestésicos generales se correlacionó directamente con sus potencias anestésicas. La inhibición de la luciferasa también exhibe un corte de alcohol de cadena larga, que está relacionado con el tamaño del bolsillo de unión del anestésico. [38]
Estas observaciones fueron importantes porque demostraron que los anestésicos generales ejercen su efecto de manera no específica, incluso cuando se unen a las proteínas. Esto también abrió la posibilidad de que los anestésicos pudieran funcionar mediante la unión directa a las proteínas, en lugar de afectar a las proteínas de membrana indirectamente a través de interacciones no específicas con la bicapa lipídica como mediador. [14] [39] Se demostró que los anestésicos alteran las funciones de muchas proteínas de señalización citoplasmática, incluida la proteína quinasa C. [ 40] [41]
Sin embargo, las proteínas consideradas los objetivos moleculares más probables de los anestésicos son los canales iónicos. Según esta teoría, los anestésicos generales son mucho más selectivos que en las hipótesis lipídicas, y se unen directamente solo a un pequeño número de objetivos en el sistema nervioso central, principalmente canales iónicos controlados por ligando en sinapsis y receptores acoplados a proteína G , alterando su flujo iónico. En particular, los receptores Cys-loop [42] son objetivos plausibles para los anestésicos generales que se unen en la interfaz entre las subunidades. La superfamilia de receptores Cys-loop incluye receptores inhibidores ( receptores GABA A , receptores GABA C , receptores de glicina ) y receptores excitadores ( receptor nicotínico de acetilcolina y receptor de serotonina 5-HT3 ). Los anestésicos generales pueden inhibir las funciones del canal de los receptores excitadores o potenciar las funciones de los receptores inhibidores, respectivamente.
La ubicación de los sitios de unión no específicos en los canales iónicos sigue siendo una cuestión importante en este campo. En particular, ¿cómo un compuesto que sigue la regla de Overton-Meyer provoca directamente un cambio conformacional en la proteína? Normalmente, la regulación alostérica implica un cambio en la forma de la proteína que se adapta a la unión del ligando. Este mecanismo es distinto del mecanismo de la luciferasa. Una segunda cuestión importante es cómo se conservan los sitios de unión no específicos de las proteínas en las distintas especies y por qué generalmente inhiben los receptores excitatorios y potencian los receptores inhibidores.
Varios estudios experimentales y computacionales han demostrado que los anestésicos generales podrían alterar la dinámica de los bucles flexibles que conectan las hélices α en un haz y están expuestos a la interfaz membrana-agua de los receptores de bucle Cys. [43] [44] [45] [46] [47] [48] Sin embargo, los principales bolsillos de unión de los anestésicos generales se encuentran dentro de los haces transmembrana de cuatro hélices α de los receptores de bucle Cys. [49] [50] [51]

El receptor GABA A (GABA A R) es un receptor ionotrópico activado por el neurotransmisor inhibidor ácido γ-aminobutírico (GABA). La activación del receptor GABA A conduce a una afluencia de iones cloruro , lo que provoca la hiperpolarización de las membranas neuronales. [52]
El receptor GABA A ha sido identificado como el objetivo principal de anestésicos intravenosos como el propofol y el etomidato . [4] [5] El sitio de unión del propofol en los receptores GABA A de mamíferos ha sido identificado mediante fotomarcado utilizando un derivado de diazirina . [53] La fuerte activación de la conductancia tónica del receptor GABA A por concentraciones clínicas de propofol ha sido confirmada con registros electrofisiológicos de neuronas CA1 del hipocampo en cortes de cerebro de rata adulta . [54]
Los receptores GABA A que contienen subunidades β3 son los principales objetivos moleculares de las acciones anestésicas del etomidato , mientras que los receptores GABA A que contienen β2 están involucrados en la sedación provocada por este fármaco. [55] Los experimentos electrofisiológicos con concentraciones amnésicas de etomidato también han mostrado una mejora de la conductancia tónica de GABA A de las neuronas piramidales CA1 en cortes del hipocampo. [56]
También se ha demostrado una potente activación de la inhibición mediada por el receptor GABA A con la consiguiente fuerte depresión de las tasas de activación de las neuronas neocorticales para concentraciones clínicas de anestésicos volátiles como el isoflurano , el enflurano y el halotano . [57]
Es poco probable que la mejora de la actividad del receptor GABA A sea el único mecanismo que explique la amplia gama de efectos conductuales de los anestésicos generales. [1] La acumulación de datos experimentales sugiere que la modulación de los canales de potasio de dominio de dos poros , [58] [59] o los canales de sodio dependientes del voltaje [60] también pueden explicar algunas de las acciones de los agentes anestésicos volátiles. Alternativamente, la inhibición de los receptores N-metil-D-aspartato dependientes del glutamato por ketamina , xenón y óxido nitroso proporciona un mecanismo de acción acorde con un perfil analgésico predominante. [1]
Los estereoisómeros que representan imágenes especulares entre sí se denominan enantiómeros o isómeros ópticos (por ejemplo, los isómeros de R-(+)- y S-(−)-etomidato). [1] Los efectos fisicoquímicos de los enantiómeros son siempre idénticos en un entorno aquiral (por ejemplo, en la bicapa lipídica). Sin embargo, los enantiómeros in vivo de muchos anestésicos generales (por ejemplo, isoflurano , tiopental , etomidato ) pueden diferir en gran medida en su potencia anestésica a pesar de los coeficientes de partición aceite/gas similares. [61] [62] Por ejemplo, el isómero R-(+) del etomidato es un anestésico 10 veces más potente que su isómero S-(-). [1] Esto significa que los isómeros ópticos se reparten de forma idéntica en los lípidos, pero tienen efectos diferenciales en los canales iónicos y la transmisión sináptica . Esta objeción proporciona una evidencia convincente de que el objetivo principal de los anestésicos no es la bicapa lipídica aquiral en sí, sino más bien los sitios de unión estereoselectivos en las proteínas de membrana que proporcionan un entorno quiral para interacciones específicas de acoplamiento anestésico-proteína. [1]
Réplica a la objeción: 1) Nunca se consideró el transporte estereoselectivo del anestésico. Los anestésicos son hidrófobos y se transportan unidos a proteínas en la sangre. Cualquier unión estereoselectiva a la proteína de transporte cambiaría la concentración en el sitio de acción. Además, un sumidero de proteína en la membrana podría unirse a uno de los isómeros ligeramente mejor y reducir la concentración efectiva que experimenta la membrana. Todos los estereoisómeros son anestésicos efectivos, solo cambiaron la sensibilidad, lo que sugiere que se deben considerar el transporte selectivo y los sumideros de proteína selectivos. 2) Los lípidos son quirales, lo mismo que las proteínas. Y al igual que las proteínas, los lípidos tienen regiones ordenadas y desordenadas. [63] [64] El campo no investigó la quiralidad de los lípidos ordenados debido a la falta de conocimiento de su existencia.
Todos los anestésicos generales inducen inmovilización (ausencia de movimiento en respuesta a estímulos nocivos) a través de la depresión de las funciones de la médula espinal, mientras que sus acciones amnésicas se ejercen dentro del cerebro. Según la correlación de Meyer-Overton, la potencia anestésica del fármaco es directamente proporcional a su solubilidad en lípidos; sin embargo, hay muchos compuestos que no satisfacen esta regla. Estos fármacos son sorprendentemente similares a los anestésicos generales potentes y se predice que son anestésicos potentes en función de su solubilidad en lípidos, pero ejercen solo un componente de la acción anestésica (amnesia) y no suprimen el movimiento (es decir, no deprimen las funciones de la médula espinal) como lo hacen todos los anestésicos. [65] [66] [67] [68] Estos fármacos se denominan no inmovilizadores. La existencia de no inmovilizadores sugiere que los anestésicos inducen diferentes componentes del efecto anestésico (amnesia e inmovilidad) al afectar diferentes dianas moleculares y no solo una diana (bicapa neuronal) como se creía anteriormente. [69] Un buen ejemplo de no inmovilizadores son los alcanos halogenados que son muy hidrófobos, pero no logran suprimir el movimiento en respuesta a la estimulación nociva en concentraciones apropiadas. Véase también: flurotilo .
Refutación a la objeción: Esta es una falacia lógica . La hipótesis no requiere que cada molécula que se haya probado obedezca a la hipótesis para que esta sea verdadera. La existencia de menos de 10-20 compuestos relacionados que se sabe que desobedecen la hipótesis de Meyer-Overton de ninguna manera niega los cientos, si no miles, de compuestos químicamente diversos que sí obedecen a la hipótesis de Overton-Meyer. Pueden existir excepciones por razones no relacionadas con el mecanismo subyacente a la hipótesis de Meyer-Overton.
Estudios experimentales han demostrado que los anestésicos generales, incluido el etanol, son potentes fluidificantes de las membranas naturales y artificiales. Sin embargo, los cambios en la densidad y fluidez de las membranas en presencia de concentraciones clínicas de anestésicos generales son tan pequeños que aumentos relativamente pequeños de temperatura (~1 °C) pueden imitarlos sin causar anestesia. [70] El cambio en la temperatura corporal de aproximadamente 1 °C está dentro del rango fisiológico y claramente no es suficiente para inducir la pérdida de conciencia per se. Por lo tanto, las membranas se fluidizan solo con grandes cantidades de anestésicos, pero no hay cambios en la fluidez de las membranas cuando las concentraciones de anestésicos son pequeñas y se limitan a ser farmacológicamente relevantes.
Refutación a la objeción: los estudios iniciales solo consideraron la fluidez de la membrana lipídica en masa. Trabajos recientes han demostrado que los cambios de temperatura pueden ocurrir en varios grados en dominios lipídicos nanoscópicos ordenados. [71] Además, la fluidez está regulada activamente por las desaturasas de ácidos grasos . Y por último, la competencia de los anestésicos con las proteínas palmitoiladas ocurre independientemente de la temperatura y a pesar del aumento de los lípidos ordenados. [29]
Según la correlación de Meyer-Overton, en una serie homóloga de cualquier anestésico general (por ejemplo, n - alcoholes o alcanos), el aumento de la longitud de la cadena aumenta la solubilidad lipídica y, por lo tanto, debería producir un aumento correspondiente en la potencia anestésica. Sin embargo, más allá de cierta longitud de cadena, el efecto anestésico desaparece. Para los n -alcoholes, este límite se produce en una longitud de cadena de carbono de aproximadamente 13 [72] y para los n -alcanos en una longitud de cadena de entre 6 y 10, dependiendo de la especie. [73]

Si los anestésicos generales alteran los canales iónicos al dividirse en bicapas lipídicas y perturbarlas, entonces se esperaría que su solubilidad en las bicapas lipídicas también mostrara el efecto de corte. Sin embargo, la partición de alcoholes en bicapas lipídicas no muestra un corte para alcoholes de cadena larga desde n - decanol hasta n - pentadecanol . Un gráfico de la longitud de la cadena frente al logaritmo del coeficiente de partición de la bicapa lipídica/tampón K es lineal, y la adición de cada grupo metileno provoca un cambio en la energía libre de Gibbs de -3,63 kJ/mol.
El efecto de corte se interpretó en un principio como prueba de que los anestésicos ejercen su efecto no actuando globalmente sobre los lípidos de la membrana, sino más bien uniéndose directamente a los bolsillos hidrófobos de volúmenes bien definidos en las proteínas. A medida que la cadena alquílica crece, el anestésico llena más el bolsillo hidrófobo y se une con mayor afinidad. Cuando la molécula es demasiado grande para ser acomodada por completo por el bolsillo hidrófobo, la afinidad de unión ya no aumenta con el aumento de la longitud de la cadena. Por tanto, el volumen de la cadena de n-alcanol en la longitud de corte proporciona una estimación del volumen del sitio de unión. Esta objeción proporcionó la base para la hipótesis de las proteínas sobre el efecto anestésico (véase más adelante).

Sin embargo, el efecto de corte todavía se puede explicar en el marco de la hipótesis de los lípidos. [31] [74] En los alcanoles de cadena corta (A), los segmentos de la cadena son bastante rígidos (en términos de entropía conformacional) y muy cerca del grupo hidroxilo atado a la región interfacial acuosa ("boya"). En consecuencia, estos segmentos redistribuyen eficientemente las tensiones laterales desde el interior de la bicapa hacia la interfaz. En los alcanoles de cadena larga (B), los segmentos de la cadena de hidrocarburos se encuentran más alejados del grupo hidroxilo y son más flexibles que en los alcanoles de cadena corta. La eficiencia de la redistribución de la presión disminuye a medida que aumenta la longitud de la cadena de hidrocarburos hasta que se pierde la potencia anestésica en algún punto. Se propuso que los polialcanoles (C) tendrán un efecto anestésico similar a los 1-alcanoles de cadena corta si la longitud de la cadena entre dos grupos hidroxilo vecinos es menor que el corte. [75] Esta idea fue apoyada por la evidencia experimental porque los polihidroxialcanos 1,6,11,16-hexadecanotetraol y 2,7,12,17-octadecanotetraol exhibieron una potencia anestésica significativa como se propuso originalmente. [74]
Refutación a la objeción: El argumento supone que todas las clases de anestésicos deben actuar de la misma manera sobre la membrana. Es muy posible que una o dos clases de moléculas puedan actuar a través de un mecanismo no mediado por la membrana. Por ejemplo, se ha demostrado que los alcoholes se incorporan a la membrana lipídica a través de una reacción enzimática de transfosfatidilación. [76] El metabolito de etanol se une a un canal anestésico y lo inhibe. Y aunque este mecanismo puede contradecir un mecanismo unitario único de anestesia, no excluye uno mediado por la membrana.