El níquel Raney / ˈ r eɪ n iː ˈ n ɪ k əl / , también llamado níquel esponjoso , [1] es un sólido de grano fino compuesto principalmente de níquel derivado de una aleación de níquel- aluminio . [2] [3] Se conocen varios grados, de los cuales la mayoría son sólidos grises. Algunos son pirofóricos , pero la mayoría se utilizan como lechadas estables al aire. El níquel Raney se utiliza como reactivo y como catalizador en química orgánica . Fue desarrollado en 1926 por el ingeniero estadounidense Murray Raney para la hidrogenación de aceites vegetales. [4] [5] Raney es una marca registrada de WR Grace and Company . Otros productores importantes son Evonik y Johnson Matthey .

La aleación Ni-Al se prepara disolviendo níquel en aluminio fundido seguido de enfriamiento ("templado"). Dependiendo de la relación Ni:Al, el enfriamiento produce varias fases diferentes. Durante el procedimiento de enfriamiento, se añaden pequeñas cantidades de un tercer metal, como zinc o cromo, para mejorar la actividad del catalizador resultante. Este tercer metal se llama " promotor ". [6] El promotor cambia la mezcla de una aleación binaria a una aleación ternaria, lo que puede conducir a diferentes propiedades de enfriamiento y lixiviación durante la activación.
En el proceso de activación, la aleación, normalmente en forma de polvo fino, se trata con una solución concentrada de hidróxido de sodio . [3] La reacción de lixiviación simplificada viene dada por la siguiente ecuación química :
La formación de aluminato de sodio (Na[Al(OH) 4 ]) requiere que se utilicen soluciones de alta concentración de hidróxido de sodio para evitar la formación de hidróxido de aluminio , que de otro modo precipitaría como bayerita . [6] Por lo tanto, se utilizan soluciones de hidróxido de sodio con concentraciones de hasta 5 M.
La temperatura utilizada para lixiviar la aleación tiene un marcado efecto sobre las propiedades del catalizador. Comúnmente, la lixiviación se realiza entre 70 y 100 °C. El área superficial del níquel Raney (y de los catalizadores relacionados en general) tiende a disminuir al aumentar la temperatura de lixiviación. [7] Esto se debe a reordenamientos estructurales dentro de la aleación que pueden considerarse análogos a la sinterización , donde los ligamentos de la aleación comenzarían a adherirse entre sí a temperaturas más altas, lo que llevaría a la pérdida de la estructura porosa. [ cita necesaria ]
Durante el proceso de activación, el Al se lixivia de las fases NiAl 3 y Ni 2 Al 3 que están presentes en la aleación, mientras que la mayor parte del Ni permanece en forma de NiAl. La eliminación de Al de algunas fases pero no de otras se conoce como " lixiviación selectiva ". Se ha demostrado que la fase NiAl proporciona la estabilidad estructural y térmica del catalizador. Como resultado, el catalizador es bastante resistente a la descomposición ("romperse", comúnmente conocido como "envejecimiento"). [7] Esta resistencia permite que el níquel Raney se almacene y reutilice durante un período prolongado; sin embargo, normalmente se prefieren las preparaciones frescas para uso en el laboratorio. [8] Por esta razón, el níquel Raney comercial está disponible tanto en forma "activa" como "inactiva".
Antes del almacenamiento, el catalizador se puede lavar con agua destilada a temperatura ambiente para eliminar el aluminato de sodio restante. Se prefiere el agua libre de oxígeno ( desgasificada ) para el almacenamiento para evitar la oxidación del catalizador, lo que aceleraría su proceso de envejecimiento y daría como resultado una actividad catalítica reducida. [6]



Macroscópicamente, el níquel Raney es un polvo gris finamente dividido. Microscópicamente, cada partícula de este polvo es una malla tridimensional , con poros de tamaño y forma irregular, la gran mayoría de los cuales se crean durante el proceso de lixiviación. El níquel Raney se destaca por ser térmica y estructuralmente estable, además de tener una gran superficie Brunauer - Emmett - Teller ( BET ). Estas propiedades son un resultado directo del proceso de activación y contribuyen a una actividad catalítica relativamente alta. [ cita necesaria ]
El área superficial normalmente se determina mediante una medición BET utilizando un gas que se adsorbe preferentemente en superficies metálicas, como el hidrógeno . Utilizando este tipo de medición, se ha demostrado que casi toda el área expuesta en una partícula del catalizador tiene Ni en su superficie. [6] Dado que el Ni es el metal activo del catalizador, una gran superficie de Ni implica que hay una gran superficie disponible para que las reacciones ocurran simultáneamente, lo que se refleja en una mayor actividad del catalizador. El níquel Raney disponible comercialmente tiene una superficie de Ni promedio de 100 m2 por gramo de catalizador. [6]
Una alta actividad catalítica, junto con el hecho de que el hidrógeno se absorbe dentro de los poros del catalizador durante la activación, hace que el níquel Raney sea un catalizador útil para muchas reacciones de hidrogenación . Su estabilidad estructural y térmica (es decir, no se descompone a altas temperaturas) permite su uso en una amplia gama de condiciones de reacción. [9] [10] Además, la solubilidad del níquel Raney es insignificante en la mayoría de los disolventes de laboratorio comunes, con la excepción de ácidos minerales como el ácido clorhídrico, y su densidad relativamente alta (aproximadamente 6,5 g cm −3 ) [1] también facilita su separación de una fase líquida después de que se completa una reacción.
El níquel Raney se utiliza en una gran cantidad de procesos industriales y en síntesis orgánica debido a su estabilidad y alta actividad catalítica a temperatura ambiente. [6] [11] [12]
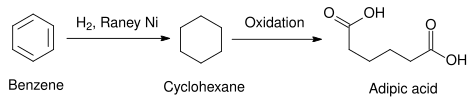
En una aplicación comercial, el níquel Raney se utiliza como catalizador para la hidrogenación de benceno a ciclohexano . En algunos casos se utilizan otros catalizadores heterogéneos, como los que utilizan elementos del grupo del platino . Los metales del platino tienden a ser más activos y requieren temperaturas más suaves, pero son más caros que el níquel Raney. [13] El ciclohexano así producido puede utilizarse en la síntesis de ácido adípico , materia prima utilizada en la producción industrial de poliamidas como el nailon. [14]
Otras aplicaciones industriales del níquel Raney incluyen la conversión de:
El níquel Raney se utiliza en síntesis orgánica para la desulfuración . Por ejemplo, los tioacetales se reducirán a hidrocarburos en el último paso de la reducción de Mozingo : [14] [15]

Los tioles [16] y los sulfuros [17] se pueden eliminar de compuestos alifáticos , aromáticos o heteroaromáticos. Asimismo, el níquel Raney eliminará el azufre del tiofeno para dar un alcano saturado . [18]

Se utiliza normalmente en la reducción de compuestos con enlaces múltiples , como alquinos , alquenos , [19] nitrilos , [20] dienos , aromáticos [21] y compuestos que contienen carbonilo . Además, el níquel Raney reducirá los enlaces heteroátomo-heteroátomo, como las hidracinas , [22] grupos nitro y nitrosaminas. [23] También ha encontrado uso en la alquilación reductora de aminas [24] y la aminación de alcoholes.
Al reducir un doble enlace carbono-carbono, el níquel Raney agregará hidrógeno de forma sintética . [14]
También se ha descrito el cobalto Raney.
En contraste con la naturaleza pirofórica de algunas formas de níquel Raney, los catalizadores basados en siliciuro de níquel representan alternativas potencialmente más seguras. [25]


Debido a su gran superficie y su gran volumen de gas hidrógeno contenido, el níquel Raney activado y seco es un material pirofórico que requiere manipulación bajo una atmósfera inerte . El níquel Raney normalmente se suministra como una suspensión al 50% en agua. Incluso después de la reacción, el níquel Raney residual contiene cantidades significativas de gas hidrógeno y puede encenderse espontáneamente cuando se expone al aire. [26]
Además, la exposición aguda al níquel Raney puede causar irritación del tracto respiratorio y de las cavidades nasales, y provoca fibrosis pulmonar si se inhala. La ingestión puede provocar convulsiones y trastornos intestinales. También puede causar irritación en los ojos y la piel. La exposición crónica puede provocar neumonitis y otros signos de sensibilización al níquel, como erupciones cutáneas ("picazón del níquel"). [27]
El níquel también está clasificado como posible carcinógeno humano por la IARC (Grupo 2B, categoría 3 de la UE ) y teratógeno , mientras que la inhalación de partículas finas de óxido de aluminio está asociada con la enfermedad de Shaver .
Murray Raney se graduó como ingeniero mecánico en la Universidad de Kentucky en 1909. En 1915 se incorporó a la Lookout Oil and Refining Company en Tennessee y fue responsable de la instalación de celdas electrolíticas para la producción de hidrógeno que se utilizaba en la hidrogenación de aceites vegetales. . Durante esa época, la industria utilizaba un catalizador de níquel preparado a partir de óxido de níquel (II) . Creyendo que se podían producir mejores catalizadores, alrededor de 1921 comenzó a realizar investigaciones independientes mientras aún trabajaba para Lookout Oil. En 1924 se produjo una aleación de Ni/ Si en proporción 1:1 que, después del tratamiento con hidróxido de sodio, resultó ser cinco veces más activa que el mejor catalizador utilizado en la hidrogenación del aceite de semilla de algodón. En diciembre de 1925 se emitió una patente para este descubrimiento. [28]
Posteriormente, Raney produjo una aleación 1:1 Ni/Al siguiendo un procedimiento similar al utilizado para el catalizador de níquel-silicio. Descubrió que el catalizador resultante era aún más activo y presentó una solicitud de patente en 1926. [29] Esta es ahora una composición de aleación común para los catalizadores de níquel Raney modernos. [2] Otras composiciones de aleaciones comunes incluyen 21:29 Ni/Al y 3:7 Ni/Al. Tanto la actividad como los protocolos de preparación de estos catalizadores varían. [2] [30]
Tras el desarrollo del níquel Raney, se consideraron otros sistemas de aleaciones con aluminio, de los cuales los más destacados incluyen el cobre, el rutenio y el cobalto . [31] Investigaciones adicionales demostraron que agregar una pequeña cantidad de un tercer metal a la aleación binaria promovería la actividad del catalizador. Algunos promotores muy utilizados son el zinc, el molibdeno y el cromo . Se ha ideado una forma alternativa de preparar níquel Raney enantioselectivo mediante adsorción superficial de ácido tartárico . [32]