

Un piretroide es un compuesto orgánico similar a las piretrinas naturales , que son producidas por las flores de los piretros ( Chrysanthemum cinerariaefolium y C. coccineum ). Los piretroides se utilizan como insecticidas comerciales y domésticos . [1]
En concentraciones domésticas, los piretroides son generalmente inofensivos para los humanos. [1] Sin embargo, los piretroides son tóxicos para insectos como abejas , libélulas , efímeras , tábanos y algunos otros invertebrados , incluidos aquellos que constituyen la base de las redes alimentarias acuáticas y terrestres . [2] Los piretroides son tóxicos para los organismos acuáticos , especialmente los peces. [3] Se ha demostrado que son una medida de control eficaz de los brotes de malaria, mediante aplicaciones en interiores. [4]
Los piretroides son excitotóxicos para los axones . Actúan impidiendo el cierre de los canales de sodio dependientes de voltaje en las membranas axonales . El canal de sodio es una proteína de membrana con un interior hidrófilo . Este interior tiene una forma precisa para permitir que los iones de sodio atraviesen la membrana, entren en el axón y propaguen un potencial de acción . Cuando la toxina mantiene los canales en su estado abierto, los nervios no pueden repolarizarse , quedando la membrana axonal permanentemente despolarizada , paralizando así el organismo. [5] Los piretroides se pueden combinar con el sinérgico butóxido de piperonilo , un conocido inhibidor de las enzimas microsomales P450 que son importantes en la metabolización del piretroide. De este modo, se aumenta la eficacia (letalidad) del piretroide. [6] Es probable que también existan otros mecanismos de intoxicación. [7] Se cree que la alteración de la actividad neuroendocrina contribuye a sus efectos irreversibles en los insectos, lo que indica una acción piretroide en los canales de calcio dependientes de voltaje (y quizás en otros canales dependientes de voltaje más ampliamente). [7]
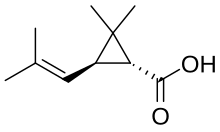
Los piretroides se clasifican según su mecanismo de acción biológica, ya que no comparten una estructura química común. Muchos son derivados del ácido 2,2-dimetilciclopropanocarboxílico, como el ácido crisantemico , esterificados con un alcohol . Sin embargo, el anillo ciclopropilo no se encuentra en todos los piretroides. El fenvalerato , que se desarrolló en 1972, es un ejemplo de ello y fue el primer piretroide comercializado sin ese grupo.
Los piretroides que carecen de un grupo α-ciano a menudo se clasifican como piretroides de tipo I y aquellos que lo tienen se denominan piretroides de tipo II . Los piretroides que tienen un nombre común que comienza con "cy" tienen un grupo ciano y son de tipo II. El fenvalerato también contiene un grupo α-ciano .
Algunos piretroides, como el etofenprox , también carecen del enlace éster que se encuentra en la mayoría de los otros piretroides y tienen un enlace éter en su lugar. El silafluofen también se clasifica como piretroide y tiene un átomo de silicio en lugar del éster. Los piretroides suelen tener centros quirales y sólo ciertos estereoisómeros funcionan eficazmente como insecticidas . [8]
Los piretroides son tóxicos para insectos como abejas , libélulas , efímeras , tábanos y algunos otros invertebrados , incluidos los que constituyen la base de las redes alimentarias acuáticas y terrestres . [2] Son tóxicos para los organismos acuáticos, incluidos los peces. [3]
Los piretroides generalmente se descomponen con la luz solar y la atmósfera en uno o dos días; sin embargo, cuando se asocian con sedimentos, pueden persistir durante algún tiempo. [9]
Los piretroides no se ven afectados por los sistemas de tratamiento secundario convencionales en las instalaciones de tratamiento de aguas residuales municipales . Aparecen en los efluentes, normalmente en niveles letales para los invertebrados. [10]
La absorción de piretroides puede ocurrir a través de la piel, inhalación o ingestión. [11] Los piretroides a menudo no se unen eficientemente a los canales de sodio de los mamíferos . [12] También se absorben mal a través de la piel y el hígado humano a menudo puede metabolizarlos de manera relativamente eficiente. Por tanto, los piretroides son mucho menos tóxicos para los humanos que para los insectos. [13]
No está bien establecido si la exposición crónica a pequeñas cantidades de piretroides es peligrosa o no. [14] Sin embargo, grandes dosis pueden causar intoxicación aguda, que rara vez pone en peligro la vida. Los síntomas típicos incluyen parestesia facial , picazón, ardor, mareos, náuseas, vómitos y casos más graves de espasmos musculares. La intoxicación grave suele ser causada por la ingestión de piretroides y puede provocar una variedad de síntomas como convulsiones, coma , hemorragia o edema pulmonar . [11] Existe una asociación entre los piretroides y un peor desarrollo socioemocional y del lenguaje temprano. [4]
Los piretroides son muy tóxicos para los gatos , pero no para los perros . El envenenamiento en gatos puede provocar convulsiones, fiebre, ataxia e incluso la muerte. Puede producirse intoxicación si se utilizan en gatos productos para el tratamiento de pulgas que contienen piretroides, destinados a perros. El hígado de los gatos desintoxica los piretroides mediante glucuronidación peor que el de los perros, lo que explica esta diferencia. [15] Aparte de los gatos, los piretroides no suelen ser tóxicos para los mamíferos ni para las aves . [16] A menudo son tóxicos para peces , reptiles y anfibios . [17]
El uso de piretroides como insecticidas ha llevado al desarrollo de una resistencia generalizada a ellos entre algunas poblaciones de insectos, especialmente mosquitos. [18] Aunque las chinches casi fueron erradicadas en América del Norte mediante el uso de DDT y organofosforados , se han desarrollado poblaciones de chinches resistentes a ambos. El uso de DDT con este fin fue prohibido y su reintroducción no ofrecería una solución al problema de las chinches, debido a su resistencia. [19] Los piretroides se utilizaron cada vez más comúnmente contra las chinches, pero ahora también se han desarrollado poblaciones resistentes a ellos. [20] [21] [22] [23] Las poblaciones de polillas Diamondback también han desarrollado comúnmente resistencia a los piretroides [24] [ se necesita una mejor fuente ] , incluso en los estados de EE. UU. , Dakota del Norte [25] y Wisconsin [26] , mientras que los piretroides todavía son Recomendado en California . [27] Se ha descubierto que varias poblaciones de mosquitos tienen un alto nivel de resistencia, incluido Anopheles gambiae sl en África occidental por Chandre et al 1999 hasta Pwalia et al 2019, A. arabiensis en Sudán por Ismail et al 2018 y Gambia por Opondo et al 2019, y Aedes aegypti en el sudeste asiático por Amelia-Yap et al 2018, Papua Nueva Guinea por Demok et al 2019 y varios otros lugares por Smith et al 2016. [18]
La resistencia al derribo ( kdr ) es uno de los tipos de resistencia más fuertes. [28] Las mutaciones kdr confieren resistencia en el sitio objetivo al DDT y a los piretroides y resistencia cruzada al DDT. [28] La mayoría de las mutaciones de kdr se encuentran dentro o cerca de los dos genes del canal de sodio de los artrópodos . [28]
Los piretroides fueron introducidos por un equipo de científicos de Rothamsted Research en las décadas de 1960 y 1970, tras el esclarecimiento de las estructuras de la piretrina I y II por Hermann Staudinger y Leopold Ružička en la década de 1920. [29] Los piretroides representaron un avance importante en la química que permitiría sintetizar el análogo de la versión natural que se encuentra en el piretro . Su actividad insecticida tiene una toxicidad para los mamíferos relativamente baja y una biodegradación inusualmente rápida. Su desarrollo coincidió con la identificación de problemas con el uso del DDT . Su trabajo consistió, en primer lugar, en identificar los componentes más activos del piretro , extraído de las flores de crisantemo del este de África y del que se sabe desde hace mucho tiempo que tiene propiedades insecticidas. El piretro derriba rápidamente a los insectos voladores pero tiene una persistencia insignificante, lo que es bueno para el medio ambiente pero da poca eficacia cuando se aplica en el campo. Los piretroides son esencialmente formas químicamente estabilizadas de piretro natural y pertenecen al grupo 3 del IRAC MoA (interfieren con el transporte de sodio en las células nerviosas de los insectos). [30]
Los piretroides de primera generación , desarrollados en la década de 1960, incluyen la bioaletrina , la tetrametrina , la resmetrina y la bioresmetrina. Son más activos que el piretro natural pero son inestables a la luz del sol. Con la revisión 91/414/CEE, [31] muchos compuestos de primera generación no se han incluido en el Anexo 1, probablemente porque el mercado no es lo suficientemente grande como para justificar los costos de un nuevo registro (en lugar de preocupaciones especiales sobre la seguridad). .
En 1974, el equipo de Rothamsted había descubierto una segunda generación de compuestos más persistentes, en particular: permetrina , cipermetrina y deltametrina . Son sustancialmente más resistentes a la degradación por la luz y el aire, lo que los hace adecuados para su uso en agricultura , pero tienen toxicidades para los mamíferos significativamente mayores. Durante las décadas siguientes, a estos derivados les siguieron otros compuestos patentados como el fenvalerato , la lambda-cialotrina y la beta- ciflutrina . La mayoría de las patentes ya han expirado, lo que hace que estos compuestos sean baratos y, por lo tanto, populares (aunque la permetrina y el fenvalerato no se han vuelto a registrar según el proceso 91/414/CEE).