Un impulso genético es un proceso natural [1] y una tecnología de ingeniería genética que propaga un conjunto particular de genes en toda una población [2] alterando la probabilidad de que un alelo específico se transmita a la descendencia (en lugar de la probabilidad mendeliana del 50 % ). . Los impulsores genéticos pueden surgir a través de una variedad de mecanismos. [3] [4] Se han propuesto para proporcionar un medio eficaz de modificar genéticamente poblaciones específicas y especies enteras.
La técnica puede emplear la adición, eliminación, alteración o modificación de genes. [5] [6]
Las aplicaciones propuestas incluyen el exterminio de insectos portadores de patógenos (en particular, mosquitos que transmiten patógenos de la malaria , el dengue y el zika ), el control de especies invasoras o la eliminación de la resistencia a herbicidas o pesticidas . [7] [5] [8] [9]
Como ocurre con cualquier técnica potencialmente poderosa, los impulsores genéticos pueden usarse indebidamente de diversas maneras o inducir consecuencias no deseadas . Por ejemplo, un impulso genético destinado a afectar sólo a una población local podría extenderse a toda una especie. Los impulsores genéticos que erradican poblaciones de especies invasoras en sus hábitats no nativos pueden tener consecuencias para la población de la especie en su conjunto, incluso en su hábitat nativo. Cualquier regreso accidental de individuos de la especie a sus hábitats originales, a través de migración natural, alteración ambiental (tormentas, inundaciones, etc.), transporte humano accidental o reubicación intencionada, podría llevar involuntariamente a la especie a la extinción si los individuos reubicados portaran genes dañinos. unidades. [10]
Los impulsores genéticos pueden construirse a partir de muchos elementos genéticos egoístas que ocurren naturalmente y que utilizan una variedad de mecanismos moleculares. [3] Estos mecanismos naturales inducen una distorsión de la segregación similar en la naturaleza, que surge cuando los alelos desarrollan mecanismos moleculares que les dan una probabilidad de transmisión mayor que el 50% normal.
La mayoría de los impulsores genéticos se han desarrollado en insectos, especialmente mosquitos, como una forma de controlar los patógenos transmitidos por insectos. Los avances recientes diseñaron impulsores genéticos directamente en los virus, en particular los herpesvirus . Estos impulsores genéticos virales pueden propagar una modificación en la población de virus y tener como objetivo reducir la infectividad del virus. [11] [12]
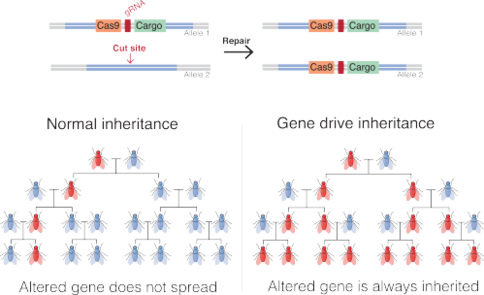
En las especies que se reproducen sexualmente , la mayoría de los genes están presentes en dos copias (que pueden ser alelos iguales o diferentes ), cualquiera de las cuales tiene un 50% de posibilidades de pasar a un descendiente. Al sesgar la herencia de genes alterados particulares, los impulsores genéticos sintéticos podrían propagar las alteraciones a través de una población. [5] [6]

A nivel molecular, un impulso genético de endonucleasa funciona cortando un cromosoma en un sitio específico que no codifica el impulso, induciendo a la célula a reparar el daño copiando la secuencia del impulso en el cromosoma dañado. La célula tiene entonces dos copias de la secuencia de conducción. El método deriva de técnicas de edición del genoma y se basa en la recombinación homóloga . Para lograr este comportamiento, los impulsores genéticos de endonucleasa constan de dos elementos anidados:
Como resultado, la inserción del impulso genético en el genoma volverá a ocurrir en cada organismo que herede una copia de la modificación y una copia del gen de tipo salvaje. Si el impulso genético ya está presente en el óvulo (por ejemplo, cuando se recibe de uno de los padres), todos los gametos del individuo portarán el impulso genético (en lugar del 50% en el caso de un gen normal). [5]
Dado que su frecuencia nunca puede más que duplicarse con cada generación, un impulso genético introducido en un solo individuo normalmente requiere docenas de generaciones para afectar a una fracción sustancial de una población. Alternativamente, la liberación de organismos que contienen impulsos en cantidades suficientes puede afectar al resto en unas pocas generaciones; por ejemplo, al introducirlo en cada mil individuos, sólo se necesitan entre 12 y 15 generaciones para estar presente en todos los individuos. [16] Si un impulso genético finalmente se fijará en una población y a qué velocidad depende de su efecto sobre la aptitud individual, la tasa de conversión de alelos y la estructura de la población. En una población bien mezclada y con frecuencias de conversión de alelos realistas (≈90%), la genética de poblaciones predice que los impulsores genéticos se fijan para un coeficiente de selección menor que 0,3; [16] en otras palabras, los impulsores genéticos se pueden utilizar para difundir modificaciones siempre que el éxito reproductivo no se reduzca en más del 30%. Esto contrasta con los genes normales, que sólo pueden propagarse a grandes poblaciones si mejoran la aptitud física.
Debido a que la estrategia generalmente se basa en la presencia simultánea de un alelo no modificado y un alelo impulsor genético en el mismo núcleo celular , generalmente se había asumido que un impulso genético sólo podría diseñarse en organismos que se reproducen sexualmente, excluyendo bacterias y virus . Sin embargo, durante una infección viral , los virus pueden acumular cientos o miles de copias del genoma en las células infectadas. Las células suelen estar coinfectadas por múltiples viriones y la recombinación entre genomas virales es una fuente de diversidad bien conocida y generalizada para muchos virus. En particular, los herpesvirus son virus de ADN de replicación nuclear con grandes genomas de ADN de doble hebra y con frecuencia experimentan recombinación homóloga durante su ciclo de replicación.
Estas propiedades han permitido el diseño de una estrategia de impulso genético que no implica reproducción sexual, sino que se basa en la coinfección de una célula determinada por un virus de origen natural y otro modificado. Tras la coinfección, el genoma no modificado se corta y repara mediante recombinación homóloga, produciendo nuevos virus impulsores genéticos que pueden reemplazar progresivamente a la población natural. En experimentos con cultivos celulares , se demostró que un impulso genético viral puede propagarse a la población viral y reducir fuertemente la infectividad del virus, lo que abre nuevas estrategias terapéuticas contra los herpesvirus. [11]
Debido a que los impulsores genéticos se propagan reemplazando otros alelos que contienen un sitio de corte y las homologías correspondientes, su aplicación se ha limitado principalmente a especies que se reproducen sexualmente (porque son diploides o poliploides y los alelos se mezclan en cada generación). Como efecto secundario, la endogamia podría ser en principio un mecanismo de escape, pero es difícil evaluar hasta qué punto esto puede suceder en la práctica. [17]
Debido al número de generaciones necesarias para que un impulso genético afecte a toda una población, el tiempo hasta la universalidad varía según el ciclo reproductivo de cada especie: puede requerir menos de un año para algunos invertebrados, pero siglos para organismos con intervalos de años. entre el nacimiento y la madurez sexual , como los humanos. [18] Por lo tanto, esta tecnología es de mayor utilidad en especies de rápida reproducción.
La eficacia en la práctica real varía entre técnicas, especialmente según la elección del promotor de la línea germinal . Lin y Potter 2016 (a) divulga la tecnología promotora CRISPR knockin asistida por homología (HACK) y Lin y Potter 2016 (b) demuestra su uso real, logrando una alta proporción de progenie alterada de cada madre de Drosophila alterada . [19]
Los problemas destacados por los investigadores incluyen: [20]
El Broad Institute del MIT y Harvard añadió los impulsores genéticos a una lista de usos de la tecnología de edición genética que no cree que las empresas deban implementar. [21] [ se necesita una mejor fuente ]
Los impulsores genéticos afectan a todas las generaciones futuras y representan la posibilidad de un cambio mayor en una especie viva de lo que ha sido posible antes. [22]
En diciembre de 2015, científicos de las principales academias del mundo pidieron una moratoria sobre las ediciones heredables del genoma humano que afectarían la línea germinal, incluidas aquellas relacionadas con las tecnologías CRISPR-Cas9, [23] pero apoyaron la continuación de la investigación básica y la edición de genes que no afectarían a las generaciones futuras. . [24] En febrero de 2016, los reguladores dieron permiso a los científicos británicos para modificar genéticamente embriones humanos mediante el uso de CRISPR-Cas9 y técnicas relacionadas con la condición de que los embriones fueran destruidos en siete días. [25] [26] En junio de 2016, las Academias Nacionales de Ciencias, Ingeniería y Medicina de EE. UU. publicaron un informe sobre sus "Recomendaciones para una conducta responsable" de los impulsores genéticos. [27]
Un estudio de modelado matemático de 2018 sugiere que a pesar de la resistencia al impulso genético preexistente y en evolución (causada por mutaciones en el sitio de corte), incluso un impulso genético de "tipo alteración" CRISPR ineficiente puede lograr la fijación en poblaciones pequeñas. Con una cantidad pequeña pero distinta de cero de flujo genético entre muchas poblaciones locales, el impulso genético puede escapar y convertir también a poblaciones externas. [28]
Kevin M. Esvelt afirmó que era necesaria una conversación abierta sobre la seguridad de los impulsores genéticos: "En nuestra opinión, es prudente suponer que es probable que los sistemas de impulsores genéticos invasivos y autopropagantes se propaguen a todas las poblaciones de las especies objetivo en todo el mundo. En consecuencia, sólo deberían construirse para combatir verdaderas plagas como la malaria, para la cual tenemos pocas contramedidas adecuadas y que ofrecen un camino realista hacia un acuerdo internacional para desplegar entre todas las naciones afectadas". [29] Pasó a un modelo abierto para su propia investigación sobre el uso de impulsores genéticos para erradicar la enfermedad de Lyme en Nantucket y Martha's Vineyard . [30] Esvelt y sus colegas sugirieron que CRISPR podría usarse para salvar de la extinción la vida silvestre en peligro de extinción. Más tarde, Esvelt se retractó de su apoyo a la idea, excepto en el caso de poblaciones extremadamente peligrosas, como los mosquitos portadores de malaria, y las islas aisladas que evitarían que la campaña se extendiera más allá del área objetivo. [31]
Austin Burt, genetista evolutivo del Imperial College de Londres , introdujo en 2003 la posibilidad de conducir impulsos genéticos basados en elementos genéticos egoístas de endonucleasas de localización natural. [6]
Los investigadores ya habían demostrado que esos genes podían actuar de forma egoísta y propagarse rápidamente a lo largo de generaciones sucesivas. Burt sugirió que los impulsores genéticos podrían usarse para evitar que una población de mosquitos transmita el parásito de la malaria o para reducir una población de mosquitos. Se han demostrado en el laboratorio impulsores genéticos basados en endonucleasas autoguiantes en poblaciones transgénicas de mosquitos [32] y moscas de la fruta. [33] [34] Sin embargo, las endonucleasas dirigidas son específicas de secuencia. Modificar su especificidad para apuntar a otras secuencias de interés sigue siendo un desafío importante. [3] Las posibles aplicaciones del impulso genético permanecieron limitadas hasta el descubrimiento de CRISPR y las endonucleasas guiadas por ARN asociadas, como Cas9 y Cas12a .
En junio de 2014, el Programa Especial de Investigación y Capacitación en Enfermedades Tropicales de la Organización Mundial de la Salud (OMS) [35] publicó directrices [36] para evaluar mosquitos genéticamente modificados. En 2013, la Autoridad Europea de Seguridad Alimentaria emitió un protocolo [37] para evaluaciones ambientales de todos los organismos genéticamente modificados .
Target Malaria , un proyecto financiado por la Fundación Bill y Melinda Gates , invirtió 75 millones de dólares en tecnología de impulso genético. La fundación estimó originalmente que la tecnología estaría lista para su uso en el campo en 2029 en algún lugar de África. Sin embargo, en 2016 Gates cambió esta estimación a algún momento dentro de los dos años siguientes. [38] En diciembre de 2017, documentos publicados en virtud de la Ley de Libertad de Información mostraron que DARPA había invertido 100 millones de dólares en investigación de impulsores genéticos. [39]
Los científicos han diseñado múltiples estrategias para mantener el control sobre los impulsores genéticos. [ cita necesaria ]
En 2020, los investigadores informaron sobre el desarrollo de dos elementos guía activos exclusivos de ARN que, según su estudio, pueden permitir detener o eliminar impulsores genéticos introducidos en poblaciones en la naturaleza con la edición del gen CRISPR-Cas9 . El autor principal del artículo advierte que los dos sistemas neutralizantes que demostraron en ensayos en jaulas "no deben usarse con una falsa sensación de seguridad para los impulsores genéticos implementados en el campo". [40] [41]
Si la eliminación no es necesaria, puede ser deseable preservar intencionalmente la población objetivo en un nivel más bajo mediante el uso de una tecnología de impulso genético menos severa. Esto funciona manteniendo indefinidamente la población semidefectuosa en el área objetivo, desplazando así a posibles poblaciones silvestres cercanas que de otro modo regresarían para llenar un vacío. [42]
CRISPR [43] es el método líder de ingeniería genética . [44] En 2014, Esvelt y sus compañeros de trabajo sugirieron por primera vez que CRISPR/Cas9 podría usarse para desarrollar impulsores genéticos. [5] En 2015, los investigadores informaron sobre la ingeniería exitosa de impulsores genéticos basados en CRISPR en Saccharomyces [45] , Drosophila , [46] y mosquitos . [47] [48] Informaron sobre una distorsión eficiente de la herencia a lo largo de generaciones sucesivas, y un estudio demostró la propagación de un gen en poblaciones de laboratorio. [48] Se esperaba que surgieran alelos resistentes a los impulsos para cada uno de los impulsores genéticos descritos; sin embargo, esto podría retrasarse o evitarse centrándose en sitios altamente conservados en los que se esperaba que la resistencia tuviera un alto costo de aptitud física.
Debido a la flexibilidad de selección de objetivos de CRISPR, los impulsores genéticos podrían teóricamente usarse para diseñar casi cualquier rasgo. A diferencia de los enfoques anteriores, podrían adaptarse para bloquear la evolución de la resistencia al impulso apuntando a múltiples secuencias. CRISPR también podría permitir arquitecturas de impulso genético que controlen poblaciones en lugar de eliminarlas. [ cita necesaria ]
En 2022, se utilizó t-CRISPR para transmitir el gen del “haplotipo t” a aproximadamente el 95% de la descendencia. El enfoque propaga copias defectuosas de un gen de fertilidad femenino a la descendencia, volviéndolas infértiles. Los investigadores informaron que sus modelos sugerían que agregar 256 animales alterados a una isla con una población de 200.000 ratones eliminaría la población en unos 25 años. Los métodos tradicionales de veneno y trampas no eran necesarios. [49]
Los impulsores genéticos tienen dos clases principales de aplicaciones, que tienen implicaciones de diferente importancia:
Debido a su riesgo potencial sin precedentes, se han propuesto y probado mecanismos de salvaguardia. [45] [50]
Una posible aplicación es modificar genéticamente mosquitos , ratones y otros vectores de enfermedades para que no puedan transmitir enfermedades, como la malaria y el dengue en el caso de los mosquitos, y las enfermedades transmitidas por garrapatas en el caso de los ratones. [51] Los investigadores han afirmado que al aplicar la técnica al 1% de la población silvestre de mosquitos, podrían erradicar la malaria en un año. [52]
Un impulso genético podría usarse para eliminar especies invasoras y, por ejemplo, se ha propuesto como una forma de eliminar especies invasoras en Nueva Zelanda . [53] Los impulsores genéticos para fines de conservación de la biodiversidad se están explorando como parte del programa de Biocontrol Genético de Roedores Invasores (GBIRd) porque ofrecen el potencial de reducir el riesgo para las especies no objetivo y reducir los costos en comparación con las técnicas tradicionales de eliminación de especies invasoras. Dados los riesgos de un enfoque de este tipo que se describe a continuación, la asociación GBIRd está comprometida con un proceso deliberado y gradual que sólo procederá con la alineación pública, según lo recomendado por los investigadores líderes en impulso genético del mundo de las Academias Nacionales de Ciencias de Australia y Estados Unidos. muchos otros. [54] Existe una red de extensión más amplia para la investigación de impulsores genéticos para crear conciencia sobre el valor de la investigación de impulsores genéticos para el bien público. [55]
Algunos científicos están preocupados por la técnica, temiendo que pueda propagarse y acabar con especies en hábitats nativos. [56] El gen podría mutar, causando potencialmente problemas imprevistos (al igual que cualquier gen). [57] Muchas especies no nativas pueden hibridarse con especies nativas, de modo que un impulso genético que afecte a una planta o animal no nativo que se hibrida con una especie nativa podría condenar a la especie nativa. Muchas especies no nativas se han naturalizado tan bien en su nuevo entorno que los cultivos y/o las especies nativas se han adaptado para depender de ellas. [58]
El proyecto Predator Free 2050 es un programa del gobierno de Nueva Zelanda para eliminar ocho especies de mamíferos depredadores invasores (incluidas ratas, comadrejas de cola corta y zarigüeyas) del país para 2050. [59] [60] El proyecto fue anunciado por primera vez en 2016 por El primer ministro de Nueva Zelanda, John Key , y en enero de 2017 se anunció que se considerarían los impulsores genéticos en el esfuerzo, pero esto aún no se ha actualizado. [60] En 2017, un grupo en Australia y otro en Texas publicaron una investigación preliminar sobre la creación de 'ratones sin hijas' utilizando impulsores genéticos en mamíferos. [61]
En 2017, científicos de la Universidad de California en Riverside desarrollaron un impulso genético para atacar a la invasora drosophila de alas manchadas , un tipo de mosca de la fruta originaria de Asia que está costando a las granjas de cerezas de California 700 millones de dólares al año debido al ovipositor con bordes afilados de su cola. que destruye el fruto sin defecto. La principal estrategia de control alternativa implica el uso de insecticidas llamados piretroides que matan a casi todos los insectos con los que entra en contacto. [21]
El filósofo transhumanista David Pearce ha abogado por el uso de impulsores genéticos basados en CRISPR para reducir el sufrimiento de los animales salvajes . [62] Kevin M. Esvelt , un biólogo estadounidense que ha ayudado a desarrollar la tecnología de impulso genético, ha argumentado que existe un argumento moral para la eliminación del gusano barrenador del Nuevo Mundo a través de tales tecnologías debido al inmenso sufrimiento que experimentan los animales salvajes infestados cuando se comen vivos. [63]