Las anhidrasas carbónicas (o carbonato deshidratasas ) ( EC 4.2.1.1) forman una familia de enzimas que catalizan la interconversión entre el dióxido de carbono y el agua y los iones disociados del ácido carbónico (es decir, iones de bicarbonato e hidrógeno ). [1] El sitio activo de la mayoría de las anhidrasas carbónicas contiene un ion de zinc . Por lo tanto, se clasifican como metaloenzimas . La enzima mantiene el equilibrio ácido-base y ayuda a transportar el dióxido de carbono. [2]
La anhidrasa carbónica ayuda a mantener la homeostasis ácido-base , regular el pH y el equilibrio de líquidos. Dependiendo de su ubicación, el papel de la enzima cambia ligeramente. Por ejemplo, la anhidrasa carbónica produce ácido en el revestimiento del estómago. En el riñón, el control de los iones de bicarbonato influye en el contenido de agua de la célula. El control de los iones de bicarbonato también influye en el contenido de agua en los ojos. Los inhibidores de la anhidrasa carbónica se utilizan para tratar el glaucoma, la acumulación excesiva de agua en los ojos. El bloqueo de esta enzima cambia el equilibrio de líquidos en los ojos para reducir la acumulación de líquido, aliviando así la presión. [2] [3]
La anhidrasa carbónica es fundamental para la función de la hemoglobina a través del efecto Bohr , que cataliza la hidratación del dióxido de carbono para formar ácido carbónico y disociarse rápidamente en agua. [4] Básicamente, un aumento del dióxido de carbono produce una reducción del pH de la sangre, lo que reduce la unión de oxígeno y hemoglobina . [5] Lo opuesto es cierto, donde una disminución en la concentración de dióxido de carbono aumenta el pH de la sangre, lo que aumenta la tasa de unión de oxígeno y hemoglobina. Relacionar el efecto Bohr con la anhidrasa carbónica es simple: la anhidrasa carbónica acelera la reacción del dióxido de carbono con el agua para producir iones de hidrógeno (protones) e iones de bicarbonato.
Para describir el equilibrio en la reacción de la anhidrasa carbónica, se utiliza el principio de Le Chatelier . La mayoría de los tejidos son más ácidos que el tejido pulmonar porque el dióxido de carbono se produce mediante la respiración celular en estos tejidos, donde reacciona con el agua para producir protones y bicarbonato. Como la concentración de dióxido de carbono es mayor, el equilibrio se desplaza hacia la derecha, hacia el lado del bicarbonato. Lo opuesto se observa en los pulmones, donde se libera dióxido de carbono, lo que reduce su concentración, por lo que el equilibrio se desplaza hacia la izquierda, lo que favorece la producción de dióxido de carbono. [6]
La anhidrasa carbónica fue aislada y caracterizada inicialmente a partir de glóbulos rojos en 1933, con informes simultáneos de Meldrum y Roughton (en la Universidad de Cambridge en el Reino Unido) y de Stadie y O'Brien (en la Universidad de Pensilvania en los Estados Unidos), [7] [8] ambos mientras buscaban un "factor catalítico... necesario para el tránsito rápido del HCO 3 - [anión bicarbonato] desde el eritrocito a... los capilares pulmonares". [9]
La anhidrasa carbónica desempeña un papel esencial en la regulación del pH de la sangre, lo que acelera la reacción CO2 + H2O HCO3- + H + para garantizar que el equilibrio se mantenga rápidamente. La reacción de equilibrio está influenciada por la proporción de bicarbonato y H + con respecto al dióxido de carbono. [10] El HCO3- es una base conjugada que neutraliza los ácidos, y el H + es un ácido conjugado que neutraliza las bases mediante la homeostasis ácido-base . El HCO3- y el H + son ideales para amortiguar el pH en la sangre y los tejidos porque el pKa está cerca del pH fisiológico = 7,2 – 7,6. Dado que el HCO3- y el H + se regulan en los riñones y el dióxido de carbono plasmático se regula en los pulmones, ambas acciones en los riñones y los pulmones son importantes para mantener la estabilidad del pH de la sangre. Por lo tanto, la anhidrasa carbónica ayuda a la secreción de H+ en el lumen del túbulo renal del riñón y a la reabsorción de HCO3- en los riñones. Además, ayuda al transporte de dióxido de carbono desde el tejido pulmonar hasta los alvéolos en el capilar pulmonar, donde el dióxido de carbono se excretará durante la exhalación. [10]
La anhidrasa carbónica es una enzima muy antigua que se encuentra en ambos dominios de los procariotas y que existe en seis clases diferentes entre la mayoría de los organismos vivos. [11] Estas familias no son similares en secuencia o estructura porque evolucionaron independientemente unas de otras, pero todas desarrollaron la misma estructura de sitio activo Zn 2+ , lo que muestra un gran ejemplo de evolución convergente. [ cita requerida ]
Una enzima es una sustancia que actúa como catalizador en los organismos vivos y que ayuda a acelerar las reacciones químicas. [12] La anhidrasa carbónica es una enzima importante que se encuentra en los glóbulos rojos, la mucosa gástrica, las células pancreáticas e incluso los túbulos renales. Se descubrió en el año 1932 y se ha clasificado en tres clases generales. [13] La clase uno es la anhidrasa carbónica alfa que se encuentra en los mamíferos, la clase dos es la anhidrasa carbónica beta que se encuentra en las bacterias y las plantas y, por último, la clase tres es la anhidrasa carbónica gamma que se encuentra en las bacterias metanógenas de las aguas termales. [14] Las tres clases de anhidrasa carbónica tienen el mismo sitio activo con un centro metálico de Zn; sin embargo, no son estructuralmente similares entre sí. La función principal de la anhidrasa carbónica en los seres humanos es catalizar la conversión de dióxido de carbono en ácido carbónico y viceversa. Sin embargo, también puede ayudar con el transporte de CO2 en la sangre, lo que a su vez ayuda a la respiración. Incluso puede funcionar en la formación de ácido clorhídrico por parte del estómago.[Cita requerida] Por lo tanto, el papel de la anhidrasa carbónica depende de dónde se encuentre en el cuerpo.
En la CA II de los mamíferos, el sitio activo consta de lo siguiente: un átomo de metal de ácido Lewis duro Zn +2 coordinado con residuos His -94, -96 y -119 separados 109˚ entre sí y un ion hidróxido (pKa = 6,8; 120° en configuración T d) , un bolsillo hidrofóbico adyacente al hidróxido unido a Zinc que consiste en Val-143 en su base y Val-121, Trp-209 y Leu-198 en su cuello, un residuo de transporte de protones (PSR) His-64 H + transporta H + dentro y fuera del sitio activo a través de un cambio conformacional, y una red de enlaces de hidrógeno que consiste en el grupo hidroxilo Thr-199 y el grupo carboxilo Glu-106 que estabiliza el hidróxido unido a Zinc al facilitar la orientación de las moléculas de agua en el lado activo a una configuración geométrica específica. La CA II tiene una frecuencia de recambio de 10 6 s −1 que es 10 7 veces más rápido que la reacción no catalizada.

La reacción que muestra la catalización de la anhidrasa carbónica en nuestros tejidos es
La catalización de la anhidrasa carbónica en los pulmones se demuestra mediante
La razón por la que las reacciones son en direcciones opuestas para los tejidos y los pulmones se debe a los diferentes niveles de pH que se encuentran en ellos. Sin el catalizador de anhidrasa carbónica, la reacción es muy lenta, sin embargo, con el catalizador, la reacción es 10 7 veces más rápida.
La reacción catalizada por la anhidrasa carbónica es
El ácido carbónico tiene un pKa de alrededor de 6,36 (el valor exacto depende del medio), por lo que a pH 7 un pequeño porcentaje del bicarbonato está protonado.
La anhidrasa carbónica es una de las enzimas más rápidas y su velocidad está limitada por la velocidad de difusión de sus sustratos . Las velocidades catalíticas típicas de las diferentes formas de esta enzima oscilan entre 10 4 y 10 6 reacciones por segundo. [15]
La reacción inversa no catalizada es relativamente lenta (la cinética es del orden de 15 segundos). Por eso, una bebida carbonatada no se desgasifica instantáneamente al abrir el envase; sin embargo, se desgasifica rápidamente en la boca cuando entra en contacto con la anhidrasa carbónica contenida en la saliva. [16]
Una anhidrasa se define como una enzima que cataliza la eliminación de una molécula de agua de un compuesto, y es esta reacción "inversa" la que le da a la anhidrasa carbónica su nombre, porque elimina una molécula de agua del ácido carbónico.
En los pulmones, la anhidrasa carbónica convierte el bicarbonato en dióxido de carbono, adecuado para la exhalación.
.jpg/440px-Active_site_of_CAII_(cropped).jpg)
El dióxido de carbono se transporta en la sangre en tres formas:
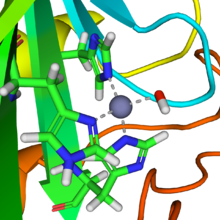

Un grupo prostético de zinc en la enzima está coordinado en tres posiciones por cadenas laterales de histidina . La cuarta posición de coordinación está ocupada por agua . Una cuarta histidina está cerca del ligando de agua, lo que facilita la formación del centro Zn-OH, que se une al CO2 para dar un bicarbonato de zinc. [18] El constructo es un ejemplo de catálisis general ácido-base general (consulte el artículo " Catálisis ácida "). El sitio activo también presenta un bolsillo adecuado para el dióxido de carbono, lo que lo acerca al grupo hidróxido. Los estudios cinéticos realizados determinan el siguiente mecanismo para la enzima: En los pasos 1 y 2, el nucleófilo O − en el ion hidróxido coordinado a Zn 2+ realiza un ataque nucleofílico en el carbono parcialmente electrofílico en la molécula de CO2 . Aquí el Zn 2+ actúa como un ácido de Lewis que reduce el pKa del ligando OH 2 coordinado de ~7-8 a 6,8 como T d , lo que impulsa la desprotonación del agua a un ion hidróxido y el protón libre es neutralizado por el tampón circundante. En el paso 3), se produce una transferencia de protones (H + ) desde el OH −1 al O − no coordinado en CO 3 −2 coordinado al átomo de Zn +2 en el sitio activo. A continuación, se libera un ion bicarbonato y el sitio catalítico se regenera a través de la unión de otra molécula de agua a cambio del ion bicarbonato. En el paso 4), el ligando de agua coordinado se desprotona facilitado por el Zn +2 para generar otro ion hidróxido para comenzar el ciclo nuevamente. [19] [20]

Se reconocen al menos cinco familias distintas de CA: α, β, γ, δ y ζ. Estas familias no tienen una similitud significativa en la secuencia de aminoácidos y en la mayoría de los casos se cree que son un ejemplo de evolución convergente . Las α-CA se encuentran en los seres humanos.
Los eucariotas, incluidos los vertebrados , las algas , las plantas y los hongos , así como algunas bacterias , contienen esta familia de CA.
Las enzimas CA que se encuentran en los mamíferos se dividen en cuatro grandes subgrupos, [ cita requerida ] que, a su vez, consisten en varias clases homólogas de genes:
Hay tres isoformas adicionales de la anhidrasa carbónica humana "acatalítica" ( CA-VIII , CA-X y CA-XI ) ( CA8 , CA10 , CA11 ) cuyas funciones siguen sin estar claras. [21]

La mayoría de las CA de los cloroplastos de procariotas y plantas pertenecen a la familia beta. Se han identificado dos patrones característicos para esta familia:
La clase gamma de CA proviene de los metanógenos , arqueas productoras de metano que crecen en fuentes termales.
La clase delta de CA se ha descrito en diatomeas . Sin embargo, recientemente [27] se ha puesto en tela de juicio la distinción entre esta clase de CA.
La clase zeta de CA se presenta exclusivamente en bacterias en unos pocos quimiolitotrofos y cianobacterias marinas que contienen carboxisomas cso . [28] Análisis tridimensionales recientes [27] sugieren que ζ-CA tiene cierta semejanza estructural con β-CA, particularmente cerca del sitio del ion metálico. Por lo tanto, las dos formas pueden estar distantemente relacionadas, aunque la secuencia de aminoácidos subyacente ha divergido considerablemente desde entonces.
Recientemente se ha descubierto la familia eta de enzimas en organismos del género Plasmodium . Se trata de un grupo de enzimas que anteriormente se creía que pertenecían a la familia alfa de enzimas, pero se ha demostrado que las η-CA tienen características únicas, como su patrón de coordinación de iones metálicos. [29]
La clase iota es la clase de CA descrita más recientemente. Se ha descubierto en la diatomea marina Thalassiosira pseudonana y está muy extendida entre el fitoplancton marino. [30] En las diatomeas, la ι-CA es esencial para los mecanismos de concentración de CO 2 y, a diferencia de otras clases de CA, puede utilizar manganeso en lugar de zinc como cofactor metálico. [30] También se han confirmado homólogos de la ι-CA en bacterias gramnegativas, donde puede estar presente como un homodímero proteico. [31]
Existen varias formas de anhidrasa carbónica en la naturaleza. En la forma de anhidrasa α-carbónica mejor estudiada , presente en animales, el ion zinc está coordinado por los anillos de imidazol de tres residuos de histidina , His94, His96 e His119. [32]
La función principal de la enzima en los animales es interconvertir el dióxido de carbono y el bicarbonato para mantener el equilibrio ácido-base en la sangre y otros tejidos, y ayudar a transportar el dióxido de carbono fuera de los tejidos.
Existen al menos 14 isoformas diferentes en los mamíferos. Las plantas contienen una forma diferente llamada anhidrasa β-carbónica , que, desde un punto de vista evolutivo, es una enzima distinta, pero participa en la misma reacción y también utiliza un ion de zinc en su sitio activo. En las plantas, la anhidrasa carbónica ayuda a aumentar la concentración de CO 2 dentro del cloroplasto para aumentar la tasa de carboxilación de la enzima RuBisCO . Esta es la reacción que integra el CO 2 en los azúcares de carbono orgánico durante la fotosíntesis , y puede utilizar solo la forma CO 2 del carbono, no el ácido carbónico ni el bicarbonato. [ cita requerida ]
Se ha descubierto que las diatomeas marinas expresan una nueva forma de anhidrasa carbónica ζ. Se descubrió que T. weissflogii , una especie de fitoplancton común en muchos ecosistemas marinos, contiene anhidrasa carbónica con un ion cadmio en lugar de zinc. [33] Anteriormente, se creía que el cadmio era un metal tóxico sin ninguna función biológica. Sin embargo, esta especie de fitoplancton parece haberse adaptado a los bajos niveles de zinc en el océano utilizando cadmio cuando no hay suficiente zinc. [34] Aunque la concentración de cadmio en el agua de mar también es baja (alrededor de 1x10 −16 molar ), existe una ventaja ambiental al poder usar cualquiera de los dos metales dependiendo de cuál esté más disponible en ese momento. Por lo tanto, este tipo de anhidrasa carbónica es cambialista, lo que significa que puede intercambiar el metal en su sitio activo con otros metales (a saber, zinc y cadmio). [35]
El mecanismo de la anhidrasa carbónica de cadmio (CDCA) es esencialmente el mismo que el de otras anhidrasas carbónicas en su conversión de dióxido de carbono y agua en bicarbonato y un protón. [36] Además, al igual que las otras anhidrasas carbónicas, la CDCA hace que la reacción sea casi tan rápida como la velocidad de difusión de sus sustratos, y puede ser inhibida por derivados de sulfonamida y sulfamato . [36]
A diferencia de la mayoría de las otras anhidrasas carbónicas, el ion metálico del sitio activo no está unido por tres residuos de histidina y un ion hidróxido. En cambio, está unido por dos residuos de cisteína , un residuo de histidina y un ion hidróxido, lo cual es característico de la β-CA. [36] [37] Debido al hecho de que el cadmio es un ácido blando , estará más fuertemente unido por ligandos de base blanda . [35] Los átomos de azufre en los residuos de cisteína son bases blandas, por lo que se unen al cadmio con más fuerza que el nitrógeno en los residuos de histidina. La CDCA también tiene una estructura de plegamiento tridimensional que es diferente a cualquier otra anhidrasa carbónica, y su secuencia de aminoácidos es diferente a las otras anhidrasas carbónicas. [36] Es un monómero con tres dominios, cada uno idéntico en secuencia de aminoácidos y cada uno conteniendo un sitio activo con un ion metálico. [37]
Otra diferencia clave entre la CDCA y las otras anhidrasas carbónicas es que la CDCA tiene un mecanismo para cambiar su ion cadmio por un ion zinc en caso de que el zinc se vuelva más disponible para el fitoplancton que el cadmio. El sitio activo de la CDCA está esencialmente "cerrado" por una cadena de nueve aminoácidos con residuos de glicina en las posiciones 1 y 9. Normalmente, esta compuerta permanece cerrada y el ion cadmio queda atrapado en su interior. Sin embargo, debido a la flexibilidad y la posición de los residuos de glicina, esta compuerta se puede abrir para eliminar el ion cadmio. Entonces se puede poner un ion zinc en su lugar y la compuerta se cerrará detrás de él. [36] Como ácido limítrofe , el zinc no se unirá tan firmemente a los ligandos de cisteína como lo haría el cadmio, pero la enzima seguirá siendo activa y razonablemente eficiente. El metal en el sitio activo se puede cambiar entre zinc y cadmio dependiendo de cuál sea más abundante en ese momento. Es la capacidad del CDCA de utilizar cadmio o zinc lo que probablemente le da a T. weissflogii una ventaja de supervivencia. [34]
El cadmio todavía se considera letal para el fitoplancton en grandes cantidades. Los estudios han demostrado que T. weissflogii tiene una respuesta tóxica inicial al cadmio cuando se expone a él. La toxicidad del metal se reduce mediante la transcripción y traducción de la fitoquelatina , que son proteínas que pueden unirse y transportar el cadmio. Una vez unido por la fitoquelatina, el cadmio ya no es tóxico y puede transportarse de forma segura a la enzima CDCA. [33] También se ha demostrado que la absorción de cadmio a través de la fitoquelatina conduce a un aumento significativo en la expresión de CDCA. [33]
Se han analizado otros fitoplancton de diferentes fuentes de agua para detectar la presencia de CDCA. Se encontró que muchos de ellos contienen proteínas homólogas a la CDCA encontrada en T. weissflogii . [33] Esto incluye especies de Great Bay, Nueva Jersey , así como del Océano Pacífico cerca del ecuador . En todas las especies analizadas, las proteínas similares a CDCA mostraron altos niveles de expresión incluso en altas concentraciones de zinc y en ausencia de cadmio. [33] La similitud entre estas proteínas y la CDCA expresada por T. weissflogii varió, pero siempre fueron al menos un 67% similares. [33]
En principio, la anhidrasa carbónica podría resultar relevante para la captura de carbono . Algunas anhidrasas carbónicas pueden soportar temperaturas de hasta 107 °C y una alcalinidad extrema (pH > 10). [38] Una prueba piloto con la CA más estable en una corriente de humos que consistía en una composición molar de 12-13% de CO₂ tuvo una tasa de captura del 63,6% durante un período de 60 horas sin efectos notables en el rendimiento de la enzima. La CA se colocó en una solución de N-metildietanolamina (MDEA) donde sirvió para aumentar la diferencia de concentración (fuerza impulsora) de CO 2 entre la corriente de humos de la planta de energía y la fase líquida en un contactor líquido-gas. [38]