Una infección adquirida en un hospital , también conocida como infección nosocomial (del griego nosokomeion , que significa "hospital"), es una infección que se adquiere en un hospital u otro centro de atención médica . [1] Para enfatizar tanto en entornos hospitalarios como no hospitalarios, a veces se le llama infección asociada a la atención médica . [2] Dicha infección se puede adquirir en un hospital, residencia de ancianos , centro de rehabilitación , clínica ambulatoria, laboratorio de diagnóstico u otros entornos clínicos. Varios procesos dinámicos pueden provocar contaminación en los quirófanos y otras áreas dentro de entornos hospitalarios. [3] [4] La infección se transmite al paciente susceptible en el entorno clínico por diversos medios. El personal sanitario también propaga infecciones, además de equipos, ropa de cama o gotitas de aire contaminadas. La infección puede originarse en el entorno exterior, en otro paciente infectado, en el personal que puede estar infectado o, en algunos casos, no se puede determinar la fuente de la infección. En algunos casos el microorganismo se origina a partir de la propia microbiota cutánea del paciente , volviéndose oportunista tras una cirugía u otros procedimientos que comprometan la barrera protectora de la piel. Aunque el paciente puede haber contraído la infección a través de su propia piel, la infección aún se considera nosocomial ya que se desarrolla en el entorno de atención médica. [5] La infección nosocomial tiende a carecer de evidencia de que estaba presente cuando el paciente ingresó al entorno de atención médica, lo que significa que se adquirió después del ingreso. [5] [6]
Durante 2002, en Estados Unidos, los Centros para el Control y la Prevención de Enfermedades estimaron que aproximadamente 1,7 millones de infecciones asociadas a la atención sanitaria, causadas por todo tipo de microorganismos , incluidas bacterias y hongos combinados, causaron o contribuyeron a 99.000 muertes. [7] En Europa , donde se han realizado encuestas hospitalarias , se estima que la categoría de infecciones por gramnegativos representa dos tercios de las 25.000 muertes cada año. [8] Las infecciones nosocomiales pueden causar neumonía grave e infecciones del tracto urinario , el torrente sanguíneo y otras partes del cuerpo. [9] [10] Muchos tipos muestran resistencia a los antimicrobianos , lo que puede complicar el tratamiento . [11]
En el Reino Unido, alrededor de 300.000 pacientes se vieron afectados en 2017, y se estimó que esto le costó al NHS alrededor de mil millones de libras esterlinas al año. [12]
Recientemente se han identificado catéteres permanentes en infecciones adquiridas en hospitales. [14] Para tratar esta complicación, se utilizan procedimientos, llamados terapia de bloqueo antimicrobiano intravascular , que pueden reducir las infecciones que no están expuestas a antibióticos transmitidos por la sangre. [15] La introducción de antibióticos, incluido el etanol, en el catéter (sin lanzarlo al torrente sanguíneo) reduce la formación de biopelículas. [13]
La transmisión por contacto se divide en dos subgrupos: transmisión por contacto directo y transmisión por contacto indirecto.
Además de reducir los vectores de transmisión, es necesario considerar la susceptibilidad de los pacientes a las infecciones adquiridas en el hospital. Los factores que hacen que los pacientes tengan un mayor riesgo de infecciones incluyen:
Dada la asociación entre los dispositivos invasivos y las infecciones adquiridas en hospitales, se utilizan términos específicos para delimitar dichas infecciones y permitir su seguimiento y prevención. Las infecciones asociadas a dispositivos observadas incluyen neumonía asociada a ventiladores , infecciones del torrente sanguíneo asociadas a catéteres, infecciones del tracto urinario asociadas a catéteres y ventriculitis asociada a dispositivos . La vigilancia de estas infecciones la llevan a cabo e informan habitualmente organismos como el Centro Europeo para la Prevención y el Control de Enfermedades y los Centros para el Control y la Prevención de Enfermedades . [ cita necesaria ]

Controlar la infección nosocomial implica implementar medidas de control de calidad en los sectores de atención médica , y la gestión basada en evidencia puede ser un enfoque factible. Para aquellos con neumonía asociada a ventilador o adquirida en el hospital, el control y monitoreo de la calidad del aire interior del hospital debe estar en la agenda del manejo, [21] mientras que para la infección nosocomial por rotavirus , se debe aplicar un protocolo de higiene de manos . [22] [23] [24]
Para reducir la cantidad de infecciones adquiridas en hospitales, el estado de Maryland implementó el Programa de Condiciones Adquiridas en Hospitales de Maryland que ofrece recompensas y sanciones financieras para hospitales individuales. Una adaptación de la política de pago de los Centros de Servicios de Medicare y Medicaid hace que los hospitales con bajo rendimiento pierdan hasta el 3% de sus ingresos por pacientes hospitalizados, mientras que los hospitales que pueden reducir las infecciones adquiridas en hospitales pueden ganar hasta el 3% en recompensas. Durante los primeros dos años del programa, las tasas de complicaciones cayeron un 15,26% en todas las enfermedades adquiridas en hospitales rastreadas por el estado (incluidas las no cubiertas por el programa), desde una tasa de complicaciones ajustada por riesgo de 2,38 por cada 1.000 personas en 2009 a una tasa de 2,02 en 2011. La disminución del 15,26% se traduce en más de $100 millones en ahorros de costos para el sistema de atención médica en Maryland, y los mayores ahorros provienen de evitar infecciones del tracto urinario, sepsis y otras infecciones graves, y neumonía y otras infecciones pulmonares. . Si se pudieran lograr resultados similares en todo el país, el programa Medicare ahorraría aproximadamente 1.300 millones de dólares en dos años, mientras que el sistema de atención sanitaria estadounidense en su conjunto ahorraría 5.300 millones de dólares. [25]
Los hospitales cuentan con protocolos de sanidad en cuanto a uniformes , esterilización de equipos , lavado y otras medidas preventivas. El lavado minucioso de manos y/o el uso de desinfectantes con alcohol por parte de todo el personal médico antes y después de cada contacto con un paciente es una de las formas más efectivas de combatir las infecciones nosocomiales. [26] También se considera vital un uso más cuidadoso de agentes antimicrobianos , como los antibióticos . [27] Como muchas infecciones adquiridas en hospitales causadas por bacterias como Staphylococcus aureus resistente a la meticilina, Staphylococcus aureus sensible a la meticilina y Clostridium difficile son causadas por un incumplimiento de estos protocolos, es común que los pacientes afectados presenten demandas por negligencia médica contra el hospital en cuestión. [28]
La desinfección de superficies es parte de las medidas de control para reducir las infecciones nosocomiales en los entornos sanitarios. Los métodos de desinfección modernos, como el vapor de alcohol no inflamable en sistemas de dióxido de carbono, han sido eficaces contra la gastroenteritis, el Staphylococcus aureus resistente a la meticilina y los agentes gripales. Se ha demostrado clínicamente que el uso de vapor de peróxido de hidrógeno reduce las tasas de infección y el riesgo de adquisición. El peróxido de hidrógeno es eficaz contra las bacterias formadoras de endosporas, como Clostridium difficile , donde se ha demostrado que el alcohol es ineficaz. [29] [ fuente no primaria necesaria ] También se pueden usar dispositivos de limpieza ultravioleta para desinfectar las habitaciones de pacientes infectados con Clostridium difficile o Staphylococcus aureus resistente a meticilina después del alta. [30] [ se necesita fuente no primaria ]
A pesar del protocolo sanitario, no se puede aislar completamente a los pacientes de los agentes infecciosos. Además, a los pacientes a menudo se les recetan antibióticos y otros medicamentos antimicrobianos para ayudar a tratar la enfermedad; esto puede aumentar la presión de selección para la aparición de cepas resistentes. [31]
La esterilización va más allá de la simple higienización. Mata todos los microorganismos en equipos y superficies mediante la exposición a productos químicos, radiación ionizante, calor seco o vapor bajo presión. [32]
El aislamiento es la implementación de precauciones de aislamiento diseñadas para prevenir la transmisión de microorganismos por rutas comunes en los hospitales. (Ver Precauciones universales y Precauciones basadas en la transmisión ). Debido a que los factores del agente y del huésped son más difíciles de controlar, la interrupción de la transferencia de microorganismos está dirigida principalmente a la transmisión, por ejemplo, el aislamiento de casos infecciosos en hospitales especiales y el aislamiento de pacientes con heridas infectadas en hospitales especiales. Salas también aislamiento de pacientes con trasplante de articulaciones en salas específicas. [ cita necesaria ]
Con frecuencia se considera que el lavado de manos es la medida más importante para reducir los riesgos de transmisión de microorganismos cutáneos de una persona a otra o de un sitio a otro en el mismo paciente. Lavarse las manos lo más rápida y minuciosamente posible entre contactos con pacientes y después del contacto con sangre , fluidos corporales , secreciones , excreciones y equipos o artículos contaminados por ellos es un componente importante del control de infecciones y las precauciones de aislamiento. La propagación de infecciones nosocomiales entre pacientes inmunocomprometidos está relacionada con la contaminación de las manos de los trabajadores sanitarios en casi el 40% de los casos y es un problema difícil en los hospitales modernos. La mejor manera para que los trabajadores superen este problema es realizar procedimientos correctos de higiene de manos; Esta es la razón por la que la OMS lanzó en 2005 el Desafío GLOBAL por la Seguridad del Paciente. [33]
En las manos de los trabajadores de la salud pueden estar presentes dos categorías de microorganismos: flora transitoria y flora residente. El primero está representado por los microorganismos que los trabajadores extraen del medio ambiente, y las bacterias que contiene son capaces de sobrevivir en la piel humana y, a veces, de crecer. El segundo grupo está representado por los microorganismos permanentes que viven en la superficie de la piel (en el estrato córneo o inmediatamente debajo de él). Son capaces de sobrevivir en la piel humana y crecer libremente sobre ella. Tienen baja patogenicidad y tasa de infección, y crean una especie de protección contra la colonización de otras bacterias más patógenas. La piel de las obreras está colonizada por 3,9 × 10 4 – 4,6 × 10 6 ufc /cm 2 . Los microbios que componen la flora residente son: Staphylococcus epidermidis , Staphylococcus hominis y Microccocus , Propionibacterium , Corynebacterium , Dermobacterium y Pitosporum spp., mientras que los organismos transitorios son Staphylococcus aureus y Klebsiella pneumoniae , y Acinetobacter, Enterobacter y Candida spp. El objetivo de la higiene de manos es eliminar la flora transitoria mediante una cuidadosa y adecuada realización del lavado de manos, utilizando diferentes tipos de jabón (normal y antiséptico) y geles a base de alcohol. Los principales problemas encontrados en la práctica de la higiene de manos están relacionados con la falta de lavabos disponibles y el lento lavado de manos. Una forma sencilla de resolver este problema podría ser el uso de desinfectantes para manos a base de alcohol, debido a que su aplicación es más rápida en comparación con el lavado de manos correcto. [34]
También se ha demostrado que mejorar el lavado de manos de los pacientes reduce la tasa de infección nosocomial. Los pacientes que están postrados en cama a menudo no tienen tanto acceso para lavarse las manos a la hora de comer o después de tocar superficies o manipular desechos como pañuelos de papel. Al reforzar la importancia del lavado de manos y proporcionar gel o toallitas desinfectantes al alcance de la cama, las enfermeras pudieron reducir directamente las tasas de infección. Un estudio publicado en 2017 demostró esto al mejorar la educación del paciente sobre el procedimiento adecuado de lavado de manos y los momentos importantes para usar desinfectante y redujo con éxito la tasa de enterococos y Staphylococcus aureus . [35]
Todos los visitantes deben seguir los mismos procedimientos que el personal del hospital para controlar adecuadamente la propagación de infecciones. Además, las infecciones multirresistentes pueden salir del hospital y pasar a formar parte de la flora comunitaria si no se toman medidas para detener esta transmisión. [ cita necesaria ]
No está claro si el esmalte de uñas o los anillos afectaron las tasas de infección de las heridas quirúrgicas. [36]
Además del lavado de manos, los guantes juegan un papel importante a la hora de reducir los riesgos de transmisión de microorganismos. Los guantes se usan por tres razones importantes en los hospitales. En primer lugar, se usan para proporcionar una barrera protectora para el personal, evitando la contaminación a gran escala de las manos al tocar sangre, fluidos corporales, secreciones, excreciones, membranas mucosas y piel no intacta. En los Estados Unidos, la Administración de Salud y Seguridad Ocupacional exige el uso de guantes para reducir el riesgo de infecciones por patógenos transmitidos por la sangre . [37] En segundo lugar, se usan guantes para reducir la probabilidad de que los microorganismos presentes en las manos del personal se transmitan a los pacientes durante procedimientos invasivos u otros procedimientos de atención al paciente que implican tocar las membranas mucosas y la piel no intacta del paciente. En tercer lugar, se usan para reducir la probabilidad de que las manos del personal contaminadas con microorganismos de un paciente o un fómite puedan transmitir esos microorganismos a otro paciente. En esta situación, se deben cambiar los guantes entre contactos con pacientes y se deben lavar las manos después de quitarse los guantes. [ cita necesaria ]
Se sabe que los microorganismos sobreviven en superficies inanimadas que se tocan durante largos períodos de tiempo. [38] [39] Esto puede ser especialmente problemático en entornos hospitalarios donde los pacientes inmunodeficientes tienen un mayor riesgo de contraer infecciones nosocomiales. Los pacientes con infecciones nosocomiales son hospitalizados predominantemente en diferentes tipos de unidades de cuidados intensivos (UCI). [40]
Superficies táctiles que se encuentran comúnmente en las habitaciones de los hospitales, como barandillas de camas, botones de llamada, placas táctiles, sillas, manijas de puertas, interruptores de luz, barras de apoyo, postes intravenosos, dispensadores (gel de alcohol, toallas de papel, jabón), carritos para vestirse y mostradores. Se sabe que las superficies de las mesas están contaminadas con Staphylococcus , Staphylococcus aureus resistente a la meticilina (una de las cepas más virulentas de bacterias resistentes a los antibióticos) y Enterococcus resistente a la vancomicina . [41] Los objetos más cercanos a los pacientes tienen los niveles más altos de Staphylococcus aureus resistente a la meticilina y Enterococcus resistente a la vancomicina . Esta es la razón por la que las superficies táctiles en las habitaciones de los hospitales pueden servir como fuentes o reservorios para la propagación de bacterias de las manos de los trabajadores de la salud y de los visitantes de los pacientes. [42]
Varios compuestos pueden disminuir el riesgo de que crezcan bacterias en las superficies, entre ellos: cobre , plata y germicidas . [43]
Se han realizado varios estudios que evalúan el uso de sistemas de limpieza sin contacto, en particular el uso de dispositivos ultravioleta C. Una revisión no fue concluyente debido a la falta de evidencia o a su mala calidad. [44] Otras revisiones han encontrado cierta evidencia, y cada vez más, de su eficacia. [45] [46]
Dos de las especies de bacterias con mayor probabilidad de infectar a los pacientes son las cepas Gram positivas de Staphylococcus aureus resistente a la meticilina y las Gram negativas de Acinetobacter baumannii . Si bien se encuentran disponibles antibióticos para tratar enfermedades causadas por Staphylococcus aureus resistente a la meticilina , hay pocos medicamentos efectivos disponibles para Acinetobacter . Las bacterias Acinetobacter están evolucionando y volviéndose inmunes a los antibióticos, por lo que en muchos casos es necesario utilizar antibacterianos del tipo polimixina . "En muchos aspectos es mucho peor que el MRSA", afirma un especialista de la Universidad Case Western Reserve . [47]
Otra enfermedad creciente, especialmente prevalente en los hospitales de la ciudad de Nueva York , es la Klebsiella pneumoniae gramnegativa, resistente a los medicamentos . Se estima que más del 20% de las infecciones por Klebsiella en los hospitales de Brooklyn "son ahora resistentes a prácticamente todos los antibióticos modernos, y esos supergérmenes se están propagando por todo el mundo". [47]
Las bacterias, clasificadas como Gram negativas debido a su color en la tinción de Gram , pueden causar neumonía grave e infecciones del tracto urinario , el torrente sanguíneo y otras partes del cuerpo. Sus estructuras celulares los hacen más difíciles de atacar con antibióticos que los organismos grampositivos como el Staphylococcus aureus resistente a la meticilina . En algunos casos, la resistencia a los antibióticos se está propagando a bacterias gramnegativas que pueden infectar a personas fuera del hospital. "Para los grampositivos necesitamos mejores medicamentos; para los gramnegativos necesitamos cualquier medicamento", dijo Brad Spellberg, especialista en enfermedades infecciosas del Centro Médico Harbor-UCLA y autor de Rising Plague , un libro sobre patógenos resistentes a los medicamentos. . [47]
La neumonía adquirida en el hospital (NHA) es la segunda infección nosocomial más común y representa aproximadamente una cuarta parte de todas las infecciones en la unidad de cuidados intensivos (UCI). [48] La HAP, o neumonía nosocomial, es una infección de las vías respiratorias inferiores que no se encontraba en incubación en el momento del ingreso hospitalario y que se presenta clínicamente dos o más días después de la hospitalización. [49] La neumonía asociada al ventilador (NAV) se define como HAP en pacientes que reciben ventilación mecánica. La incidencia de VAP es de 10 a 30% entre los pacientes que requieren ventilación mecánica durante >48 h. [50] Un protocolo de tratamiento estándar se basa en definiciones de diagnóstico precisas, confirmación microbiológica de NAV y la administración de imipenem más ciprofloxacina como tratamiento antibiótico empírico inicial. [51]
Un tercio de las infecciones nosocomiales se consideran prevenibles. Los CDC estiman que 687.000 personas en Estados Unidos resultaron infectadas por infecciones adquiridas en hospitales en 2015, lo que provocó 72.000 muertes. [52] Las infecciones nosocomiales más comunes son las del tracto urinario , el sitio quirúrgico y diversas neumonías . [7]
Un tratamiento alternativo dirigido a infecciones localizadas es el uso de irradiación ultravioleta C. [53]
Los métodos utilizados difieren de un país a otro (definiciones utilizadas, tipo de infecciones nosocomiales cubiertas, unidades de salud encuestadas, inclusión o exclusión de infecciones importadas, etc.), por lo que las comparaciones internacionales de las tasas de infecciones nosocomiales deben realizarse con sumo cuidado. [ cita necesaria ]
En Bélgica, la prevalencia de infecciones nosocomiales es de alrededor del 6,2%. Anualmente unos 125.500 pacientes resultan infectados por una infección nosocomial, lo que provoca casi 3.000 muertes. Los costes adicionales del seguro médico se estiman en aproximadamente 400 millones de euros al año. [54]
Las estimaciones oscilaron entre el 6,7% en 1990 y el 7,4% (los pacientes pueden tener varias infecciones). [55] A nivel nacional, la prevalencia entre los pacientes en centros de atención de salud fue del 6,7% en 1996, [56] del 5,9% en 2001 [57] y del 5,0% en 2006. [58] Las tasas de infecciones nosocomiales fueron del 7,6% en 1996, 6,4% en 2001 y 5,4% en 2006. [ cita necesaria ]
En 2006, los sitios de infección más comunes fueron infecciones del tracto urinario (30,3%), neumopatía (14,7%), infecciones del sitio de la cirugía (14,2%). Infecciones de la piel y mucosas (10,2%), otras infecciones respiratorias (6,8%) e infecciones bacterianas/intoxicaciones sanguíneas (6,4%). [59] Las tasas entre pacientes adultos en cuidados intensivos fueron del 13,5% en 2004, el 14,6% en 2005, el 14,1% en 2006 y el 14,4% en 2007. [60]
Se estima que las infecciones nosocomiales hacen que los pacientes permanezcan en el hospital entre cuatro y cinco días más. Alrededor de 2004-2005, unas 9.000 personas morían cada año a causa de una infección nosocomial, de las cuales unas 4.200 habrían sobrevivido sin esta infección. [61]
La tasa se estimó en 8,5% de los pacientes en 2005. [62]
Desde el año 2000, las estimaciones muestran una tasa de infección del 6,7%, es decir, entre 450.000 y 700.000 pacientes, lo que provocó entre 4.500 y 7.000 muertes. [63] Una encuesta realizada en Lombardía arrojó una tasa del 4,9% de pacientes en 2000. [64]
Las estimaciones oscilan entre el 2 y el 14%. [65] Una encuesta nacional arrojó una tasa del 7,2 por ciento en 2004. [66]
En 2012, la Agencia de Protección de la Salud informó que la tasa de prevalencia de infecciones adquiridas en hospitales en Inglaterra fue del 6,4% en 2011, frente a una tasa del 8,2% en 2006, [67] siendo las infecciones del tracto respiratorio , del tracto urinario y del sitio quirúrgico los tipos más comunes. de infecciones reportadas. [67] En 2018, se informó que las infecciones hospitalarias habían aumentado de 5.972 en 2008 a 48.815 en 2017. [68]
Los Centros para el Control y la Prevención de Enfermedades (CDC) estimaron que aproximadamente 1,7 millones de infecciones asociadas a hospitales, de todo tipo de bacterias combinadas, causan o contribuyen a 99.000 muertes cada año. [69] Otras estimaciones indican que el 10%, o 2 millones, de pacientes al año se infectan, con un coste anual que oscila entre 4.500 y 11.000 millones de dólares. [70] En los EE. UU., el tipo más frecuente de infección hospitalaria es la infección del tracto urinario (36%), seguida de la infección del sitio quirúrgico (20%) y la infección del torrente sanguíneo y la neumonía (ambas 11%). [47] [ necesita actualización ]
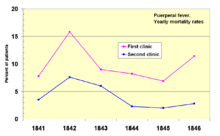
En 1841, Ignaz Semmelweis , un obstetra húngaro , trabajaba en una maternidad de Viena. Se mostró "conmocionado" por la tasa de mortalidad de las mujeres que desarrollaron fiebre puerperal . Documentó que la mortalidad era tres veces mayor en la sala donde las estudiantes de medicina daban a luz que en la sala contigua atendida por estudiantes de partería . [71] Los estudiantes de medicina también trabajaban habitualmente con cadáveres . Comparó las tasas de infección con las de un hospital similar en Dublín, Irlanda , y planteó la hipótesis de que eran los estudiantes de medicina quienes de alguna manera infectaban a las mujeres después del parto. Instituyó el lavado de manos obligatorio en mayo de 1847 y las tasas de infección disminuyeron drásticamente. Louis Pasteur propuso la teoría de los gérmenes de las enfermedades y comenzó su trabajo sobre el cólera en 1865 identificando que eran microorganismos los que estaban asociados con las enfermedades . [72] [73]