
Los antagonistas de los receptores adrenérgicos β (también llamados betabloqueantes o β-bloqueantes) se desarrollaron inicialmente en la década de 1960, para el tratamiento de la angina de pecho, pero ahora también se utilizan para la hipertensión , la insuficiencia cardíaca congestiva y ciertas arritmias . [1] En la década de 1950, se descubrió que el dicloroisoproterenol (DCI) era un β-antagonista que bloqueaba los efectos de las aminas simpaticomiméticas sobre la broncodilatación, la relajación uterina y la estimulación cardíaca. Aunque el DCI no tenía utilidad clínica, un cambio en el compuesto proporcionó un candidato clínico, el pronetalol , que se introdujo en 1962. [2]

Los betabloqueantes son una clase de fármacos de enorme importancia debido a su alta prevalencia de uso. El descubrimiento de los betabloqueantes se remonta a hace más de 100 años, cuando los primeros investigadores idearon la idea de que las catecolaminas se unían selectivamente a estructuras similares a receptores y que esta era la causa de sus acciones farmacológicas . [3] En 1948, Raymond P. Ahlquist publicó un artículo seminal en el que concluía sus hallazgos: que existían dos receptores distintos para los fármacos catecolámicos y que causaban respuestas diferentes en el músculo cardíaco . Los denominó adrenoceptores α y β. Estos hallazgos pronto serían la base para futuras investigaciones en el desarrollo de fármacos . [4]
A principios de la década de 1960, James Black , un farmacólogo escocés , y sus asociados en la Imperial Chemical Industries (ICI) en Gran Bretaña estaban trabajando en una serie de compuestos bloqueadores β-adrenérgicos , pronethalol y propranolol . El Dr. Black se centró en el desarrollo de un fármaco que aliviara el dolor de la angina de pecho , que resulta de la falta de oxígeno en el corazón. Su plan era crear un fármaco que disminuyera el requerimiento de oxígeno del corazón. Planteó la hipótesis de que estos compuestos reducirían el consumo de oxígeno del corazón al interferir con los efectos de las catecolaminas. [4] En 1958, se describieron las propiedades farmacológicas del dicloroisoproterenol (DCI), un β-antagonista descubierto unos años antes por el grupo de Eli Lilly. [2] Fue la síntesis de DCI la que estableció que los receptores β podían bloquearse químicamente y, por lo tanto, se pudo confirmar su existencia. [5] El DCI no tenía utilidad clínica, pero un reemplazo de los sustituyentes 3,4-dicloro, con un puente de carbono para formar un derivado de naftiletanolamina, proporcionó un candidato clínico, el pronetalol. [2]
En abril de 1963, las pruebas de toxicidad del pronetalol mostraron resultados de tumores tímicos en ratones. Sin embargo, se lanzó bajo el nombre comercial Alderlin, como el primer betabloqueante clínicamente útil. El lanzamiento tuvo lugar en noviembre de 1963, cuando muchos ensayos clínicos a pequeña escala habían demostrado su eficacia en la angina y ciertos tipos de arritmias. El pronetalol solo se comercializó para su uso en situaciones que amenazaban la vida. El Dr. James Black pasó a crear otro betabloqueante, llamado propranolol ; un betabloqueante no selectivo . Los ensayos clínicos comenzaron en el verano de 1964 y un año después, el propranolol se lanzó bajo el nombre comercial Inderal , solo dos años y medio después de haber sido probado por primera vez. [4] Resultó tener una mayor potencia que el pronetalol, con menos efectos secundarios . [6] El propranolol se convirtió en el primer fármaco importante en el tratamiento de la angina de pecho , desde la introducción de los vasodilatadores coronarios (como la nitroglicerina ), casi 100 años antes. El propranolol se convirtió en un fármaco de gran éxito, utilizado para tratar una amplia gama de enfermedades cardiovasculares como la arritmia, la hipertensión y la miocardiopatía hipertrófica . [4] [7]
Cuando se lanzó el propranolol, ICI estaba empezando a experimentar la competencia de otras compañías. Esta amenaza potencial llevó a continuos refinamientos en la estructura farmacológica de los betabloqueantes y posteriores avances en la administración de fármacos . ICI estudió análogos más a fondo y en 1970 lanzó practolol ( figura 4 ) bajo el nombre comercial Eraldin. Fue retirado del mercado unos años más tarde debido a los graves efectos secundarios que causaba, sin embargo jugó un papel importante en el estudio fundamental del betabloqueante y los betareceptores. [4] La retirada de Eraldin dio a ICI el empujón para lanzar otro betabloqueante, atenolol , que se lanzó en 1976 bajo el nombre comercial Tenormin. El atenolol es un antagonista selectivo del receptor β1 y fue desarrollado con el propósito de obtener el "betabloqueante ideal". Pronto se convirtió en uno de los fármacos cardíacos más vendidos . [4] El proyecto de ICI sobre los betabloqueantes se basó en la teoría de los receptores duales de Ahlquist. Los fármacos que surgieron de este proyecto, desde el propranolol hasta el atenolol, ayudaron a establecer la teoría de los receptores entre los científicos y las compañías farmacéuticas. [4] [6]
El progreso en el desarrollo de betabloqueantes condujo a la introducción de fármacos con una variedad de propiedades. Se desarrollaron betabloqueantes que tenían una selectividad relativa para los receptores β1 cardíacos (por ejemplo, metoprolol y atenolol), actividad agonista adrenérgica parcial ( pindolol ), actividad de bloqueo α-adrenérgico concomitante (por ejemplo, labetalol y carvedilol ) y actividad vasodilatadora directa adicional ( nebivolol ). Además, se desarrollaron formulaciones de acción prolongada y ultracorta de betabloqueantes. [7] En 1988, Sir James Black recibió el Premio Nobel de Medicina por su trabajo en el desarrollo de fármacos. [3] [4] [6] [7]
Todos los antagonistas de los receptores β-adrenérgicos tienen acciones terapéuticas y farmacodinámicas similares en pacientes con trastornos cardiovasculares. Varían mucho en sus propiedades farmacocinéticas , ya que demuestran un amplio rango de valores en la unión a proteínas plasmáticas , el porcentaje de fármaco eliminado por metabolismo o sin cambios en la orina y la relación de extracción hepática . [7] [8] Cada uno de los β-bloqueantes posee al menos un centro quiral y un alto grado de enantioselectividad al unirse al receptor β-adrenérgico. Para aquellos β-bloqueantes que contienen un solo centro quiral , el enantiómero (-) tiene una afinidad mucho mayor en la unión al receptor β-adrenérgico que el enantiómero (+). Todos los β-bloqueantes utilizados sistémicamente se administran como racemato , excepto el timolol . [8]

Se han identificado tres tipos diferentes de receptores β-adrenérgicos mediante farmacología molecular. Los receptores β1 se encuentran en el corazón y constituyen aproximadamente el 75% de todos los receptores β. Los receptores β2 se pueden encontrar en los músculos lisos de los vasos y los bronquios. Se presume que los receptores β3 están involucrados en el metabolismo de los ácidos grasos y se encuentran en los adipocitos . [10] Los β-bloqueantes causan una inhibición competitiva del receptor β, que contrarresta los efectos de las catecolaminas. [10] [11] Los receptores β1 y β2 son receptores acoplados a proteína G , que se acoplan a proteínas Gαs. Cuando se activan, estimulan un aumento del AMPc intracelular a través de la adenilil ciclasa. El AMPc, que es el segundo mensajero, activa entonces la proteína quinasa A , que fosforila el canal de calcio de la membrana y aumenta la entrada de calcio al citosol . La proteína quinasa A también aumenta la liberación de calcio del retículo sarcoplásmico , lo que provoca un efecto inotrópico positivo . La fosforilación de la troponina I y el fosfolambano por la proteína quinasa A provoca los efectos lusitrópicos de los betabloqueantes. Esto aumenta la recaptación de calcio por el retículo sarcoplásmico . [10]
Los betabloqueantes son fármacos simpaticolíticos . Algunos betabloqueantes activan parcialmente el receptor al mismo tiempo que impiden que las catecolaminas se unan al receptor, lo que los convierte en agonistas parciales . Proporcionan un fondo de actividad simpática, al tiempo que impiden la actividad simpática normal y aumentada. Estos betabloqueantes poseen actividad simpaticomimética intrínseca (ASI). Algunos de ellos también poseen lo que se denomina actividad estabilizadora de la membrana (AMS) en las fibras musculares del miocardio . [12]
Los betabloqueantes pueden ser selectivos para los receptores adrenérgicos β 1 y β 2 o no selectivos. Al bloquear el receptor β 1 es posible reducir la frecuencia cardíaca, la velocidad de conducción y la contractilidad. El bloqueo del receptor β 2 promueve la contracción del músculo liso vascular, lo que produce un aumento de la resistencia periférica . [13] El bloqueo del receptor β 2 reduce eficazmente la actividad simpática, lo que produce una reducción de la activación plaquetaria y de la coagulación asociada . Por eso, un tratamiento con betabloqueantes no selectivos puede dar como resultado un menor riesgo de eventos embólicos tanto arteriales como venosos . [14]


La síntesis de un β-bloqueador estándar comienza con la monoalquilación del catecol para dar un éter (véase la figura 4 ). [15]
El paso fundamental, y habitualmente el último, en la síntesis de β-bloqueantes consiste en añadir una cadena lateral de propanolamina. Esto se puede hacer siguiendo dos vías que implican la alquilación de un fenóxido apropiado con epiclorhidrina (ECH). La primera vía se muestra como la vía superior en la figura 5. Consiste en que el fenóxido reacciona en el oxirano y da como resultado un alcóxido, que desplaza el cloruro adyacente para formar un nuevo anillo epóxido . La segunda vía se muestra como la vía inferior en la figura 5. Consiste en el desplazamiento del halógeno directamente con una reacción S N 2 para dar el mismo éter glicídico. Al seguir ambas vías, el carbono quiral central conserva su configuración, lo que es una parte importante a tener en cuenta al sintetizar fármacos definidos enantioméricamente. La apertura del anillo de epóxido en el éter glicídico se realiza con una amina apropiada, como la isopropilamina o la terc-butilamina, y da lugar al compuesto ariloxipropanolamina, que consiste en una amina secundaria. Esta amina se conoce normalmente como el requisito estructural para la actividad de bloqueo β-adrenérgico. [15]
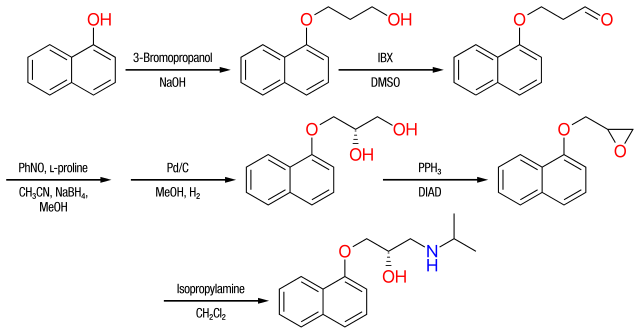
El propranolol existe en dos enantiómeros diferentes, los enantiómeros ( S )-(−)- y ( R )-(+)-. El isómero ( S )- es 100 veces más potente que el isómero ( R )- y esa es la regla general para la mayoría de los β-bloqueantes. Es posible producir el enantiómero ( S )-propranolol a partir de α-naftol y 3-bromopropanol como se ve en la figura 6 . [16] [17] El α-naftol y el 3-bromopropanol se refluyen durante 6 horas para dar alcohol. El alcohol se oxida utilizando ácido 2-yodoxibenzoico (IBX) para dar aldehído . El aldehído se somete a α-aminoxilación asimétrica catalizada por L -prolina y se realiza una reducción con NaBH 4 en metanol . Se obtiene un diol mediante hidrogenólisis catalizada por Pd/C. Finalmente, el diol se convierte en epóxido utilizando la reacción de Mitsunobu y se agita con isopropilamina en CH 2 Cl 2 para dar ( S )-propranolol. [16]
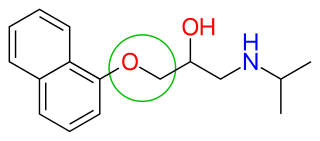
El sitio de unión de los β-bloqueantes al receptor es el mismo que el de las catecolaminas endógenas , como la noradrenalina y la adrenalina . Esta unión se basa en enlaces de hidrógeno entre el β-bloqueante y el receptor, y por lo tanto no se basa en enlaces covalentes , lo que da como resultado la reversibilidad de la unión. [18] Un paso significativo en el desarrollo de los antagonistas β adrenérgicos fue el descubrimiento de que un puente de oximetileno (—OCH 2 —, figura 7 ) podía insertarse en la estructura de ariletanolamina del pronetalol para producir propranolol. El propranolol es una ariloxipropanolamina, que son β-bloqueantes más potentes que las ariletanolaminas. Hoy en día, la mayoría de los β-bloqueantes utilizados clínicamente son ariloxipropanolaminas. La longitud de la cadena lateral aumenta cuando se introduce un puente de oximetileno. Se ha demostrado que las cadenas laterales de ariloxipropanolamina pueden adoptar una conformación que coloca los grupos hidroxilo y amina en más o menos la misma posición que con los betabloqueantes que no tienen este grupo como parte de la cadena lateral. [2]
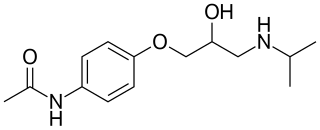
Después de la liberación del propranolol, la lipofilicidad relativa de los betabloqueantes, como factor significativo en su variada y compleja farmacología, se convirtió en un factor importante. Se sospechó que los efectos secundarios inducidos centralmente por el propranolol podrían deberse a su alta lipofilicidad. Por lo tanto, se centró en sintetizar análogos con fracciones hidrófilas , en una posición favorable para ver si los efectos secundarios disminuirían. Al seleccionar grupos para -acilamino como la fracción hidrófila, los científicos sintetizaron un grupo de para -acilfenoxietanol y propanolaminas, y seleccionaron practolol para ensayos clínicos. El practolol tenía una propiedad que no se había visto anteriormente con los betabloqueantes: exhibía cardioselectividad (selectividad β 1 ). Los estudios con practolol mostraron que mover el grupo acilamino a posiciones meta u orto, en el anillo de benceno , causaba una pérdida de selectividad, pero no la pérdida del betabloqueo en sí. Esto ilustró la importancia de la para -sustitución para la selectividad β1 de los β-bloqueantes. [5]

La figura 8 muestra la relación estructura-actividad (SAR) de los betabloqueantes. Para que un betabloqueante funcione es esencial que el compuesto contenga un anillo aromático y una betaetanolamina. El anillo aromático puede ser benzoheterocíclico (como el indol ) o heterocíclico (como el tiadiazol). Esto es obligatorio. [5] [19] Las cadenas laterales pueden ser variables:
La regla general para la sustitución aromática es: orto > meta > para . Esto da como resultado betabloqueantes no selectivos. Los grandes sustituyentes para suelen disminuir la actividad, pero los grandes grupos orto conservan cierta actividad. La polisustitución en el carbono 2 y 6 hace que el compuesto sea inactivo, pero cuando la sustitución es en el carbono 3 y 5 hay cierta actividad. Para la cardioselectividad más alta, los sustituyentes deberían ser los siguientes: para > meta > orto . Todo el betabloqueante está en un isómero, ( S )-ariloxipropilamina y ( R )-etanolamina. [5]
Durante décadas, los betabloqueantes se han utilizado en medicina cardiovascular . Han demostrado reducir la morbilidad y la mortalidad . [20] En el síndrome coronario agudo , los betabloqueantes se han recomendado como una indicación de clase IA en las guías de práctica clínica, porque el tratamiento disminuye la tasa de mortalidad. [21] Los betabloqueantes, junto con los bloqueadores de los canales de calcio , reducen la carga de trabajo del corazón y su requerimiento de oxígeno. Los betabloqueantes a veces se utilizan en una terapia combinada para tratar la angina, si un betabloqueante no funciona lo suficientemente bien por sí solo. [20] Se utilizan como fármacos antiarrítmicos en pacientes con hipertiroidismo , arritmia cardíaca , fibrilación auricular , aleteo auricular y taquicardia ventricular . El tratamiento con betabloqueantes reduce la incidencia de insuficiencia cardíaca súbita cuando el paciente ya ha tenido un infarto de miocardio. La razón probablemente se deba a sus efectos antiarrítmicos y también a sus efectos antiisquémicos. [10] La terapia con betabloqueantes también es útil en el infarto de miocardio, independientemente de la insuficiencia cardíaca. La terapia ha sido muy útil para pacientes de alto riesgo. [22] Aunque los betabloqueantes reducen eficazmente la presión arterial, no se recomiendan como agente de primera línea en el tratamiento de la hipertensión, ya que los diuréticos tiazídicos, los inhibidores de la ECA y los bloqueadores de los canales de calcio muestran un mayor beneficio. [23] Por lo tanto, los betabloqueantes se utilizan habitualmente junto con otros medicamentos para la presión arterial, como los bloqueadores de los canales de calcio. [24] También tienen un efecto sobre la miocardiopatía , el síndrome de taquicardia ortostática postural y la hipertensión portal , por nombrar algunos. [25] [26] [27]
Aparte de las enfermedades cardiovasculares, hay pocas enfermedades en las que los betabloqueantes tengan un efecto clínico. Estas enfermedades se mencionan en los siguientes subcapítulos. Además, hay enfermedades en las que los betabloqueantes tienen un efecto clínico pero no son la primera opción de tratamiento. No se mencionarán en los subcapítulos.
Cuando los síntomas de los temblores esenciales son muy intensos, los betabloqueantes no selectivos son una opción de tratamiento importante y, por lo general, la primera opción. Los estudios han demostrado que el propranolol redujo en mayor medida los síntomas en esa categoría. Los betabloqueantes pueden utilizarse solos o en combinación. [28]
El glaucoma es causado por una presión intraocular (PIO) elevada. Los betabloqueantes reducen la PIO y son la terapia más común. La mayoría de los pacientes que usan betabloqueantes tópicos necesitan terapia adyuvante para lograr una reducción de la PIO deseada. Uno de los fármacos más utilizados en la terapia adyuvante es la dorzolamida . [29]
Se ha informado que la hipertensión complica uno de cada diez embarazos, lo que la convierte en el trastorno médico más común durante el embarazo. Es importante tener un diagnóstico correcto de la hipertensión durante el embarazo, con énfasis en diferenciar la hipertensión preexistente de la hipertensión inducida por el embarazo ( gesta y síndrome de preeclampsia ). Durante el embarazo, el desafío es determinar cuándo usar medicamentos antihipertensivos y qué nivel de presión arterial se debe alcanzar. [30] Se debe encontrar un equilibrio entre el riesgo potencial para la salud del bebé relacionado con la exposición a medicamentos y el riesgo para la madre y el bebé debido a una condición médica no tratada (hipertensión grave). [31]
El uso de fármacos antihipertensivos durante el embarazo es relativamente común y está aumentando. [32] Solo una pequeña proporción de los fármacos antihipertensivos disponibles se han probado en mujeres embarazadas, y muchos están contraindicados. [ cita requerida ] Es importante hacer que la exposición del bebé a los medicamentos sea lo más pequeña posible. [30] No está claro si el tratamiento de las mujeres que tienen hipertensión leve o moderada durante el embarazo con medicamentos antihipertensivos es beneficioso. [33] [31]
Los betabloqueantes son los fármacos antihipertensivos más comunes durante el primer trimestre . Las consecuencias del tratamiento con betabloqueantes durante el embarazo son discutibles. Algunos estudios indican una conexión entre el tratamiento con betabloqueantes y el tamaño pequeño para la edad gestacional (PEG) de los recién nacidos y el parto prematuro, mientras que otros no lo indican. [34] Según los metanálisis, el uso de betabloqueantes orales durante el primer trimestre no mostró un aumento de las probabilidades de anomalías congénitas importantes . Sin embargo, los análisis que examinaron malformaciones específicas de órganos observaron un aumento de las probabilidades de defectos cardiovasculares, labio leporino y defectos del tubo neural . [35] La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) clasifica los betabloqueantes en diferentes categorías de embarazo según la seguridad de los fármacos y van de la categoría B a la D, es decir, ningún betabloqueante es completamente seguro para su uso durante el embarazo. [36]