Corynebacterium striatum es una bacteria que pertenece al género Corynebacterium . [1] Está clasificada como no diftérica . [2] La bacteria es un procariota grampositivo que asume una morfología "similar a un palo", más formalmente conocida como estructura de corinebacteria . [1] [3] [4] No es lipofílica y experimenta respiración aeróbica . Es un anaerobio facultativo. Es catalasa negativa y es un fermentador de glucosa y sacarosa oxidasa positivo. [1] [3]
Se encuentra generalmente como un microorganismo ubicuo y como un comensal de los humanos que coloniza la nasofaringe. . [1] [5] Recientemente se ha reconocido como un patógeno emergente, aunque el género de Corynebacterium no suele considerarse patógeno. Particularmente en el contexto de la enfermedad humana, Corynebacterium striatum generalmente se considera un patógeno oportunista. Esto es particularmente en un entorno nosocomial . [5] [6] Se ha registrado que infecta la piel y el tracto respiratorio superior e inferior e incluso se disemina, lo que resulta en sepsis . Recientemente se ha despertado un interés en el microorganismo, ya que se sabe que es resistente y está adquiriendo resistencia a muchos antibióticos . [7]
Corynebacterium striatum es un miembro del género Corynebacterium . [4] Inicialmente, la especie fue descrita en 1901. [8] Los artículos científicos que datan de aproximadamente 1980 relatan casos de Corynebacterium striatum comensal que contaminaron muestras de sitios de infecciones. Un artículo publicado en 1993 encontró que los aislamientos de Corynebacterium Striatum descritos almacenados por la Colección Americana de Cultivos Tipo y la Colección Nacional de Cultivos Tipo no eran de hecho los de Corynebacterium striatum , aunque las secuencias registradas correspondían con otros aislamientos conocidos de la especie. [9] Por lo tanto, se determinó que, en el momento del aislamiento para el almacenamiento, se había almacenado la especie bacteriana incorrecta. [9] Hasta 1993, solo había habido tres casos documentados de infecciones respiratorias causadas por la especie. [10] Posteriormente, se volvió a definir formalmente en 1995. [6] Durante mucho tiempo, las bacterias corineformes se habían descrito como comensales de los humanos, que colonizaban la piel y las membranas mucosas sin causar enfermedades. [11] Más recientemente, se descubrió que Corynebacterium striatum , de hecho, era la causa de infección o enfermedad si se le daba la oportunidad. [6] Las primeras pruebas clínicas de pacientes hospitalizados descubrieron que la infección generalmente solo se producía en individuos inmunodeprimidos o en aquellos que tenían algún tipo de dispositivo protésico colocado de forma permanente o intermitente. [2] No mucho después, los investigadores comenzaron a proponer la noción de que Corynebacterium striatum era la causa de la enfermedad incluso en pacientes que no cumplían dichos criterios. [2] [7]

Se han desarrollado métodos estandarizados de identificación para mejorar la identificación y el aislamiento de Coronyforms. Uno de estos métodos es el sistema API Coryne V2.0. [12] Las tiras API combinan una serie de pruebas bioquímicas a pequeña escala para distinguir las características clave de una bacteria, en función de la actividad metabólica . [13] Los resultados se interpretan a través de indicadores y gráficos estandarizados. [13] Este es un método de identificación rentable, pero que requiere mucho tiempo y demora aproximadamente 16 horas. Esto se aplica específicamente a entornos clínicos.
Las técnicas de identificación más modernas incluyen la secuenciación del genoma, en particular la secuenciación del ARN ribosómico 16S (ARNr) . [12] Esta técnica se basa en la comparación computarizada de secuencias genómicas entre bacterias. [14] La secuencia del ARNr 16S está altamente conservada entre bacterias, aunque mostrará ligeras variaciones y mutaciones entre cepas. [14] La comparación de variaciones en el genoma de Corynebacterium permite la identificación específica de Corynebacterium Striatum . Este es actualmente un método de identificación relativamente caro, en comparación con la tira API, aunque esto está mejorando a medida que mejoran las tecnologías. [14] El sistema MALDI-TOF es un método de detección clínicamente relevante que proporciona una identificación rápida (10 minutos) de bacterias específicas. [12]
Tanto la identificación bioquímica como la molecular se acompañan de una caracterización física. El cultivo de las bacterias en hemocultivos y la tinción de Gram para confirmar la morfología son complementos integrales del proceso de identificación. [11]
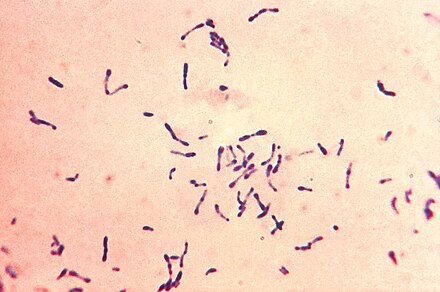
Corynebacterium striatum es una bacteria grampositiva . Tiene una estructura de pared celular externa delgada de peptidoglicano . [1] [15] Se ha descrito como de forma pleomórfica irregular y no móvil. [16] Bajo un microscopio, parece tener un híbrido de la morfología de bacilo y cocos con un polo abultado unido a un extremo en forma de varilla, más comúnmente descrito como una estructura "similar a un garrote". [1] [17] Se describe ampliamente como de 1,5 a 8,0 micrómetros de longitud, pero la medición formal de los aislados clínicos individuales variará según la observación. [17] Las colonias de C. striatum se pueden sembrar in vitro ; cuando crecen en agar sangre, las colonias aparecerán pequeñas (1-2 mm de diámetro) con una apariencia blanca, húmeda y suave. [1] [18] También se le llama difteroide o corineforme debido a su estrecha relación filogenética con la bacteria causante de la difteria Corynebacterium diphtheriae . [4]
Corynebacterium striatum se puede diferenciar de otros tipos de Corynebacterium en función de su capacidad para fermentar glucosa y sacarosa, y su incapacidad para fermentar maltosa. [1] [16] En comparación con otros miembros del género Corynebacterium , fermenta azúcares rápidamente. [5] También se sabe que las especies de Corynebacterium fermentan nitratos. [16] Es capaz de hidrolizar tirosina y pirazinamida . No metaboliza la ureasa, puede hidrolizar la esculina y también puede fermentar manitol y xilosa. [5] En un entorno de laboratorio, se distingue mejor de otras coronioformas a través de su actividad fermentativa. Estas bacterias no son lipofílicas y prefieren persistir [ cita requerida ] . Se han reconstruido modelos metabólicos a escala del genoma específicos de la cepa para las cepas de C. striatum 1054, 1197, 1115 y 1116. [19]
El organismo en sí posee pocos factores de virulencia, lo que le da el título de colonizador oportunista en lugar de un verdadero patógeno . [7] La virulencia surge de sus propiedades de resistencia a los antibióticos. [1] La creciente adquisición de genes de resistencia a los antibióticos permite la patogénesis de Corynebacterium striatum a través de la colonización . [1] [6]
La resistencia a los antibióticos es la adquisición de resistencia a los tratamientos con antibióticos a través de transferencia horizontal de genes o mutación genética . [20] La adquisición de dichas características por parte de Corynebacterium striatum es relevante para su aparición como patógeno. [ cita requerida ]
Un estudio encontró que el 93,7% de las cepas de Corynebacterium striatum aisladas mostraron resistencia a al menos uno de los compuestos antimicrobianos probados. En este experimento, el 82,5% de las cepas expresaron resistencia al antibiótico penicilina . [7] Los investigadores dedujeron que debido a la exposición prolongada de Corynebacterium striatum a la penicilina, la mayoría de los aislados habían adquirido resistencia. En el mismo experimento, se observó resistencia a múltiples fármacos en el 49,2% de las cepas. [7]
Se ha descubierto que Corynebacterium striatum es portador del gen bla . [7] Este gen codifica una β-lactamasa de clase A. Las β-lactamasas son un grupo de enzimas antimicrobianas que actúan para contrarrestar el efecto de los antibióticos β-lactámicos como la ampicilina y la penicilina.
Otros genes asociados con la resistencia a los antibióticos incluyen, entre otros: el gen gyrA, que se atribuye a la resistencia al principal grupo de antibióticos , las fluoroquinolonas , el gen aph ( 3 ′) -Ic, que confiere resistencia a la kanamicina , el aph ( 3 ″) -Ib y el aph ( 6 ) -Id, que causan resistencia a la estreptomicina. Los investigadores también descubrieron que el gen erm ( X ) causa resistencia a la eritromicina. [7] [21] [22]
Inicialmente se pensó que la infección con Corynebacterium striatum se producía por autoinfección, transmitiendo la bacteria desde un sitio donde persiste como comensal y luego permitiéndole colonizar como patógeno . [2] [23] Ahora se sabe que puede transmitirse de persona a persona, particularmente en un entorno hospitalario. [2] [23]
Si bien las infecciones por Corynebacterium no son comunes, se han observado en personas con dispositivos protésicos o inmunodeprimidas. [6] Cuando se detecta en estas condiciones, se considera un verdadero patógeno. También se reconocen los tipos de Corynebacterium no diftéricos por su impacto en quienes padecen enfermedades respiratorias a largo plazo. [24]
Se han documentado muchos casos de infección por Corynebacterium striatum con especial relevancia en la adquisición de la infección en hospitales, también conocida como infección nosocomial . [23] [3] Se sabe que Corynebacterium striatum coloniza prótesis , en particular válvulas cardíacas, prótesis articulares e incluso aparatos intravenosos como catéteres. [7] Las infecciones de este tipo se han descrito como una infección local o como capaces de convertirse en una infección diseminada más extendida, también conocida como bacteriemia . Otras infecciones documentadas incluyen la osteomielitis , una infección ósea que puede ocurrir a través de una infección transmitida por la sangre o una lesión en el propio hueso. [4] [25]
Una de las primeras infecciones descritas de un individuo con Corynebacterium striatum ocurrió en 1980. [26] El hombre estaba severamente inmunodeprimido, ya sufría de leucemia. [26] Después de esto, se documentaron varios casos aislados. Un brote bien documentado, en el Hospital Joan March - Mallorca, España , vio a 21 individuos infectados con Corynebacterium striatum . [23] Todos los individuos sufrían de enfermedad pulmonar obstructiva crónica (EPOC), y también recibieron una exposición significativa al tabaco a lo largo de sus vidas, y como tal, eran ingresados constantemente en el hospital donde eran tratados por personal de atención con equipo compartido. [23] En este caso, Corynebacterium striatum estaba causando infección en el tracto respiratorio de los pacientes y se detectó en muestras de esputo. [23] De los 21 casos en el brote, hubo seis muertes asociadas. [23]
Otro estudio sobre la infección por Corynebacterium striatum describió a una paciente que fue ingresada en un hospital para recibir tratamiento por un paro cardíaco en 2008. [3] Durante su estadía, a la paciente se le colocó un catéter venoso central a través del cual contrajo bacteriemia por Corynebacterium striatum que resultó en su muerte. [3] La edad de la paciente y su estado inmunocomprometido resultante de una insuficiencia renal preexistente finalmente permitieron el establecimiento y la diseminación de la infección. [3]
Hay poca o ninguna evidencia de infección o colonización de especímenes animales por Corynebacterium Striatum.
La resistencia a múltiples fármacos es el principal factor que se considera al tratar la enfermedad causada por Corynebacterium striatum . [20] [6] Por lo tanto, puede ser necesario el tratamiento con una mezcla de antibióticos de amplio espectro . La selección de una mayor resistencia a los antibióticos es una consideración importante que se debe tener en cuenta al seleccionar el tratamiento del paciente. Un estudio sobre la aparición de infecciones no difteroides determinó que, de todas las bacterias analizadas, Corynebacterium Striatum tuvo la mayor incidencia , representando el 47% de las infecciones. [27] En el mismo estudio, se determinó que todas las corinebacterias no difteroides eran susceptibles al tratamiento con vancomicina , quinupristina-dalfopristina , linezolida y gentamicina . [27] Si bien varios estudios confirmaron que la vancomicina fue muy eficaz en todas las especies aisladas. [10] [28] Anteriormente se sabía que Coronybacterium era susceptible a las β-lactáminas , tetraciclina y fluoroquinolonas , pero recientemente, se han observado genes de resistencia a tales tratamientos en aislados clínicos. [28] Se observó una resistencia similar en un estudio con todos los aislados que mostraban resistencia a la ciprofloxacina . [10] De importancia clínica significativa es una resistencia creciente a las betalactámicas en las últimas dos décadas, un grupo de antibióticos que incluye la penicilina . [29] Los tratamientos orales sugeridos incluyen una clase de oxazolidinonas : linezolid . [28] Aunque el tratamiento con linezolid no se prescribe a menudo, puede afectar la función hepática y tener efectos secundarios negativos como dolores de cabeza y náuseas. [30] Aunque se han observado diferentes resultados de susceptibilidad al tratamiento con antibióticos entre experimentos, dicha susceptibilidad específica de los aislados debe obtenerse mediante pruebas de sensibilidad a los antibióticos . En situaciones clínicas, la sensibilidad a los antibióticos se puede obtener mediante ensayos de difusión en disco de la prueba E-strip. El tratamiento de los casos clínicos, como el brote del Hospital Joan March, se realizó caso por caso, basándose en el antibiograma obtenido de la muestra de esputo de cada paciente . [23]
En términos más generales, la prevención de la infección inicial, en particular en el ámbito hospitalario, es un elemento clave del tratamiento. La esterilización de todas las superficies y prótesis, así como el reemplazo y mantenimiento constantes de las prótesis, es un elemento integral para detener la aparición de la enfermedad. [31]