
El sistema de grupo sanguíneo ABO se utiliza para indicar la presencia de uno, ambos o ninguno de los antígenos A y B en los eritrocitos (glóbulos rojos). [1] Para las transfusiones de sangre humana , es el más importante de los 44 sistemas de clasificación de tipos (o grupos) sanguíneos diferentes actualmente reconocidos por la Sociedad Internacional de Transfusiones de Sangre (ISBT) a diciembre de 2022. [2] [3] Un desajuste en este serotipo (o en varios otros) puede provocar una reacción adversa potencialmente mortal después de una transfusión, o una respuesta inmunitaria no deseada a un trasplante de órgano. [4] Estos desajustes son poco frecuentes en la medicina moderna. Los anticuerpos anti-A y anti-B asociados suelen ser anticuerpos IgM , producidos en los primeros años de vida por sensibilización a sustancias ambientales como alimentos, bacterias y virus.
Los tipos de sangre ABO fueron descubiertos por Karl Landsteiner en 1901; recibió el Premio Nobel de Fisiología o Medicina en 1930 por este descubrimiento. [5] Los tipos de sangre ABO también están presentes en otros primates como simios , monos y monos del Viejo Mundo . [6]
Los tipos de sangre ABO fueron descubiertos por primera vez por un médico austríaco, Karl Landsteiner , que trabajaba en el Instituto Anatómico Patológico de la Universidad de Viena (ahora Universidad Médica de Viena ). En 1900, descubrió que los glóbulos rojos se agrupaban ( aglutinaban ) cuando se mezclaban en tubos de ensayo con sueros de diferentes personas, y que cierta sangre humana también se aglutinaba con sangre animal. [7] Escribió una nota a pie de página de dos oraciones:
El suero de seres humanos sanos no sólo aglutina glóbulos rojos animales, sino también, a menudo, los de origen humano, de otros individuos. Queda por ver si esta apariencia está relacionada con diferencias innatas entre individuos o es el resultado de algún daño de tipo bacteriano. [8]
Esta fue la primera evidencia de que existen variaciones en la sangre de los humanos: se creía que todos los humanos tienen sangre similar. Al año siguiente, en 1901, hizo una observación definitiva: el suero sanguíneo de un individuo se aglutinaría solo con el de ciertos individuos. Basándose en esto, clasificó la sangre humana en tres grupos, a saber, el grupo A, el grupo B y el grupo C. Definió que la sangre del grupo A se aglutina con el grupo B, pero nunca con su propio tipo. De manera similar, la sangre del grupo B se aglutina con el grupo A. La sangre del grupo C es diferente en que se aglutina tanto con A como con B. [9]
Este fue el descubrimiento de los grupos sanguíneos por el que Landsteiner recibió el Premio Nobel de Fisiología o Medicina en 1930. En su artículo, se refirió a las interacciones específicas de los grupos sanguíneos como isoaglutinación, y también introdujo el concepto de aglutininas (anticuerpos), que es la base real de la reacción antígeno-anticuerpo en el sistema ABO. [10] Afirmó:
Se puede decir que existen al menos dos tipos diferentes de aglutininas, una en A, otra en B y ambas juntas en C. Los glóbulos rojos son inertes a las aglutininas que están presentes en el mismo suero. [9]
Así, descubrió dos antígenos ( aglutinógenos A y B) y dos anticuerpos (aglutininas: anti-A y anti-B). Su tercer grupo (C) indicaba la ausencia de antígenos A y B, pero contenía anti-A y anti-B. [10] Al año siguiente, sus estudiantes Adriano Sturli y Alfred von Decastello descubrieron el cuarto tipo (pero sin nombrarlo, y simplemente se refirieron a él como "ningún tipo en particular"). [11] [12]

En 1910, Ludwik Hirszfeld y Emil Freiherr von Dungern introdujeron el término 0 (nulo) para el grupo que Landsteiner designó como C, y AB para el tipo descubierto por Sturli y von Decastello. También fueron los primeros en explicar la herencia genética de los grupos sanguíneos. [13] [14]

El serólogo checo Jan Janský introdujo de forma independiente la clasificación de los tipos de sangre en 1907 en una revista local. [15] Utilizó los números romanos I, II, III y IV (que corresponden a los actuales O, A, B y AB). Sin que Janský lo supiera, un médico estadounidense, William L. Moss, ideó una clasificación ligeramente diferente utilizando el mismo número; [16] sus I, II, III y IV corresponden a los actuales AB, A, B y O. [12]
Estos dos sistemas crearon confusión y un peligro potencial en la práctica médica. El sistema de Moss fue adoptado en Gran Bretaña, Francia y Estados Unidos, mientras que el de Janský fue el preferido en la mayoría de los países europeos y algunas partes de Estados Unidos. Para resolver el caos, la Asociación Estadounidense de Inmunólogos , la Sociedad Estadounidense de Bacteriólogos y la Asociación de Patólogos y Bacteriólogos hicieron una recomendación conjunta en 1921 para que se adoptara la clasificación de Janský en función de la prioridad. [17] Pero no se siguió particularmente donde se había utilizado el sistema de Moss. [18]
En 1927, Landsteiner se había trasladado al Instituto Rockefeller de Investigación Médica en Nueva York. Como miembro de un comité del Consejo Nacional de Investigación que se ocupaba de la agrupación sanguínea, sugirió sustituir los sistemas de Janský y Moss por las letras O, A, B y AB. (Hubo otra confusión sobre el uso de la cifra 0 para el alemán null introducido por Hirszfeld y von Dungern, porque otros usaban la letra O para ohne , es decir, sin o cero; Landsteiner eligió esta última. [18] ) Esta clasificación fue adoptada por el Consejo Nacional de Investigación y se conoció de diversas formas: la clasificación del Consejo Nacional de Investigación, la clasificación internacional y, más popularmente, la "nueva" clasificación de Landsteiner. El nuevo sistema fue aceptado gradualmente y, a principios de la década de 1950, era universalmente seguido. [19]
El primer uso práctico de la tipificación sanguínea en transfusiones fue realizado por un médico estadounidense, Reuben Ottenberg, en 1907. La aplicación a gran escala comenzó durante la Primera Guerra Mundial (1914-1915), cuando se empezó a utilizar ácido cítrico para la prevención de coágulos sanguíneos . [10] Felix Bernstein demostró el patrón correcto de herencia del grupo sanguíneo de múltiples alelos en un locus en 1924. [20] Watkins y Morgan, en Inglaterra, descubrieron que los epítopos ABO eran conferidos por azúcares, para ser específicos, N-acetilgalactosamina para el tipo A y galactosa para el tipo B. [21] [22] [23] Después de mucha literatura publicada que afirmaba que las sustancias ABH estaban todas unidas a glicoesfingolípidos, Finne et al . (1978) encontraron que las glicoproteínas de eritrocitos humanos contienen cadenas de polilactosamina [24] que contienen sustancias ABH unidas y representan la mayoría de los antígenos. [25] [26] [27] Se identificaron las principales glicoproteínas que transportan los antígenos ABH como las proteínas Band 3 y Band 4.5 y la glicoforina. [28] Más tarde, el grupo de Yamamoto demostró el conjunto preciso de glicosil transferasas que confiere los epítopos A, B y O. [29]
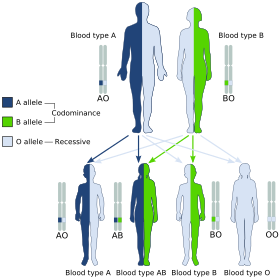

Los grupos sanguíneos se heredan de ambos padres. El tipo sanguíneo ABO está controlado por un solo gen (el gen ABO ) con tres tipos de alelos inferidos a partir de la genética clásica : i , I A y I B. La designación I significa isoaglutinógeno , otro término para antígeno . [31] El gen codifica una glicosiltransferasa , es decir, una enzima que modifica el contenido de carbohidratos de los antígenos de los glóbulos rojos . El gen está ubicado en el brazo largo del noveno cromosoma (9q34). [32]
El alelo I A da el tipo A, el I B da el tipo B y el i da el tipo O. Como tanto I A como I B son dominantes sobre i , solo las personas ii tienen sangre tipo O. Los individuos con I A I A o I A i tienen sangre tipo A, y los individuos con I B I B o I B i tienen tipo B. Las personas I A I B tienen ambos fenotipos , porque A y B expresan una relación de dominancia especial: codominancia , lo que significa que los padres de tipo A y B pueden tener un hijo AB. Una pareja con tipo A y tipo B también puede tener un hijo tipo O si ambos son heterocigotos ( I B i e I A i ). El fenotipo cis-AB tiene una sola enzima que crea antígenos A y B. Los glóbulos rojos resultantes no suelen expresar el antígeno A o B al mismo nivel que se esperaría en los glóbulos rojos comunes del grupo A 1 o B, lo que puede ayudar a resolver el problema de un grupo sanguíneo aparentemente genéticamente imposible. [33]
Los individuos con el raro fenotipo Bombay (hh) producen anticuerpos contra los grupos A, B y O y solo pueden recibir transfusiones de otros individuos hh. La tabla anterior resume los diversos grupos sanguíneos que los niños pueden heredar de sus padres. [34] [35] Los genotipos se muestran en la segunda columna y en letra pequeña para la descendencia: AO y AA dan como tipo A; BO y BB dan como tipo B. Las cuatro posibilidades representan las combinaciones obtenidas cuando se toma un alelo de cada progenitor; cada una tiene una probabilidad del 25%, pero algunas ocurren más de una vez. El texto sobre ellas resume los resultados.
Históricamente, las pruebas de sangre ABO se utilizaban en las pruebas de paternidad , pero en 1957 solo el 50% de los hombres estadounidenses acusados falsamente pudieron usarlas como evidencia contra la paternidad. [36] Ocasionalmente, los tipos de sangre de los niños no son consistentes con las expectativas (por ejemplo, un niño tipo O puede nacer de un padre AB) debido a situaciones raras, como el fenotipo Bombay y el cis AB . [37]
El tipo sanguíneo A contiene alrededor de 20 subgrupos, de los cuales A1 y A2 son los más comunes (más del 99%). A1 constituye alrededor del 80% de toda la sangre de tipo A, y A2 constituye casi todo el resto. [38] Estos dos subgrupos no siempre son intercambiables en lo que respecta a la transfusión, ya que algunos individuos A2 producen anticuerpos contra el antígeno A1. A veces pueden surgir complicaciones en casos raros al tipificar la sangre. [38]
Con el desarrollo de la secuenciación del ADN , ha sido posible identificar un número mucho mayor de alelos en el locus ABO, cada uno de los cuales puede categorizarse como A, B u O en términos de la reacción a la transfusión, pero que pueden distinguirse por variaciones en la secuencia del ADN . Hay seis alelos comunes en individuos blancos del gen ABO que producen el tipo de sangre de una persona: [39] [40]
El mismo estudio también identificó 18 alelos raros, que generalmente tienen una actividad de glicosilación más débil. Las personas con alelos débiles de A a veces pueden expresar anticuerpos anti-A, aunque estos no suelen ser clínicamente significativos ya que no interactúan de manera estable con el antígeno a temperatura corporal. [41]
Cis AB es otra variante rara, en la que los genes A y B se transmiten juntos desde un solo progenitor. [42]
La distribución de los grupos sanguíneos A, B, O y AB varía en todo el mundo según la población. También existen variaciones en la distribución de los tipos de sangre dentro de las subpoblaciones humanas. [ cita requerida ]
En el Reino Unido, la distribución de frecuencias de tipos de sangre en la población aún muestra cierta correlación con la distribución de los nombres de lugares y con las invasiones y migraciones sucesivas, incluidos los celtas , los nórdicos , los daneses , los anglosajones y los normandos , que aportaron los morfemas a los nombres de lugares y los genes a la población. Los celtas nativos tendían a tener más sangre tipo O, mientras que las otras poblaciones tendían a tener más tipo A. [43]
Los dos alelos O comunes, O01 y O02, comparten sus primeros 261 nucleótidos con el alelo A01 del grupo A. [44] Sin embargo, a diferencia del alelo del grupo A, posteriormente se elimina una base de guanosina . Un codón de terminación prematuro resulta de esta mutación por cambio de marco . Esta variante se encuentra en todo el mundo y probablemente es anterior a la migración humana desde África . Se considera que el alelo O01 es anterior al alelo O02. [ cita requerida ]
Algunos biólogos evolucionistas teorizan que existen cuatro linajes principales del gen ABO y que las mutaciones que crean el tipo O han ocurrido al menos tres veces en humanos. [45] Desde el más antiguo al más joven, estos linajes comprenden los siguientes alelos: A101/A201/O09 , B101 , O02 y O01 . Se plantea la hipótesis de que la presencia continua de los alelos O es el resultado de la selección equilibradora . [45] Ambas teorías contradicen la teoría previamente sostenida de que la sangre de tipo O evolucionó primero. [ cita requerida ]
Es posible que los antígenos alimentarios y ambientales (antígenos bacterianos, virales o vegetales) tengan epítopos lo suficientemente similares a los antígenos de las glicoproteínas A y B. Los anticuerpos creados contra estos antígenos ambientales en los primeros años de vida pueden reaccionar de forma cruzada con los glóbulos rojos incompatibles con ABO con los que entran en contacto durante una transfusión de sangre más adelante en la vida. Se plantea la hipótesis de que los anticuerpos anti-A se originan a partir de la respuesta inmunitaria al virus de la gripe , cuyos epítopos son lo suficientemente similares a la α-DN-galactosamina de la glicoproteína A como para poder provocar una reacción cruzada. Se plantea la hipótesis de que los anticuerpos anti-B se originan a partir de anticuerpos producidos contra bacterias gramnegativas , como E. coli , que reaccionan de forma cruzada con la α-D-galactosa de la glicoproteína B. [46]
Sin embargo, es más probable que la fuerza que impulsa la evolución de la diversidad de alelos sea simplemente una selección negativa dependiente de la frecuencia; el sistema inmunológico distingue más fácilmente las células con variantes raras de antígenos de membrana de los patógenos que portan antígenos de otros huéspedes. Por lo tanto, los individuos que poseen tipos raros están mejor equipados para detectar patógenos. La alta diversidad intrapoblacional observada en las poblaciones humanas sería, entonces, una consecuencia de la selección natural sobre los individuos. [47]
Las moléculas de carbohidratos en las superficies de los glóbulos rojos tienen funciones en la integridad de la membrana celular , la adhesión celular , el transporte de moléculas a través de la membrana y actúan como receptores para ligandos extracelulares y enzimas. Se ha descubierto que los antígenos ABO tienen funciones similares en las células epiteliales y en los glóbulos rojos. [48] [49]
El antígeno ABO también se expresa en la glicoproteína del factor von Willebrand (vWF) , [50] que participa en la hemostasia (control del sangrado). De hecho, tener sangre tipo O predispone al sangrado, [51] ya que el 30% de la variación genética total observada en el vWF plasmático se explica por el efecto del grupo sanguíneo ABO, [52] y los individuos con sangre del grupo O normalmente tienen niveles plasmáticos significativamente más bajos de vWF (y Factor VIII ) que los individuos no O. [53] [54] Además, el vWF se degrada más rápidamente debido a la mayor prevalencia del grupo sanguíneo O con la variante Cys1584 de vWF (un polimorfismo de aminoácidos en el VWF): [55] el gen para ADAMTS13 ( proteasa de escisión de vWF ) se asigna a la banda q34.2 del cromosoma 9 humano , el mismo locus que el tipo sanguíneo ABO. Los niveles más altos de vWF son más comunes entre las personas que han tenido un accidente cerebrovascular isquémico (por coagulación sanguínea) por primera vez. Los resultados de este estudio encontraron que la ocurrencia no fue afectada por el polimorfismo ADAMTS13, y el único factor genético significativo fue el grupo sanguíneo de la persona. [56]
Los antígenos del grupo sanguíneo ABO(H) también son transportados por otras glicoproteínas hemostáticamente relevantes, como la glicoproteína plaquetaria Ibα, que es un ligando para vWF en las plaquetas. [57] La importancia de la expresión del antígeno ABO(H) en estas otras glicoproteínas hemostáticas no está completamente definida, pero también puede ser relevante para el sangrado y la trombosis.
Las incompatibilidades de grupo sanguíneo ABO entre la madre y el niño no suelen causar enfermedad hemolítica del recién nacido (EHRN) porque los anticuerpos contra los grupos sanguíneos ABO suelen ser del tipo IgM , que no atraviesan la placenta. Sin embargo, en una madre de tipo O, se producen anticuerpos ABO IgG y el bebé puede desarrollar potencialmente enfermedad hemolítica del recién nacido ABO . [58]
En las células humanas, los alelos ABO y sus glicosiltransferasas codificadas se han descrito en varias condiciones oncológicas. [59] Utilizando anticuerpos monoclonales anti-GTA/GTB, se demostró que una pérdida de estas enzimas se correlacionaba con epitelios malignos de vejiga y boca. [60] [61] Además, la expresión de antígenos del grupo sanguíneo ABO en tejidos humanos normales depende del tipo de diferenciación del epitelio. En la mayoría de los carcinomas humanos, incluido el carcinoma oral, un evento significativo como parte del mecanismo subyacente es la expresión disminuida de los antígenos A y B. [62] Varios estudios han observado que una regulación negativa relativa de GTA y GTB ocurre en carcinomas orales en asociación con el desarrollo de tumores. [62] [63] Más recientemente, un estudio de asociación de todo el genoma (GWAS) ha identificado variantes en el locus ABO asociadas con la susceptibilidad al cáncer de páncreas. [64] Además, otro gran estudio GWAS ha asociado los grupos sanguíneos ABO-histo así como el estado secretor de FUT2 con la presencia en el microbioma intestinal de especies bacterianas específicas. En este caso la asociación fue con Bacteroides y Faecalibacterium spp . Se ha demostrado que los Bacteroides de la misma OTU (unidad taxonómica operativa) están asociados con la enfermedad inflamatoria intestinal, [65] [66] por lo tanto el estudio sugiere un papel importante para los antígenos del grupo sanguíneo ABO-histo como candidatos para la modulación directa del microbioma humano en la salud y la enfermedad. [67]
Un estudio de puntuación de riesgo genético de múltiples loci basado en una combinación de 27 loci, incluido el gen ABO, identificó a individuos con mayor riesgo de eventos de enfermedad arterial coronaria incidentes y recurrentes, así como un mayor beneficio clínico de la terapia con estatinas. El estudio se basó en un estudio de cohorte comunitaria (el estudio Malmo Diet and Cancer) y cuatro ensayos controlados aleatorizados adicionales de cohortes de prevención primaria (JUPITER y ASCOT) y cohortes de prevención secundaria (CARE y PROVE IT-TIMI 22). [68]
En abril de 2007, un equipo internacional de investigadores anunció en la revista Nature Biotechnology una forma barata y eficiente de convertir sangre de los tipos A, B y AB en sangre de tipo O. [69] Esto se hace utilizando enzimas glicosidasas de bacterias específicas para eliminar los antígenos del grupo sanguíneo de los glóbulos rojos . La eliminación de los antígenos A y B todavía no resuelve el problema del antígeno del grupo sanguíneo Rh en las células sanguíneas de individuos Rh positivos, por lo que debe utilizarse sangre de donantes Rh negativos. La sangre modificada se denomina "enzima convertida a O" (sangre ECO), pero a pesar del éxito temprano en la conversión de glóbulos rojos de tipo B a O y de los ensayos clínicos sin efectos adversos en la transfusión a pacientes de tipo A y O, [70] la tecnología aún no se ha convertido en una práctica clínica. [71]
Otro enfoque al problema del antígeno sanguíneo es la fabricación de sangre artificial , que podría actuar como sustituto en situaciones de emergencia. [72]
En Japón y otras partes de Asia Oriental, existe una creencia popular en la teoría de la personalidad basada en el tipo de sangre , que afirma que los tipos de sangre predicen o influyen en la personalidad. Esta afirmación no tiene base científica y existe consenso científico de que no existe tal vínculo; la comunidad científica la considera una pseudociencia y una superstición . [73]
La creencia se originó en la década de 1930, cuando se introdujo como parte del programa eugenésico de Japón. [74] Su popularidad se desvaneció tras la derrota de Japón en la Segunda Guerra Mundial y el apoyo japonés a la eugenesia flaqueó, pero resurgió en la década de 1970 de la mano de un periodista llamado Masahiko Nomi . A pesar de su condición de pseudociencia, sigue siendo muy popular en todo el este de Asia. [75]
Otras ideas populares son las necesidades dietéticas específicas del tipo de sangre , que el grupo A causa resacas severas , que el grupo O está asociado con mejores dientes y que aquellos con el grupo A2 tienen los puntajes de CI más altos . Al igual que con la teoría de la personalidad del tipo de sangre, estas y otras ideas populares carecen de evidencia científica, y muchas están desacreditadas o son pseudocientíficas. [76]
Die Vererbung der durch Isoaglutinine nachweisbaren spezifischen Strukturen A und B der menschlichen Blutkfirper erfolgt nach der Mendelschen Regel, wobei die Eigenschaft der Struktur dominante ist, das Fehlen der Struktur rezessiv. Die Tatsache, dafi die nachweisbaren Bestandteile der Blutkorper niemals rezessiv sind und daher bei den Kindern nie erscheinen, wenn nicht einer der Eltern sie enthait, ist forensisch zu verwerten.