La cisteína (símbolo Cys o C ; [5] / ˈ s ɪ s t ɪ iː n / ) [6] es un aminoácido proteinogénico semiesencial [7] con la fórmula HOOC−CH(−NH 2 )−CH 2 −SH . La cadena lateral de tiol de la cisteína participa a menudo en reacciones enzimáticas como nucleófilo . La cisteína es quiral, pero tanto la D como la L -cisteína se encuentran en la naturaleza. La L -cisteína es un monómero proteico presente en toda la biota y la D -cisteína actúa como molécula de señalización en el sistema nervioso de los mamíferos. [8] La cisteína debe su nombre a su descubrimiento en la orina, que proviene de la vejiga urinaria o quiste, de kystis "vejiga". [9]
El tiol es susceptible a la oxidación para dar el derivado disulfuro cistina , que desempeña un papel estructural importante en muchas proteínas . En este caso, a veces se utiliza el símbolo Cyx . [10] [11] La forma desprotonada generalmente también se puede describir con el símbolo Cym . [11] [12]
Cuando se utiliza como aditivo alimentario, la cisteína tiene el número E E920.
La cisteína está codificada por los codones UGU y UGC.
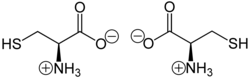
Al igual que otros aminoácidos (no como residuo de una proteína), la cisteína existe como un zwitterión . La cisteína tiene quiralidad l en la notación d / l más antigua basada en la homología con d - y l -gliceraldehído. En el sistema R / S más nuevo para designar quiralidad, basado en los números atómicos de los átomos cerca del carbono asimétrico, la cisteína (y la selenocisteína) tienen quiralidad R , debido a la presencia de azufre (o selenio) como segundo vecino del carbono asimétrico. átomo. Los aminoácidos quirales restantes, que tienen átomos más ligeros en esa posición, tienen quiralidad S. La sustitución del azufre por selenio da selenocisteína .
El cisteinilo es un residuo de los alimentos ricos en proteínas . Algunos alimentos considerados ricos en cisteína incluyen aves, huevos, carne de res y cereales integrales. En las dietas ricas en proteínas, la cisteína puede ser parcialmente responsable de la reducción de la presión arterial y del riesgo de accidente cerebrovascular. [13] Aunque está clasificada como un aminoácido no esencial , [14] en casos raros, la cisteína puede ser esencial para los bebés, los ancianos y las personas con ciertas enfermedades metabólicas o que sufren síndromes de malabsorción . Normalmente, el cuerpo humano puede sintetizar cisteína en condiciones fisiológicas normales si se dispone de una cantidad suficiente de metionina .
La mayor parte de la L -cisteína se obtiene industrialmente mediante hidrólisis de materiales animales, como plumas de aves o pelo de cerdo. A pesar de los rumores generalizados, [15] el cabello humano rara vez es un material de partida. [ cita necesaria ] De hecho, los fabricantes de aditivos alimentarios o productos cosméticos no pueden obtener legalmente cabello humano en la Unión Europea. [16] [17]
Algunas fuentes de l -cisteína de origen animal como aditivo alimentario contravienen las dietas kosher, halal, veganas o vegetarianas. [15] Para evitar este problema, también está disponible l -cisteína sintética, que cumple con las leyes judías kosher y musulmanas halal , aunque a un precio más alto. [18] La ruta sintética típica implica la fermentación con una cepa artificial de E. coli . [19]
Alternativamente, Evonik (anteriormente Degussa) introdujo una vía a partir de tiazolinas sustituidas . [20] Pseudomonas tiazolinophilum hidroliza el ácido 2-amino-Δ 2 -tiazolina-4-carboxílico racémico a l -cisteína. [19]

En los animales, la biosíntesis comienza con el aminoácido serina . El azufre se deriva de la metionina , que se convierte en homocisteína a través del intermediario S -adenosilmetionina . La cistationina beta-sintasa luego combina homocisteína y serina para formar la cistationina tioéter asimétrica . La enzima cistationina gamma-liasa convierte la cistationina en cisteína y alfa-cetobutirato . En plantas y bacterias , la biosíntesis de cisteína también comienza a partir de serina, que la enzima serina transacetilasa convierte en O -acetilserina . La enzima cisteína sintasa , utilizando fuentes de sulfuro, convierte este éster en cisteína, liberando acetato. [21]
El grupo sulfhidrilo de cisteína es nucleofílico y se oxida fácilmente. La reactividad aumenta cuando el tiol se ioniza y los residuos de cisteína en las proteínas tienen valores de pKa cercanos a la neutralidad, por lo que a menudo se encuentran en su forma de tiolato reactivo en la célula. [22] Debido a su alta reactividad, el grupo sulfhidrilo de la cisteína tiene numerosas funciones biológicas.
Debido a la capacidad de los tioles para sufrir reacciones redox, los residuos de cisteína y cisteinilo tienen propiedades antioxidantes . Sus propiedades antioxidantes se expresan típicamente en el tripéptido glutatión , que se encuentra en humanos y otros organismos. La disponibilidad sistémica de glutatión oral (GSH) es insignificante; por lo que debe ser biosintetizado a partir de sus aminoácidos constituyentes, cisteína, glicina y ácido glutámico . Si bien el ácido glutámico suele ser suficiente porque el nitrógeno del aminoácido se recicla a través del glutamato como intermediario, la suplementación dietética con cisteína y glicina puede mejorar la síntesis de glutatión. [23]
La cisteína es una fuente importante de sulfuro en el metabolismo humano . El sulfuro de los grupos hierro-azufre y de la nitrogenasa se extrae de la cisteína, que en el proceso se convierte en alanina . [24]
Más allá de las proteínas hierro-azufre, muchos otros cofactores metálicos en las enzimas están unidos al sustituyente tiolato de los residuos cisteinilo. Los ejemplos incluyen zinc en dedos de zinc y alcohol deshidrogenasa , cobre en las proteínas de cobre azul , hierro en el citocromo P450 y níquel en las [NiFe] -hidrogenasas . [25] El grupo sulfhidrilo también tiene una alta afinidad por los metales pesados , de modo que las proteínas que contienen cisteína, como la metalotioneína , se unirán firmemente a metales como el mercurio, el plomo y el cadmio. [26]
En la traducción de moléculas de ARN mensajero para producir polipéptidos, la cisteína está codificada por los codones UGU y UGC .
Tradicionalmente se ha considerado que la cisteína es un aminoácido hidrófilo , basándose en gran medida en el paralelo químico entre su grupo sulfhidrilo y los grupos hidroxilo en las cadenas laterales de otros aminoácidos polares. Sin embargo, se ha demostrado que la cadena lateral de cisteína estabiliza las interacciones hidrófobas en micelas en mayor grado que la cadena lateral del aminoácido no polar glicina y el aminoácido polar serina. [27] En un análisis estadístico de la frecuencia con la que aparecen los aminoácidos en varias proteínas, se encontró que los residuos de cisteína se asocian con regiones hidrofóbicas de las proteínas. Su tendencia hidrófoba era equivalente a la de los aminoácidos no polares conocidos, como la metionina y la tirosina (la tirosina es aromática polar pero también hidrófoba [28] ), los cuales eran mucho mayores que los de los aminoácidos polares conocidos, como la serina y la treonina . [29] Las escalas de hidrofobicidad , que clasifican los aminoácidos desde los más hidrófobos hasta los más hidrófilos, colocan consistentemente a la cisteína hacia el extremo hidrófobo del espectro, incluso cuando se basan en métodos que no están influenciados por la tendencia de las cisteínas a formar enlaces disulfuro en las proteínas. . Por lo tanto, la cisteína ahora se agrupa a menudo entre los aminoácidos hidrófobos, [30] [31] aunque a veces también se clasifica como ligeramente polar, [32] o polar. [7]
La mayoría de los residuos de cisteína están unidos covalentemente a otros residuos de cisteína para formar enlaces disulfuro , que desempeñan un papel importante en el plegamiento y la estabilidad de algunas proteínas, generalmente proteínas secretadas al medio extracelular. [33] Dado que la mayoría de los compartimentos celulares son ambientes reductores , los enlaces disulfuro son generalmente inestables en el citosol con algunas excepciones, como se indica a continuación.

Los enlaces disulfuro en las proteínas se forman mediante la oxidación del grupo sulfhidrilo de los residuos de cisteína. El otro aminoácido que contiene azufre, la metionina, no puede formar enlaces disulfuro. Oxidantes más agresivos convierten la cisteína en el correspondiente ácido sulfínico y ácido sulfónico . Los residuos de cisteína desempeñan un papel valioso al reticular proteínas, lo que aumenta la rigidez de las proteínas y también funciona para conferir resistencia proteolítica (dado que la exportación de proteínas es un proceso costoso, minimizar su necesidad es ventajoso). Dentro de la célula, los puentes disulfuro entre los residuos de cisteína dentro de un polipéptido sostienen la estructura terciaria de la proteína. La insulina es un ejemplo de una proteína con entrecruzamiento de cistina, en la que dos cadenas peptídicas separadas están conectadas por un par de enlaces disulfuro.
Las isomerasas disulfuro de proteínas catalizan la formación adecuada de enlaces disulfuro ; la célula transfiere ácido deshidroascórbico al retículo endoplásmico , que oxida el ambiente. En este entorno, las cisteínas, en general, se oxidan a cistina y ya no son funcionales como nucleófilos.
Aparte de su oxidación a cistina, la cisteína participa en numerosas modificaciones postraduccionales . El grupo sulfhidrilo nucleofílico permite que la cisteína se conjugue con otros grupos, por ejemplo, en prenilación . Las ubiquitina ligasas transfieren ubiquitina a su colgante, proteínas y caspasas , que participan en la proteólisis en el ciclo apoptótico. Los intestinos a menudo funcionan con la ayuda de una cisteína catalítica. Estas funciones suelen limitarse al medio intracelular, donde el entorno se reduce y la cisteína no se oxida a cistina.
La cisteína se considera un aminoácido "recién llegado", siendo el aminoácido número 17 incorporado al código genético. [34] [35] Al igual que otros aminoácidos agregados posteriormente, como metionina, tirosina y triptófano, la cisteína exhibe fuertes propiedades nucleofílicas y redox activas. [36] [37] Estas propiedades contribuyen al agotamiento de la cisteína de los complejos de la cadena respiratoria, como los complejos I y IV [38] , ya que las especies reactivas de oxígeno (ROS) producidas por la cadena respiratoria pueden reaccionar con los residuos de cisteína en estos complejos. , lo que lleva a proteínas disfuncionales y potencialmente contribuye al envejecimiento. La respuesta principal de una proteína a las ROS es la oxidación de la cisteína y la pérdida de grupos tiol libres [39] , lo que da como resultado un aumento de radicales tiilo y entrecruzamiento de proteínas asociadas [40] [41] . Por el contrario, otro aminoácido activo redox que contiene azufre, la metionina, no exhibe estas propiedades bioquímicas y su contenido está relativamente regulado positivamente en las proteínas codificadas mitocondrialmente [42] .
La cisteína, principalmente el enantiómero l , es un precursor en las industrias alimentaria, farmacéutica y de cuidado personal. Una de las aplicaciones más importantes es la producción de sabores. Por ejemplo, la reacción de la cisteína con los azúcares en una reacción de Maillard produce sabores a carne. [43] La l -cisteína también se utiliza como coadyuvante tecnológico para hornear. [44]
En el ámbito del cuidado personal, la cisteína se utiliza para aplicaciones de ondas permanentes , principalmente en Asia. Nuevamente, la cisteína se usa para romper los enlaces disulfuro en la queratina del cabello .
La cisteína es un objetivo muy popular para experimentos de etiquetado dirigidos al sitio para investigar la estructura y dinámica biomolecular. Las maleimidas se unen selectivamente a la cisteína mediante una adición covalente de Michael . El etiquetado de espín dirigido al sitio para EPR o RMN mejorada con relajación paramagnética también utiliza cisteína ampliamente.
La cisteína se ha propuesto como preventivo o antídoto para algunos de los efectos negativos del alcohol, incluidos el daño hepático y la resaca . Contrarresta los efectos venenosos del acetaldehído . [45] Se une al acetaldehído para formar el heterociclo metil tioprolina de baja toxicidad . [46]
En un estudio con ratas , los animales de prueba recibieron una dosis LD 90 de acetaldehído. Los que recibieron cisteína tuvieron una tasa de supervivencia del 80%; cuando se administraron cisteína y tiamina , todos los animales sobrevivieron. El grupo de control tuvo una tasa de supervivencia del 10%. [47]
En 2020 se publicó un artículo que sugiere que la L-cisteína también podría funcionar en humanos. [48]
La N -Acetil- l- cisteína es un derivado de la cisteína en el que un grupo acetilo está unido al átomo de nitrógeno. Este compuesto se vende como suplemento dietético y se utiliza como antídoto en casos de sobredosis de paracetamol . [49]
Las ovejas necesitan cisteína para producir lana. Es un aminoácido esencial que se ingiere de su alimentación. Como consecuencia, durante condiciones de sequía, las ovejas producen menos lana; sin embargo, se han desarrollado ovejas transgénicas que pueden producir su propia cisteína. [50]
Al ser multifuncional, la cisteína sufre una variedad de reacciones. Se ha prestado mucha atención a la protección del grupo sulfhidrilo. [51] La metilación de la cisteína da S-metilcisteína . El tratamiento con formaldehído da la tiazolidina tioprolina . La cisteína forma una variedad de complejos de coordinación tras el tratamiento con iones metálicos. [52]
En comparación con la mayoría de los demás aminoácidos, la cisteína es mucho más tóxica. [53]
En 1884, el químico alemán Eugen Baumann descubrió que cuando la cistina era tratada con un agente reductor, ésta se revelaba como un dímero de un monómero al que llamó "cisteína". [54]
...clorhidrato de L-cisteína o monohidrato de clorhidrato. No se puede utilizar cabello humano como fuente de esta sustancia.
...ANEXO II LISTA DE SUSTANCIAS PROHIBIDAS EN PRODUCTOS COSMÉTICOS...416 Células, tejidos o productos de origen humano
{{cite journal}}: Verifique los valores de fecha en: |date=( ayuda )Mantenimiento CS1: formato PMC ( enlace ){{cite journal}}: Verifique los valores de fecha en: |date=( ayuda ){{cite journal}}: Mantenimiento CS1: formato PMC ( enlace ){{cite journal}}: Verifique los valores de fecha en: |date=( ayuda ){{cite journal}}: Verifique los valores de fecha en: |date=( ayuda )