Fotoquímica
La fotoquímica puede ser introducida como una reacción que procede con la absorción de luz.
Para que esta reacción se lleve a cabo debe ser suministrada energía de activación.
Otros términos importantes para la fotoquímica son: Fotones, absorción y emisión (transiciones electrónicas), el principio de Franck-Condon, los niveles de energía, el espín, la conversión interna, el efecto fotoeléctrico y el efecto Compton.
La primera ley de la fotoquímica, conocida como Ley de Grotthuss-Draper (por los químicos Theodor Grotthuss y John W. Draper), establece que la luz debe ser absorbida por una sustancia química para que se produzca una reacción fotoquímica.
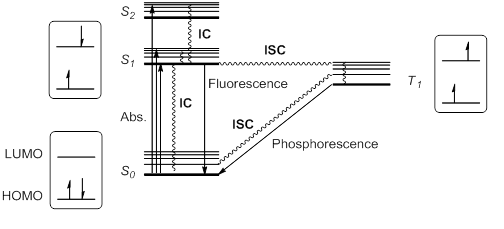
[2][3] Cuando una molécula o átomo en estado básico (S0) absorbe luz, un electrón es excitado a un nivel orbital superior.
La regla de Kasha estipula que los estados singlete superiores se relajarían rápidamente por desintegración sin radiación o conversión interna (CI) a S1.
Estas especies excitadas, ya sean S1 o T1, tienen un orbital de baja energía medio vacío y, en consecuencia, son más oxidantes que el estado básico.
Pero, al mismo tiempo, tienen un electrón en un orbital de alta energía y, por tanto, son más reductores.
Alternativamente, los haces láser suelen ser monocromáticos (aunque pueden obtenerse dos o más longitudes de onda utilizando óptica no lineal) y los LEDs tienen una banda relativamente estrecha que puede utilizarse eficazmente, así como las lámparas Rayonet, para obtener haces aproximadamente monocromáticos.
La gran relación superficie/volumen de un microreactor maximiza la iluminación, y al mismo tiempo permite un enfriamiento eficiente, lo que disminuye los productos térmicos secundarios.
Si se emplea luz láser, es posible excitar selectivamente una molécula para producir un estado electrónico y vibracional deseado.
El espectro electromagnético es amplio, sin embargo, un fotoquímico se encontrará trabajando con algunas regiones clave.
La ventaja de la fotoquímica es que proporciona una vía directa y rápida para la reacción química.
Se dice que las molécula de oxígeno en la reacción en el ambiente ha sido descompuesta fotoquímicamente o bien ha sufrido una fotólisis.
Dentro de las reacciones fotoquímicas encontramos que se rige por una serie de leyes fundamentales como: Dentro de las tecnologías aplicadas a las reacciones fotoquímicas encontramos que estas tecnologías se basan en los efectos determinados por la luz en determinadas sustancias químicas mediante procedimientos pertenecientes a fenómenos físicos como la óptica y procedimientos mecánicos como el obturador.
Por lo general, las reacciones post-columna fotólisis son explotados en la CE, donde se somete a la disociación del analito para formar entidades electroactivos.
Por ejemplo, los compuestos orgánicos nitrados producir el anión nitrito, que se oxida en un electrodo de carbón vítreo para formar nitrato.
Química ambiental colin baird university of westerm ontario editorial reverté S.A.pag.33 y 91 Química medioambiental segunda edición, thomas G. spiro princeton university, william M. stigliani editorial pearson prentice hall.
Sciencedirect.com http://www.sciencedirect.com/science?_ob=ArticleURL&_udi=B6TF4-4XFPR28-1&_user=3179229&_coverDate=01%2F04%2F2010&_alid=1296986363&_rdoc=1&_fmt=high&_orig=search&_cdi=5216&_sort=r&_docanchor=&view=c&_ct=68707&_acct=C000059970&_version=1&_urlVersion=0&_userid=3179229&md5=885f0886a653acd7067615fcabc34502 (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
En inglés: http://www.sciencedirect.com/science?_ob=ArticleListURL&_method=list&_ArticleListID=1349569680&_sort=r&view=c&_acct=C000050221&_version=1&_urlVersion=0&_userid=10&md5=396003de1e7d98e74a978eca97bc8ca5 (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).