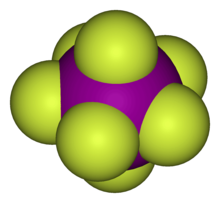
Hipervalencia
[1] Existen algunas clases específicas de moléculas hipervalentes: Dado que las moléculas hipervalentes no parecen obedecer la regla del octeto, se han propuesto algunos modelos para describir las propiedades del enlace.
Por otra parte, Gilbert N. Lewis, su oponente en aquel entonces, creía en la expansión del octeto.
Sin embargo, avances en el estudio de cálculos ab initio han revelado que la contribución de los orbitales d al enlace hipervalente es demasiado pequeña para describir las propiedades del enlace, y esta descripción por orbitales híbridos es vista como muy poco importante.
Este modelo en el que se preserva la regla del octeto también es defendido por Musher.
"[6] Para moléculas hipercoordinadas con ligandos electronegativos como el PF5 se ha demostrado que los ligandos atraen hacia sí suficiente densidad electrónica del átomo central, tal que el contenido neto es nuevamente 8 electrones o menos.