Efecto trans
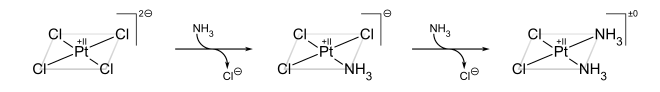
[3] A partir del PtCl42−, el primer ligando NH3 se agrega a cualquiera de las cuatro posiciones equivalentes al azar.
Sin embargo, dado que el Cl− tiene un mayor efecto trans que el NH3, el segundo NH3 se adiciona trans al Cl− y, por lo tanto, cis al primer NH3: Si, por otro lado, uno comienza con Pt(NH3)42+, el producto trans se obtiene en su lugar: En química de coordinación, se denomina efecto trans termodinámico o estructural o influencia trans, al efecto de un ligando sobre las propiedades del estado fundamental (longitud de enlace, espectro IR...) sobre un ligando que está en posición trans con respecto a él.
El efecto estructural trans puede cuantificarse experimentalmente mediante cristalografía de rayos X, y se observa en forma de alargamiento del enlace entre el metal y el ligando ubicado en la posición trans de un ligando que induce un efecto trans.
Se observa un alargamiento de hasta 20 μm con los ligandos que inducen el efecto trans más fuerte, como el ion hidruro.
Se han propuesto modelos a partir de sus orbitales atómicos.