Criptoquiralidad
Por ejemplo, el alcano 5-etil-5-propilundecano que se encuentra en ciertas especies de Phaseolus vulgaris es quiral en su carbono cuaternario central, pero ninguna forma enantiomérica tiene una rotación óptica observable:[1] Todavía es posible distinguir entre los dos enantiómeros usándolos en la síntesis asimétrica de otro químico cuya naturaleza estereoquímica se puede medir.
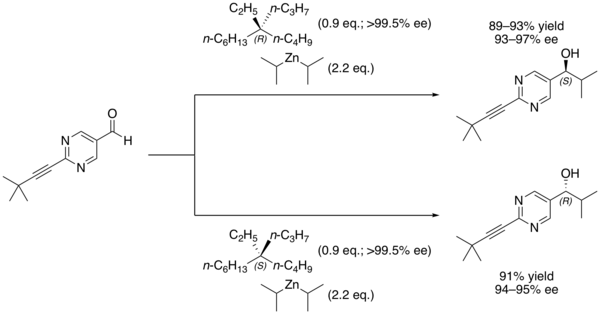
Por ejemplo, la reacción Soai de 2-(3,3-dimetilbut-1-inil)pirimidina-5-carbaldehído con diisopropilzinc realizada en presencia de 5-etil-5-propilundecano forma un alcohol secundario con un alto exceso enantiomérico basado en el enantiómero principal del alcano que se utilizó.
Incluso un ligero exceso enantiomérico del alcano se amplifica rápidamente debido a su naturaleza autocatalítica.
La criptoquiralidad también ocurre en sistemas poliméricos que crecen a partir de iniciadores quirales, por ejemplo, en dendrímeros que tienen lóbulos de diferentes tamaños unidos a un núcleo central.
[2] El término también se utiliza para describir una situación en la que un exceso enantiomérico se encuentra muy por debajo del horizonte de observación, pero sigue siendo relevante, por ejemplo, en reacciones autoamplificadoras altamente enantiosensibles.