La dualidad onda-partícula es el concepto en mecánica cuántica de que las entidades cuánticas exhiben propiedades de partícula u onda según las circunstancias experimentales. [1] : 59 Expresa la incapacidad de los conceptos clásicos como partícula u onda para describir completamente el comportamiento de los objetos cuánticos. [2] : III:1-1 Durante el siglo XIX y principios del XX, se descubrió que la luz se comportaba como una onda y luego se descubrió que tenía un comportamiento de partículas, mientras que los electrones se comportaban como partículas en los primeros experimentos y luego se descubrió que tenían un comportamiento ondulatorio. El concepto de dualidad surgió para nombrar estas aparentes contradicciones.
A finales del siglo XVII, Sir Isaac Newton había defendido que la luz eran partículas, pero Christiaan Huygens adoptó un enfoque ondulatorio opuesto. [3] Los experimentos de interferencia de Thomas Young en 1801 y la detección de la mancha de Poisson por François Arago en 1819 validaron los modelos de ondas de Huygen. Sin embargo, el modelo ondulatorio fue cuestionado en 1901 por la ley de Planck para la radiación del cuerpo negro . [4] Max Planck derivó heurísticamente una fórmula para el espectro observado suponiendo que un oscilador hipotético cargado eléctricamente en una cavidad que contenía radiación de cuerpo negro solo podía cambiar su energía en un incremento mínimo, E , que era proporcional a la frecuencia de su onda electromagnética asociada . En 1905 Einstein interpretó el efecto fotoeléctrico también con energías discretas para los fotones. [5] Ambos indican el comportamiento de las partículas. A pesar de la confirmación de varias observaciones experimentales, la teoría de los fotones (como llegó a llamarse) siguió siendo controvertida hasta que Arthur Compton realizó una serie de experimentos entre 1922 y 1924 para demostrar el impulso de la luz. [6] : 211 La evidencia experimental del momento y la energía similares a las partículas aparentemente contradecía el trabajo anterior que demostraba la interferencia ondulatoria de la luz.
La evidencia contradictoria de los electrones llegó en el orden opuesto. Muchos experimentos de JJ Thomson , [6] : I:361 Robert Millikan , [6] : I:89 y Charles Wilson [6] : I:4 entre otros habían demostrado que los electrones libres tenían propiedades de partículas, por ejemplo, la medición de su masa por Thompson en 1897. [7] En 1924, Louis de Broglie introdujo su teoría de las ondas de electrones en su tesis doctoral Recherches sur la théorie des quanta . [8] Sugirió que un electrón alrededor de un núcleo podría considerarse como una onda estacionaria y que los electrones y toda la materia podrían considerarse ondas. Fusionó la idea de pensar en ellas como partículas y de pensar en ellas como ondas. Propuso que las partículas son haces de ondas ( paquetes de ondas ) que se mueven con una velocidad de grupo y tienen una masa efectiva . Ambos dependen de la energía, que a su vez se conecta con el vector de onda y la formulación relativista de Albert Einstein unos años antes.
Siguiendo la propuesta de De Broglie de la dualidad onda-partícula de los electrones, entre 1925 y 1926, Erwin Schrödinger desarrolló la ecuación ondulatoria del movimiento de los electrones. Esto rápidamente pasó a formar parte de lo que Schrödinger llamó mecánica ondulatoria , [9] ahora llamada ecuación de Schrödinger y también "mecánica ondulatoria".
En 1926, Max Born dio una charla en una reunión de Oxford sobre el uso de experimentos de difracción de electrones para confirmar la dualidad onda-partícula de los electrones. En su charla, Born citó datos experimentales de Clinton Davisson en 1923. Sucedió que Davisson también asistió a esa charla. Davisson regresó a su laboratorio en los EE. UU. para cambiar su enfoque experimental y probar la propiedad ondulatoria de los electrones. [10]
En 1927, dos experimentos confirmaron empíricamente la naturaleza ondulatoria de los electrones. El experimento Davisson-Germer en Bell Labs midió electrones dispersos desde superficies metálicas de Ni . [11] [12] [13] [14] [15] George Paget Thomson y Alexander Reid de la Universidad de Cambridge dispersaron electrones a través de finas películas metálicas y observaron anillos de difracción concéntricos. [16] Alexander Reid, que era estudiante de posgrado de Thomson, realizó los primeros experimentos, [17] pero murió poco después en un accidente de motocicleta [18] y rara vez se lo menciona. Estos experimentos fueron seguidos rápidamente por el primer modelo de difracción de electrones no relativista de Hans Bethe [19] basado en la ecuación de Schrödinger , que es muy similar a cómo se describe ahora la difracción de electrones. Significativamente, Davisson y Germer notaron [14] [15] que sus resultados no podían interpretarse utilizando el enfoque de la ley de Bragg ya que las posiciones eran sistemáticamente diferentes; el enfoque de Bethe, [19] que incluye la refracción debida al potencial medio, arrojó resultados más precisos. Davisson y Thomson recibieron el Premio Nobel en 1937 por la verificación experimental de la propiedad ondulatoria de los electrones mediante experimentos de difracción. [20] Otto Stern llevó a cabo experimentos similares de difracción de cristales en la década de 1930 utilizando haces de átomos de helio y moléculas de hidrógeno. Estos experimentos verificaron además que el comportamiento ondulatorio no se limita a los electrones y es una propiedad general de la materia a escala microscópica.
Antes de continuar, es fundamental introducir algunas definiciones de ondas y partículas tanto en el sentido clásico como en la mecánica cuántica. Las ondas y las partículas son dos modelos muy diferentes de sistemas físicos, cada uno con una gama excepcionalmente amplia de aplicaciones. Las ondas clásicas obedecen a la ecuación de onda ; tienen valores continuos en muchos puntos del espacio que varían con el tiempo; su extensión espacial puede variar con el tiempo debido a la difracción y muestran interferencia de ondas . Los sistemas físicos que exhiben un comportamiento ondulatorio y se describen mediante las matemáticas de ecuaciones ondulatorias incluyen ondas de agua , ondas sísmicas , ondas sonoras , ondas de radio y más.
Las partículas clásicas obedecen a la mecánica clásica ; tienen algún centro de masa y extensión; siguen trayectorias caracterizadas por posiciones y velocidades que varían en el tiempo; en ausencia de fuerzas sus trayectorias son rectas. Estrellas , planetas , naves espaciales , pelotas de tenis , balas , granos de arena : los modelos de partículas funcionan a gran escala. A diferencia de las ondas, las partículas no presentan interferencias.
Algunos experimentos con sistemas cuánticos muestran interferencias y difracciones ondulatorias; algunos experimentos muestran colisiones similares a partículas.
Los sistemas cuánticos obedecen a ecuaciones de onda que predicen distribuciones de probabilidad de partículas. Estas partículas están asociadas con valores discretos llamados cuantos para propiedades como el espín , la carga eléctrica y el momento magnético . Estas partículas llegan una a la vez, al azar, pero forman un patrón. La probabilidad de que los experimentos midan partículas en un punto del espacio es el cuadrado de una onda valorada en números complejos. Se pueden diseñar experimentos para exhibir difracción e interferencia de la amplitud de probabilidad . [1] Por lo tanto, un número estadísticamente grande de apariciones aleatorias de partículas puede mostrar propiedades ondulatorias. Ecuaciones similares gobiernan excitaciones colectivas llamadas cuasipartículas .
El experimento de la doble rendija del electrón es una demostración de libro de texto de la dualidad onda-partícula. [2] En la siguiente figura se muestra esquemáticamente una versión moderna del experimento.
Los electrones de la fuente chocan contra una pared con dos finas rendijas. Una máscara detrás de las rendijas puede exponer una o abrirse para exponer ambas rendijas. Los resultados para una alta intensidad de electrones se muestran a la derecha, primero para cada rendija individualmente y luego con ambas rendijas abiertas. Con cualquiera de las rendijas abiertas hay una suave variación de intensidad debido a la difracción. Cuando ambas rendijas están abiertas la intensidad oscila, característica de la interferencia de ondas.
Habiendo observado el comportamiento de las ondas, ahora cambie el experimento, reduciendo la intensidad de la fuente de electrones hasta que solo se detecten uno o dos por segundo, que aparecen como partículas individuales, puntos en el video. Como se muestra en el clip de película a continuación, los puntos en el detector parecen al principio aleatorios. Después de un tiempo, emerge un patrón que eventualmente forma una secuencia alterna de bandas claras y oscuras.
El experimento muestra que la interferencia de ondas reveló una sola partícula a la vez: los electrones de la mecánica cuántica muestran un comportamiento tanto de onda como de partícula. Se han mostrado resultados similares para átomos e incluso moléculas grandes. [22]
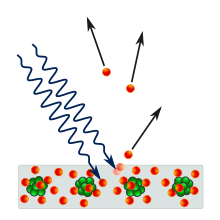
Mientras que se pensaba que los electrones eran partículas hasta que se descubrieron sus propiedades ondulatorias; para los fotones fue todo lo contrario. En 1887, Heinrich Hertz observó que cuando la luz con suficiente frecuencia incide sobre una superficie metálica, la superficie emite rayos catódicos , lo que ahora se llaman electrones. [23] : 399 En 1902, Philipp Lenard descubrió que la energía máxima posible de un electrón expulsado no está relacionada con su intensidad . [24] Esta observación está en desacuerdo con el electromagnetismo clásico, que predice que la energía del electrón debe ser proporcional a la intensidad de la radiación incidente. [25] : 24 En 1905, Albert Einstein sugirió que la energía de la luz debe ocurrir en un número finito de cuantos de energía. [26] Postuló que los electrones pueden recibir energía de un campo electromagnético sólo en unidades discretas (cuantos o fotones): una cantidad de energía E que estaba relacionada con la frecuencia f de la luz por

donde h es la constante de Planck (6,626×10 −34 J⋅s). Sólo los fotones de una frecuencia suficientemente alta (por encima de un cierto valor umbral que es la función de trabajo ) podrían liberar un electrón. Por ejemplo, los fotones de luz azul tenían suficiente energía para liberar un electrón del metal que utilizaba, pero los fotones de luz roja no. Un fotón de luz por encima de la frecuencia umbral sólo podría liberar un electrón; cuanto mayor es la frecuencia de un fotón, mayor es la energía cinética del electrón emitido, pero ninguna cantidad de luz por debajo de la frecuencia umbral podría liberar un electrón. A pesar de la confirmación de varias observaciones experimentales, la teoría de los fotones (como se la llamó más tarde) siguió siendo controvertida hasta que Arthur Compton realizó una serie de experimentos entre 1922 y 1924 para demostrar el impulso de la luz. [6] : 211
Tanto las energías discretas (cuantizadas) como el momento son, clásicamente, atributos de partículas. Hay muchos otros ejemplos en los que los fotones muestran propiedades de tipo partícula, por ejemplo en las velas solares , donde la luz solar podría impulsar un vehículo espacial y el enfriamiento por láser, donde el impulso se utiliza para frenar (enfriar) los átomos. Estos son un aspecto diferente de la dualidad onda-partícula.
Normalmente, el momento angular se considera una propiedad similar a una partícula, por ejemplo, una peonza. Sin embargo, las ondas de luz pueden tener momento angular cuando forman un vórtice, [27] como se ilustra en la Figura. También se han producido ondas electrónicas con momento angular [28] , con hasta mil cuantos de momento angular. [29] Estas ondas de materia se difractarán e interferirán, al mismo tiempo que tendrán un momento angular similar a una partícula, por lo que interactuarán con campos magnéticos, de manera similar a un bucle de corriente.
En un experimento de "en qué dirección", se colocan detectores de partículas en las rendijas para determinar por qué rendija viajó el electrón. Cuando se insertan estos detectores, la mecánica cuántica predice que el patrón de interferencia desaparece porque la parte detectada de la onda del electrón ha cambiado (pérdida de coherencia ). [2] Se han hecho muchas propuestas similares y muchas se han convertido en experimentos y se han probado. [30] Todos y cada uno de ellos muestran el mismo resultado: tan pronto como se detectan las trayectorias de los electrones, la interferencia desaparece.
Un ejemplo sencillo de estos experimentos de "en qué dirección" utiliza un interferómetro Mach-Zehnder , un dispositivo basado en láseres y espejos que se muestra a continuación. [31]

Un rayo láser a lo largo del puerto de entrada se divide en un espejo semiplateado. Parte del haz continúa recto, pasa a través de un desfasador de vidrio y luego se refleja hacia abajo. La otra parte del haz se refleja en el primer espejo y luego gira hacia otro espejo. Los dos haces se encuentran en un segundo divisor de haz semiplateado.
Cada puerto de salida tiene una cámara para registrar los resultados. Los dos haces muestran interferencias características de la propagación de ondas. Si la intensidad del láser se reduce lo suficiente, aparecen puntos individuales en las cámaras, formando el patrón como en el ejemplo del electrón. [31]
El primer espejo divisor de haz actúa como rendijas dobles, pero en el caso del interferómetro podemos quitar el segundo divisor de haz. Luego, el haz que se dirige hacia abajo termina en el puerto de salida 1: cualquier partícula de fotones en este camino se cuenta en ese puerto. El haz que atraviesa la parte superior termina en el puerto de salida 2. En cualquier caso, los recuentos seguirán las trayectorias de los fotones. Sin embargo, tan pronto como se retira el segundo divisor de haz, el patrón de interferencia desaparece. [31]