
El tetracloruro de titanio es el compuesto inorgánico de fórmula TiCl 4 . Es un intermediario importante en la producción de titanio metálico y el pigmento dióxido de titanio . TiCl 4 es un líquido volátil . Al entrar en contacto con el aire húmedo, forma espesas nubes de dióxido de titanio ( TiO 2 ) y ácido clorhídrico , reacción que antiguamente se aprovechaba para su uso en máquinas de humo. A veces se le denomina “cosquillas” o “cosquillas 4”, como representación fonética de los símbolos de su fórmula molecular ( TiCl 4 ). [7] [8]
El TiCl 4 es un líquido denso e incoloro, aunque las muestras crudas pueden ser de color amarillo o incluso marrón rojizo. Es uno de los raros haluros de metales de transición que es líquido a temperatura ambiente, siendo el VCl 4 otro ejemplo. Esta propiedad refleja el hecho de que las moléculas de TiCl 4 se autoasocian débilmente. La mayoría de los cloruros metálicos son polímeros , en los que los átomos de cloruro forman puentes entre los metales. Su punto de fusión es similar al del CCl 4 . [9] [10]
El Ti 4+ tiene una capa electrónica "cerrada", con el mismo número de electrones que el gas noble argón . La estructura tetraédrica del TiCl 4 es consistente con su descripción como un centro metálico ad 0 ( Ti 4+ ) rodeado por cuatro ligandos idénticos. Esta configuración conduce a estructuras altamente simétricas , de ahí la forma tetraédrica de la molécula. TiCl 4 adopta estructuras similares a TiBr 4 y TiI 4 ; Los tres compuestos comparten muchas similitudes. TiCl 4 y TiBr 4 reaccionan para dar haluros mixtos TiCl 4− x Br x , donde x = 0, 1, 2, 3, 4. Las mediciones de resonancia magnética también indican que el intercambio de haluro también es rápido entre TiCl 4 y VCl 4 . [11]
TiCl 4 es soluble en tolueno y clorocarbonos . Ciertos arenos forman complejos del tipo [(C 6 R 6 )TiCl 3 ] + . [12] El TiCl 4 reacciona exotérmicamente con disolventes donantes como el THF para dar aductos hexacoordinados . [13] Los ligandos más voluminosos (L) dan aductos pentacoordinados TiCl 4 L .
El TiCl 4 se produce mediante el proceso de cloruro , que implica la reducción de minerales de óxido de titanio, típicamente ilmenita ( FeTiO 3 ), con carbono bajo cloro que fluye a 900 °C. Las impurezas se eliminan por destilación . [10]
La coproducción de FeCl 3 es indeseable, lo que ha motivado el desarrollo de tecnologías alternativas. En lugar de utilizar directamente ilmenita, se utiliza "escoria de rutilo". Este material, una forma impura de TiO 2 , se deriva de la ilmenita mediante la eliminación del hierro, ya sea mediante reducción de carbono o extracción con ácido sulfúrico . El TiCl 4 crudo contiene una variedad de otros haluros volátiles, incluido el cloruro de vanadilo ( VOCl 3 ), el tetracloruro de silicio ( SiCl 4 ) y el tetracloruro de estaño ( SnCl 4 ), que deben separarse. [10]
El suministro mundial de titanio metálico, unas 250.000 toneladas al año, se fabrica a partir de TiCl 4 . La conversión implica la reducción del tetracloruro con magnesio metálico. Este procedimiento se conoce como proceso de Kroll : [14]
En el proceso Hunter , el sodio líquido es el agente reductor en lugar del magnesio. [15]
Alrededor del 90% de la producción de TiCl 4 se utiliza para fabricar el pigmento dióxido de titanio ( TiO 2 ). La conversión implica la hidrólisis de TiCl 4 , un proceso que forma cloruro de hidrógeno : [14]
En algunos casos, el TiCl 4 se oxida directamente con oxígeno :
Se ha utilizado para producir cortinas de humo , ya que produce un humo blanco y denso que tiene poca tendencia a ascender. "Tickle" era el medio estándar para producir efectos de humo en el set de películas, antes de ser eliminado gradualmente en la década de 1980 debido a preocupaciones sobre los efectos del HCl hidratado en el sistema respiratorio. [dieciséis]
El tetracloruro de titanio es un reactivo versátil que forma diversos derivados, incluidos los que se ilustran a continuación. [17]
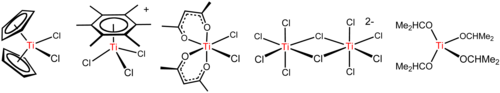
Una reacción característica del TiCl 4 es su fácil hidrólisis , señalada por la liberación de vapores de HCl y óxidos y oxicloruros de titanio . El tetracloruro de titanio se ha utilizado para crear cortinas de humo navales , ya que el aerosol de ácido clorhídrico y el dióxido de titanio que se forma dispersan la luz de manera muy eficiente. Sin embargo, este humo es corrosivo. [10]
Los alcoholes reaccionan con TiCl 4 para dar alcóxidos con la fórmula [Ti(OR) 4 ] n (R = alquilo , n = 1, 2, 4). Como indica su fórmula, estos alcóxidos pueden adoptar estructuras complejas que van desde monómeros hasta tetrámeros. Estos compuestos son útiles en la ciencia de los materiales y en la síntesis orgánica . Un derivado bien conocido es el isopropóxido de titanio , que es un monómero. El dicloruro de bis(acetilacetonato) de titanio resulta del tratamiento del tetracloruro de titanio con un exceso de acetilacetona : [18]
Las aminas orgánicas reaccionan con TiCl 4 para dar complejos que contienen complejos amido ( que contienen R 2 N − ) e imido ( que contienen RN 2− ). Con el amoníaco se forma nitruro de titanio . Una reacción ilustrativa es la síntesis de tetrakis(dimetilamido)titanio Ti(N(CH 3 ) 2 ) 4 , un líquido amarillo soluble en benceno: [19] Esta molécula es tetraédrica, con centros de nitrógeno planos. [20]
TiCl 4 es un ácido de Lewis como lo implica su tendencia a hidrolizarse . Con el éter THF , el TiCl 4 reacciona para dar cristales amarillos de TiCl 4 (THF) 2 . Con las sales de cloruro, el TiCl 4 reacciona para formar secuencialmente [Ti 2 Cl 9 ] − , [Ti 2 Cl 10 ] 2 − (ver figura anterior) y [TiCl 6 ] 2 − . [21] La reacción de los iones cloruro con TiCl 4 depende del contraión. [N(CH 2 CH 2 CH 2 CH 3 ) 4 ]Cl y TiCl 4 dan el complejo pentacoordinado [N(CH 2 CH 2 CH 2 CH 3 ) 4 ][TiCl 5 ] , mientras que [N(CH 2 CH 3 ) más pequeño ) 4 ] + da [N(CH 2 CH 3 ) 4 ] 2 [Ti 2 Cl 10 ] . Estas reacciones resaltan la influencia de la electrostática en las estructuras de compuestos con enlaces altamente iónicos.
La reducción de TiCl 4 con aluminio da como resultado una reducción de un electrón. El tricloruro ( TiCl 3 ) y el tetracloruro tienen propiedades contrastantes: el tricloruro es un sólido coloreado, es un polímero de coordinación y es paramagnético . Cuando la reducción se realiza en solución de THF , el producto Ti(III) se convierte en el aducto azul claro TiCl 3 (THF) 3 .
La química organometálica del titanio normalmente comienza con TiCl 4 . Una reacción importante implica el ciclopentadienilo de sodio para dar dicloruro de titanoceno , TiCl 2 (C 5 H 5 ) 2 . Este compuesto y muchos de sus derivados son precursores de los catalizadores de Ziegler-Natta . El reactivo de Tebbe , útil en química orgánica, es un derivado del titanoceno que contiene aluminio y que surge de la reacción del dicloruro de titanoceno con trimetilaluminio . Se utiliza para las reacciones de "olefinación". [17]
Los arenos , como C 6 (CH 3 ) 6 , reaccionan para dar los complejos piano-taburete [Ti(C 6 R 6 )Cl 3 ] + (R = H, CH 3 ; consulte la figura anterior). Esta reacción ilustra la alta acidez de Lewis del TiCl . +3entidad, que se genera por extracción de cloruro de TiCl 4 por AlCl 3 . [12]
El TiCl 4 encuentra uso ocasional en la síntesis orgánica , aprovechando su acidez de Lewis , su oxofilicidad y las propiedades de transferencia de electrones de sus haluros de titanio reducidos. Se utiliza en la adición de aldol catalizada por ácido de Lewis [22] . La clave para esta aplicación es la tendencia del TiCl 4 a activar aldehídos (RCHO) mediante la formación de aductos como (RCHO)TiCl 4 OC(H)R . [23]
Los peligros que plantea el tetracloruro de titanio generalmente surgen de su reacción con el agua que libera ácido clorhídrico , que en sí mismo es muy corrosivo y cuyos vapores también son extremadamente irritantes. TiCl 4 es un ácido de Lewis fuerte , que forma exotérmicamente aductos incluso con bases débiles como THF y agua.
{{cite web}}: Mantenimiento CS1: copia archivada como título ( enlace ) Universidad Estatal de Iowa : "Hojas de datos de seguridad de materiales químicos"{{cite book}}: |journal=ignorado ( ayuda )