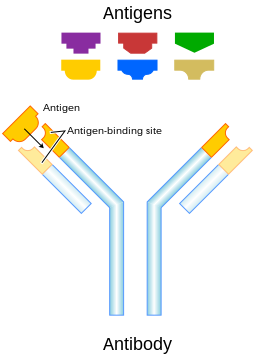
En inmunología , un antígeno ( Ag ) es una molécula , fracción , materia particulada extraña o un alérgeno , como el polen , que puede unirse a un anticuerpo específico o un receptor de células T. [1] La presencia de antígenos en el cuerpo puede desencadenar una respuesta inmunitaria . [2]
Los antígenos pueden ser proteínas , péptidos (cadenas de aminoácidos), polisacáridos (cadenas de azúcares simples), lípidos o ácidos nucleicos . [3] [4] Los antígenos existen en células normales , células cancerosas , parásitos , virus , hongos y bacterias . [1] [3]
Los antígenos son reconocidos por receptores de antígenos, incluidos los anticuerpos y los receptores de células T. [3] Las células del sistema inmunitario producen diversos receptores de antígenos de modo que cada célula tiene una especificidad para un solo antígeno. [3] Tras la exposición a un antígeno, solo los linfocitos que reconocen ese antígeno se activan y se expanden, un proceso conocido como selección clonal . [4] En la mayoría de los casos, los anticuerpos son específicos de antígeno , lo que significa que un anticuerpo solo puede reaccionar y unirse a un antígeno específico; en algunos casos, sin embargo, los anticuerpos pueden reaccionar de forma cruzada para unirse a más de un antígeno. La reacción entre un antígeno y un anticuerpo se denomina reacción antígeno-anticuerpo .
El antígeno puede tener su origen en el interior del organismo (" proteína propia " o "antígeno propio") o en el entorno externo ("no propio"). [2] El sistema inmunitario identifica y ataca a los antígenos externos "no propios". Los anticuerpos normalmente no reaccionan con los antígenos propios debido a la selección negativa de las células T en el timo y de las células B en la médula ósea . [5] Las enfermedades en las que los anticuerpos reaccionan con los antígenos propios y dañan las células del propio organismo se denominan enfermedades autoinmunes . [6]
Las vacunas son ejemplos de antígenos en forma inmunogénica que se administran intencionalmente a un receptor para inducir la función de memoria del sistema inmunitario adaptativo hacia los antígenos del patógeno que invade a ese receptor. La vacuna contra la gripe estacional es un ejemplo común. [7]
Paul Ehrlich acuñó el término anticuerpo ( en alemán : Antikörper ) en su teoría de la cadena lateral a finales del siglo XIX. [8] En 1899, Ladislas Deutsch (László Detre) nombró a las sustancias hipotéticas a medio camino entre los constituyentes bacterianos y los anticuerpos "sustancias antigénicas o inmunogénicas" ( en francés : chemicals immunogènes ou antigènes ). Originalmente creía que esas sustancias eran precursoras de anticuerpos, al igual que un zimógeno es un precursor de una enzima . Pero, en 1903, entendió que un antígeno induce la producción de cuerpos inmunes (anticuerpos) y escribió que la palabra antígeno es una contracción de antisomatógeno ( Immunkörperbildner ). El Oxford English Dictionary indica que la construcción lógica debería ser "anti(body)-gen". [9] El término originalmente se refería a una sustancia que actúa como generador de anticuerpos. [10]
Las células presentadoras de antígenos presentan antígenos en forma de péptidos en moléculas de histocompatibilidad . Las células T reconocen selectivamente los antígenos; dependiendo del antígeno y del tipo de molécula de histocompatibilidad, se activarán diferentes tipos de células T. Para el reconocimiento del receptor de células T (TCR), el péptido debe procesarse en pequeños fragmentos dentro de la célula y presentarse mediante un complejo mayor de histocompatibilidad (MHC). [12] El antígeno no puede provocar la respuesta inmunitaria sin la ayuda de un adyuvante inmunológico . [13] De manera similar, el componente adyuvante de las vacunas desempeña un papel esencial en la activación del sistema inmunitario innato. [14] [15]
Un inmunógeno es una sustancia antigénica (o aducto ) que es capaz de desencadenar una respuesta inmunitaria humoral (innata) o mediada por células. [16] Primero inicia una respuesta inmunitaria innata, que luego provoca la activación de la respuesta inmunitaria adaptativa. Un antígeno se une a los productos inmunorreceptores altamente variables (receptor de células B o receptor de células T) una vez que estos se han generado. Los inmunógenos son aquellos antígenos, denominados inmunogénicos , capaces de inducir una respuesta inmunitaria. [17]
A nivel molecular, un antígeno se puede caracterizar por su capacidad de unirse a los parátopos de un anticuerpo . Diferentes anticuerpos tienen el potencial de discriminar entre epítopos específicos presentes en la superficie del antígeno. Un hapteno es una molécula pequeña que solo puede inducir una respuesta inmune cuando se une a una molécula portadora más grande, como una proteína . Los antígenos pueden ser proteínas, polisacáridos, lípidos , ácidos nucleicos u otras biomoléculas. [4] Esto incluye partes (capas, cápsulas, paredes celulares, flagelos, fimbrias y toxinas) de bacterias , virus y otros microorganismos . Los antígenos no propios no microbianos pueden incluir polen, clara de huevo y proteínas de tejidos y órganos trasplantados o en la superficie de células sanguíneas transfundidas.
Los antígenos se pueden clasificar según su fuente.
Los antígenos exógenos son antígenos que han entrado en el cuerpo desde el exterior, por ejemplo, por inhalación , ingestión o inyección . La respuesta del sistema inmunitario a los antígenos exógenos suele ser subclínica. Por endocitosis o fagocitosis , los antígenos exógenos son absorbidos por las células presentadoras de antígenos (CPA) y procesados en fragmentos. Las CPA presentan luego los fragmentos a las células T colaboradoras ( CD4 + ) mediante el uso de moléculas de histocompatibilidad de clase II en su superficie. Algunas células T son específicas para el complejo péptido:MHC. Se activan y comienzan a secretar citocinas, sustancias que activan los linfocitos T citotóxicos (CTL), las células B secretoras de anticuerpos , los macrófagos y otras partículas.
Algunos antígenos comienzan siendo exógenos y luego se vuelven endógenos (por ejemplo, los virus intracelulares). Los antígenos intracelulares pueden volver a la circulación tras la destrucción de la célula infectada.
Los antígenos endógenos se generan dentro de las células normales como resultado del metabolismo celular normal , o debido a una infección bacteriana intracelular o viral . Luego, los fragmentos se presentan en la superficie celular en el complejo con moléculas MHC de clase I. Si las células T CD8 + citotóxicas activadas los reconocen, las células T secretan varias toxinas que causan la lisis o apoptosis de la célula infectada. Para evitar que las células citotóxicas maten células solo por presentar proteínas propias , las células citotóxicas (células T autorreactivas) se eliminan como resultado de la tolerancia (selección negativa). Los antígenos endógenos incluyen antígenos xenogénicos (heterólogos), autólogos e idiotípicos o alogénicos (homólogos). A veces, los antígenos son parte del propio huésped en una enfermedad autoinmune . [2]
Un autoantígeno es generalmente una proteína propia o un complejo proteico (y a veces ADN o ARN) que es reconocido por el sistema inmunológico de pacientes con una enfermedad autoinmune específica . En condiciones normales, estas proteínas propias no deberían ser el objetivo del sistema inmunológico, pero en las enfermedades autoinmunes, sus células T asociadas no se eliminan y, en cambio, atacan.
Los neoantígenos son aquellos que están completamente ausentes del genoma humano normal. En comparación con las proteínas propias no mutadas, los neoantígenos son relevantes para el control de tumores, ya que la calidad del grupo de células T disponible para estos antígenos no se ve afectada por la tolerancia central de las células T. La tecnología para analizar sistemáticamente la reactividad de las células T contra los neoantígenos se ha vuelto disponible recientemente. [18] Los neoantígenos se pueden detectar y cuantificar directamente. [19]
En el caso de los tumores asociados a virus, como el cáncer de cuello uterino y un subconjunto de cánceres de cabeza y cuello , los epítopos derivados de marcos de lectura abiertos virales contribuyen al conjunto de neoantígenos. [18]
Los antígenos tumorales son aquellos antígenos que son presentados pormoléculas MHC de clase I o MHC de clase II en la superficie de las células tumorales . Los antígenos que se encuentran solo en dichas células se denominan antígenos específicos de tumores (TSA) y generalmente son el resultado de una mutación específica del tumor . Más comunes son los antígenos que son presentados por células tumorales y células normales, llamados antígenos asociados a tumores (TAA). Los linfocitos T citotóxicos que reconocen estos antígenos pueden ser capaces de destruir las células tumorales. [18]
Los antígenos tumorales pueden aparecer en la superficie del tumor en forma, por ejemplo, de un receptor mutado, en cuyo caso son reconocidos por las células B. [18]
En el caso de tumores humanos sin etiología viral, se crean nuevos péptidos (neoepítopos) mediante alteraciones del ADN específicas del tumor. [18]
Una gran fracción de las mutaciones tumorales humanas son efectivamente específicas del paciente. Por lo tanto, los neoantígenos también pueden basarse en genomas tumorales individuales. Las tecnologías de secuenciación profunda pueden identificar mutaciones dentro de la parte codificante de proteínas del genoma (el exoma ) y predecir neoantígenos potenciales. En modelos de ratones, para todas las secuencias de proteínas nuevas, se predijeron péptidos de unión al MHC potenciales. El conjunto resultante de neoantígenos potenciales se utilizó para evaluar la reactividad de las células T. Los análisis basados en el exoma se explotaron en un entorno clínico, para evaluar la reactividad en pacientes tratados con terapia celular de linfocitos infiltrantes de tumores (TIL) o bloqueo de puntos de control. La identificación de neoantígenos fue exitosa para múltiples sistemas modelo experimentales y neoplasias malignas humanas. [18]
La tasa de falsos negativos en la secuenciación del exoma del cáncer es baja, es decir, la mayoría de los neoantígenos se encuentran dentro de la secuencia exónica con una cobertura suficiente. Sin embargo, la gran mayoría de las mutaciones dentro de los genes expresados no producen neoantígenos que sean reconocidos por las células T autólogas. [18]
A partir de 2015, la resolución de la espectrometría de masas es insuficiente para excluir muchos falsos positivos del conjunto de péptidos que pueden presentar las moléculas del CMH. En su lugar, se utilizan algoritmos para identificar los candidatos más probables. Estos algoritmos consideran factores como la probabilidad de procesamiento proteosomal , el transporte al retículo endoplasmático , la afinidad por los alelos relevantes de clase I del CMH y los niveles de expresión génica o traducción de proteínas. [18]
La mayoría de los neoantígenos humanos identificados en pruebas imparciales muestran una alta afinidad de unión al MHC prevista. Los antígenos de histocompatibilidad menor, una clase de antígenos conceptualmente similar, también se identifican correctamente mediante algoritmos de unión al MHC. Otro filtro potencial examina si se espera que la mutación mejore la unión al MHC. La naturaleza de los residuos centrales expuestos al TCR de los péptidos unidos al MHC está asociada con la inmunogenicidad del péptido. [18]
Un antígeno nativo es un antígeno que aún no ha sido procesado por una APC en partes más pequeñas. Las células T no pueden unirse a antígenos nativos, sino que requieren que sean procesados por APC, mientras que las células B pueden ser activadas por las células nativas.
La especificidad antigénica es la capacidad de las células huésped de reconocer un antígeno específicamente como una entidad molecular única y distinguirlo de otro con una precisión exquisita. La especificidad antigénica se debe principalmente a las conformaciones de la cadena lateral del antígeno. Es medible y no necesita ser lineal o de un paso o ecuación de velocidad limitada. [2] [7] Tanto las células T como las células B son componentes celulares de la inmunidad adaptativa . [2] [4]