
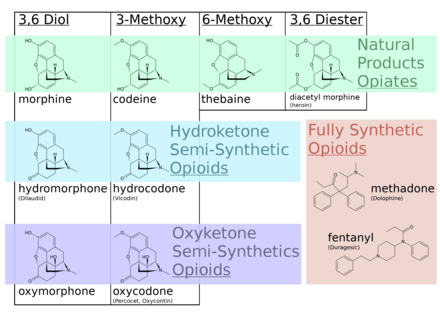
Un opiáceo es una sustancia alcaloide derivada del opio (o paja de adormidera ). [1] Tiene un significado diferente del término similar opioide , utilizado para designar todas las sustancias, tanto naturales como sintéticas, que se unen a los receptores opioides en el cerebro (incluidos los antagonistas). [2] Los opiáceos son compuestos alcaloides que se encuentran naturalmente en la planta de adormidera Papaver somniferum . [3] Los compuestos psicoactivos que se encuentran en la planta del opio incluyen morfina , codeína y tebaína . Los opiáceos se han utilizado durante mucho tiempo para una variedad de afecciones médicas, y hay evidencia de su comercio y uso para aliviar el dolor ya en el siglo VIII d.C. [4] La mayoría de los opiáceos se consideran drogas con un potencial de abuso de moderado a alto y figuran en varios "Programas de control de sustancias" en virtud de la Ley Uniforme de Sustancias Controladas de los Estados Unidos de América.
En 2014, entre 13 y 20 millones de personas consumieron opioides de forma recreativa (0,3% a 0,4% de la población mundial entre 15 y 65 años). [5] Según los CDC, de esta población hubo 47.000 muertes, con un total de 500.000 muertes entre 2000 y 2014. [6] En 2016, la Organización Mundial de la Salud informó que 27 millones de personas padecen trastorno por consumo de opioides . También informaron que en 2015, 450.000 personas murieron como resultado del consumo de drogas, y entre un tercio y la mitad de esa cifra se atribuyeron a los opioides. [7]
Los opiáceos pertenecen al gran grupo biosintético de los alcaloides de bencilisoquinolina y se denominan así porque son alcaloides naturales que se encuentran en la adormidera. Los principales opiáceos psicoactivos son la morfina , la codeína y la tebaína . La papaverina , la noscapina y aproximadamente otros 24 alcaloides también están presentes en el opio, pero tienen poco o ningún efecto sobre el sistema nervioso central humano . Los alcaloides que no tienen ningún efecto sobre el sistema nervioso central no siempre se consideraron opiáceos, pero la tendencia actual es referirse a todos los alcaloides derivados del opio o de la paja de adormidera como tales. En raras ocasiones se detectan cantidades muy pequeñas de hidrocodona e hidromorfona en los análisis del opio; parece ser producido por la planta en circunstancias y mediante procesos que no se comprenden en este momento. [ cita necesaria ] Dihidrocodeína , oximorfol , oxicodona , oximorfona , metopon Posiblemente otros derivados de la morfina y/o hidromorfona también se encuentren en pequeñas cantidades en el opio. [ cita necesaria ]
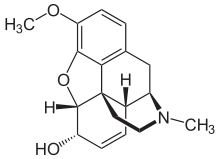
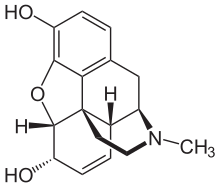
A pesar de que la morfina es el opioide de mayor importancia médica, con fines médicos se consumen mayores cantidades de codeína, la mayor parte sintetizada a partir de morfina. La codeína tiene una biodisponibilidad oral mayor y más predecible . La codeína no se metaboliza de forma fiable a su forma activa, la morfina, mediante el CYP2D6 debido a la considerable cantidad de polimorfismo. Muchas personas carecen de un metabolismo apreciable de la morfina y no experimentan efectos terapéuticos (aunque aún pueden tener náuseas, vómitos o estreñimiento). Una población importante es metabolizadores rápidos o ultrarrápidos y puede desarrollar rápidamente una toxicidad mortal incluso con la pequeña cantidad presente en la leche materna o con unas pocas dosis. Se cree ampliamente que la codeína tiene menos potencial de abuso que la morfina, a pesar de que se abusa mucho de ella. Su potencial de abuso está limitado en gran medida por su perfil de efectos adversos. [8] El uso de codeína en muchos países está disminuyendo debido a la amplia gama de metabolismo, los frecuentes efectos adversos en dosis terapéuticas (dosis de 30 a 60 mg) y en la mayoría de las personas su eficacia analgésica es comparable a una dosis terapéutica de paracetamol.

Los efectos del síndrome de abstinencia de opiáceos se asocian con el cese abrupto o la reducción del consumo prolongado de opiáceos.
La manifestación de la dependencia y el abuso de opiáceos depende de una variedad de factores, incluidas las propiedades farmacocinéticas del opiáceo y la predisposición del consumidor a la adicción. [9]
Si bien es posible la síntesis completa de opioides a partir de naftoquinona (síntesis de Gates) u otros materiales de partida orgánicos simples, se trata de procesos tediosos y antieconómicos. Por lo tanto, la mayoría de los analgésicos de tipo opiáceo que se utilizan hoy en día se extraen del Papaver somniferum o se sintetizan a partir de esos opiáceos, especialmente la tebaína . [10]
En 2015, los investigadores informaron sobre una biosíntesis exitosa de tebaína e hidrocodona utilizando levadura modificada genéticamente . Una vez adaptado para uso comercial, el proceso reduciría el tiempo de producción de un año a varios días y podría reducir los costos en un 90%. [11] [12]
La codeína es un profármaco que se convierte en morfina y actúa sobre los receptores μ -opiáceos. Se convierte en morfina mediante el metabolismo de las enzimas CYP2D6 . Es posible que las personas que tienen una menor actividad de CYP2D6 no metabolicen la codeína en absoluto y no experimenten sus efectos analgésicos. Por el contrario, las personas con actividad rápida o ultrarrápida de CYP2D6 pueden metabolizar el fármaco demasiado rápido y experimentar efectos secundarios relacionados con la dosis, como sedación y depresión respiratoria mortal. [13]
El fentanilo es un opioide de piperidina sintético estructuralmente similar a las arilpiperidinas. Es un fuerte agonista del receptor μ que es 80 a 100 veces más potente que la morfina y tiene un inicio rápido con una duración de acción más corta que la morfina debido a la redistribución desde la ubicación del SNC al tejido adiposo. Cuando se utiliza como fármaco continuo (p. ej., parches transdérmicos, uso a largo plazo de fentanilo intravenoso en pacientes de la UCI), su vida media de eliminación y la duración del efecto son más largas que las de la morfina. Se metaboliza en el hígado mediante las enzimas CYP3A4 al compuesto norfentanilo. [14]
La heroína, el nombre común de la diacetilmorfina , es el primero de varios opioides semisintéticos que se derivan de la morfina, un componente del opio natural. [16] Se forma por la acetilación de la morfina para aumentar la solubilidad en lípidos. [17] La heroína (diacetilmorfina) es un profármaco de morfina ; el hígado lo metaboliza en morfina después de su administración. Uno de los principales metabolitos de la heroína, la 6-monoacetilmorfina (6-MAM), es también un profármaco de morfina.
La hidromorfona se deriva de la morfina y puede utilizarse como alternativa. Tiene un metabolismo de primer paso elevado cuando se administra por vía oral y se glucuronida principalmente en el hígado a hidromorfona-3-glucorónido (H3G). El 75% de la hidromorfona se excreta por vía renal y el 7% se excreta como opiáceo original. [14]
La meperidina es un opiáceo sintético, que forma parte de la clase de las arilpiperidinas. Es un fuerte agonista del receptor μ con 1/10 de la potencia de la morfina. Históricamente también se ha utilizado para tratar los escalofríos y tiene una vida media de tres a cuatro horas. Se metaboliza hepáticamente a los metabolitos activos de normeperidina, ácido normepiridínico y ácido medperidínico. La normeperidina puede acumularse hasta niveles tóxicos en pacientes con insuficiencia renal con dosis repetidas y puede provocar excitación del SNC y convulsiones. [14]
La metadona tiene una mayor biodisponibilidad y vida media en comparación con la morfina. [18] Se metaboliza a un producto inactivo mediante N-desmetilación mediante enzimas CYP3A4 en el hígado. Tiene una alta variabilidad de persona a persona debido a los diferentes niveles de CYP3A4 en los individuos. [19] Está aprobado para el tratamiento del dolor moderado a intenso, así como para la dependencia de opioides. [20] Debido a su alto riesgo de interacciones medicamentosas, toxicidad hepática y variabilidad de los pacientes, los pacientes deben ser monitoreados de cerca en las clínicas de metadona . [21] Además, existe un mayor riesgo de mortalidad en pacientes tratados con metadona en comparación con otros opioides, lo que se cree que se debe a la prolongación del QTc y arritmias cardíacas.
La nicomorfina (Vilan, dinicotinato de morfina), la diamorfina (heroína, diacetato de morfina), la dipropanoilmorfina (dipropionato de morfina), la desomorfina (Permonid, di-hidro-desoximorfina), la metildesorfina , la acetilpropionilmorfina , la dibenzoilmorfina , la diacetildihidromorfina y varios otros también se derivan de morfina. [22]
La morfina se metaboliza en el hígado a morfina-3-glucurónido (M3G) y morfina-6-glucurónido (M6G) y se excreta por los riñones. También puede cruzar la barrera hematoencefálica hacia el líquido cefalorraquídeo. M6G tiene una potente actividad analgésica, se une a los receptores opioides y contribuye principalmente al beneficio terapéutico de la morfina. [23] M3G no actúa como analgésico, tiene baja afinidad por los receptores opioides y posiblemente antagonice los efectos terapéuticos de la morfina y el M6G. Además, las dosis altas de morfina y, por tanto, de M3G, se asocian con efectos secundarios neurotóxicos como hiperalgesia , alodinia y mioclonías . [24]
La oximorfona es un congénere de la morfina. Se metaboliza a 6-hidroxioximorfona y oximorfona-3-glucurónido y el 40% se excreta como metabolitos. La 6-hidroxioximorfina es activa y existe en una proporción de 1:1 con el fármaco original. Se desconoce la actividad del oximorfona-3-glucurónido. [14]
Los opiáceos con actividad opioide se utilizan principalmente para el tratamiento del dolor con la premisa de que habrá beneficios tanto para el dolor como para la función que superarán los riesgos para el paciente. [25] Otra indicación es el alivio sintomático de la dificultad para respirar , tanto en situaciones agudas (por ejemplo, edema pulmonar ) como en pacientes terminales. [26] [27]
A pesar de la escasa evidencia, a menudo contradictoria, a veces los estudios no muestran ningún beneficio, los opioides como la codeína, la hidrocodona y la hidromorfona se han utilizado tradicionalmente para el tratamiento de la tos viral aguda (también conocida como "bronquitis aguda"), la tos debida a la EPOC exacerbación, tos crónica posviral, tos crónica idiopática y tos por otras causas. Dado el potencial de abuso, los frecuentes efectos secundarios gastrointestinales y varios estudios que no muestran ningún beneficio discernible, las recomendaciones están en contra del uso de opioides para la tos en niños. A pesar del uso generalizado, la ciencia que respalda el uso de opioides para la tos en adultos es más notable por el pequeño tamaño de la muestra, el diseño deficiente del estudio y los resultados no concluyentes que sugieren que puede haber una pequeña reducción en la cantidad de tos cuando es precisamente Medido. La evidencia real de los resultados orientados al paciente (por ejemplo, si los pacientes se sienten mejor que cuando se les administra un placebo) es difícil de alcanzar, y se ha puesto en duda el uso de codeína como el "estándar de oro" para comparar otros medicamentos (como demostrar que una droga es tan buena, o al menos no peor, que una droga sin ningún beneficio y sólo efectos secundarios nocivos y un potencial de abuso deja mucho que desear). [ cita necesaria ]
Es posible que sea necesario realizar conversiones de dosis de opioides al cambiar de medicamento, dada la diferente farmacodinámica de los opioides. Generalmente, la morfina parenteral (IV o IM) se utiliza como estándar para la conversión entre opiáceos para lograr efectos analgésicos equivalentes. Estas diferencias en los equivalentes de morfina pueden diferir entre las formulaciones del mismo medicamento y, ciertamente, entre las formulaciones orales y las inyectables. [28] El cálculo de la dosis diaria total utilizando equivalentes de miligramos de morfina se utiliza para identificar a los pacientes con riesgo de sobredosis. [29]
Los efectos secundarios comunes asociados con el uso de opioides incluyen: sedación , náuseas , mareos, vómitos, estreñimiento , dependencia física, tolerancia y depresión respiratoria potencialmente fatal . De estos, los más comunes son el estreñimiento y las náuseas. No se desarrolla tolerancia al estreñimiento. [30] Esta es la razón por la que a menudo se recetan ablandadores de heces o laxantes (polietilenglicol, docusato y sen) junto con los opioides. [31]
En caso de sobredosis, ya sea intencional, accidental o debida a la rápida conversión 2D6 de codeína (o tramadol, un opioide no opiáceo que, como la codeína, tiene poco efecto intrínseco sobre los receptores μ, sino que actúa como profármaco con un metabolito activo ese es un agonista μ .
Los efectos secundarios menos comunes incluyen: retraso en el vaciamiento gástrico, hiperalgesia , disfunción inmunológica y hormonal (el hipogonadismo se observa a menudo en hombres que toman opioides crónicos, pero no siempre es clínicamente evidente), rigidez muscular y mioclonías . [32]
El uso de opiáceos para el dolor está ampliamente aceptado en el sistema sanitario. Sin embargo, el tratamiento a largo plazo para el dolor crónico es controvertido ya que existe un alto riesgo de adicción asociado con su uso, lo que lleva al abuso y el desvío hacia otros, incluso cuando se toma correctamente. [33] Los adictos a los opiáceos darán prioridad a la adquisición de estas drogas sobre otras actividades de sus vidas, lo que afectará negativamente a sus relaciones profesionales y personales. Además, no hay muchos estudios bien diseñados que evalúen la seguridad y eficacia generales. Muchos estudios pequeños que utilizan dosis pequeñas (a menudo la mitad de la dosis recomendada) no han demostrado mucho efecto, pero no se puede confiar en que brinden mucha información sobre la práctica más común de terapia gradual y aumento lento de la dosis.
Como era de esperar, el uso crónico de opioides conduce a la tolerancia y puede hacerlo con bastante rapidez (de días a semanas). Esto ocurre incluso con dosis consideradas modestas (por ejemplo, ≥25 mg de oxicodona al día). Esto puede hacer que el paciente necesite dosis más altas y/o más frecuentes del fármaco para obtener efectos eufóricos, aunque puede no ser un factor en los efectos analgésicos ya que la tolerancia a una dosis de opioide no parece estar relacionada con la pérdida de eficacia. [34] La tolerancia está asociada con la regulación positiva de los receptores μ (y posiblemente de otros).
Los efectos adversos de la dependencia de la concentración pueden variar según los polimorfismos genéticos del usuario que pueden alterar el metabolismo del fármaco. El citocromo P450 (en particular CYP2D6 , pero también CYP3A4 ) es responsable del metabolismo de varios opiáceos en metabolitos activos y las variaciones en la actividad de CYP450 conducen a niveles variables del fármaco en suero. [35]
El dolor es una experiencia sensorial y emocional desagradable asociada con un daño tisular real o potencial. Es una función defensiva esencial donde el dolor funciona como alarma para evitar o limitar el daño tisular. Su neurobiología es compleja e implica la estimulación de varios tipos diferentes de nervios. Los opioides actúan sobre los receptores opioides que están acoplados a los receptores acoplados a la proteína G inhibidora (GPCR). Estos receptores se dividen en 3 clases: receptores μ (mu) , δ (delta) y κ (kappa) . [36]
Más del 70% de los receptores opioides son receptores μ, ubicados predominantemente en las terminales centrales de los nociceptores en el asta dorsal de la médula espinal. El 30% restante de los receptores opioides se encuentran postsinápticamente en las dendritas de las neuronas e interneuronas espinotalámicas de segundo orden . [36]
Cuando un opiáceo se une como agonista al GPCR, habrá una cascada de señalización que dará como resultado la inhibición de la adenilato ciclasa y los canales iónicos de calcio con la estimulación de los canales iónicos de potasio. El efecto neto de estos cambios es una reducción del AMPc intracelular y una hiperpolarización de la célula neuronal que reduce la liberación de neurotransmisores. [37] A través de esta vía, cuando los opiáceos se unen y activan el receptor mu, hay una menor transmisión de la señalización del dolor. Esta vía apuntaba a las propiedades analgésicas por las que se conocen y utilizan los opiáceos. Otras funciones clínicamente importantes de mu son su participación en las funciones respiratorias y cardiovasculares, la peristalsis gastrointestinal , la alimentación y el estado de ánimo. [38] Estas otras vías son importantes porque explican los efectos secundarios del uso de opiáceos, como depresión respiratoria en dosis altas, estreñimiento con el uso crónico y propiedades adictivas. [32]
Las personas con las siguientes afecciones no deberían usar opioides: [39]
Los siguientes son factores de riesgo para el abuso de prescripción de opiáceos: [40]
Estadísticamente, los pacientes de mediana edad con antecedentes de uso de sustancias y comorbilidades psiquiátricas tienen mayores riesgos de mortalidad, como el suicidio.
La dependencia de drogas iatrogénica , fisiológica y psicológica, puede ocurrir en cualquier persona con cualquier origen. Algunos médicos son más liberales al recetar opiáceos y sus pacientes se vuelven dependientes de los opiáceos simplemente siguiendo las órdenes de su médico. [41]
Opiáceo es el término más antiguo utilizado clásicamente en farmacología para referirse a una droga derivada del opio. Se ha utilizado en el pasado para referirse a drogas con efectos similares al opio, pero ese uso está anticuado. Opioide, un término más moderno, se utiliza para designar todas las sustancias, tanto naturales como sintéticas, que se unen a los receptores opioides (incluidos los antagonistas).
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )