Una ligasa de ubiquitina (también llamada ligasa de ubiquitina E3 ) es una proteína que recluta una enzima conjugadora de ubiquitina E2 que se ha cargado con ubiquitina , reconoce un sustrato proteico y ayuda o cataliza directamente la transferencia de ubiquitina desde la E2 al sustrato proteico. En términos simples y más generales, la ligasa permite el movimiento de ubiquitina desde un transportador de ubiquitina a otra proteína (el sustrato) mediante algún mecanismo. La ubiquitina , una vez que llega a su destino, termina uniéndose mediante un enlace isopeptídico a un residuo de lisina , que es parte de la proteína objetivo. [2] Las ligasas E3 interactúan tanto con la proteína objetivo como con la enzima E2, y así imparten especificidad de sustrato a la E2. Comúnmente, las E3 poliubiquitinan su sustrato con cadenas de ubiquitina unidas a Lys48, dirigiendo el sustrato para su destrucción por el proteasoma . Sin embargo, son posibles muchos otros tipos de enlaces que alteran la actividad, las interacciones o la localización de una proteína. La ubiquitinación por las ligasas E3 regula diversas áreas, como el tráfico celular, la reparación del ADN y la señalización, y es de gran importancia en la biología celular. Las ligasas E3 también son actores clave en el control del ciclo celular, mediando la degradación de ciclinas , así como de proteínas inhibidoras de quinasas dependientes de ciclinas . [3] El genoma humano codifica más de 600 supuestas ligasas E3, lo que permite una enorme diversidad de sustratos. [4]
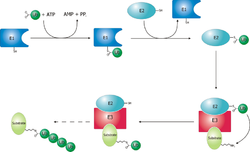
La ubiquitina ligasa se denomina E3 y funciona en conjunto con una enzima activadora de ubiquitina E1 y una enzima conjugadora de ubiquitina E2 . Existe una enzima principal, E1, compartida por todas las ubiquitina ligasas, que utiliza ATP para activar la ubiquitina para la conjugación y la transfiere a una enzima E2. La enzima E2 interactúa con un socio E3 específico y transfiere la ubiquitina a la proteína objetivo . La E3, que puede ser un complejo multiproteico , es, en general, responsable de dirigir la ubiquitinación a proteínas de sustrato específicas . [ cita requerida ]
La reacción de ubiquitinación se lleva a cabo en tres o cuatro pasos, dependiendo del mecanismo de acción de la ligasa de ubiquitina E3. En el primer paso, que es conservado, un residuo de cisteína de E1 ataca la glicina C-terminal activada por ATP de la ubiquitina, lo que da como resultado un complejo tioéster Ub-S-E1. La energía del ATP y la hidrólisis del difosfato impulsan la formación de este tioéster reactivo, y los pasos posteriores son termoneutrales. A continuación, se produce una reacción de transtiolación, en la que un residuo de cisteína de E2 ataca y reemplaza a la E1. Las ligasas de tipo dominio HECT de E3 tendrán una reacción de transtiolación más para transferir la molécula de ubiquitina a la E3, mientras que las ligasas de tipo dominio RING finger, mucho más comunes , transfieren la ubiquitina directamente de E2 al sustrato. [5] El paso final en el primer evento de ubiquitinación es un ataque del grupo amino de la lisina de la proteína objetivo, que eliminará la cisteína y formará un enlace isopeptídico estable. [6] Una notable excepción a esto es la proteína p21 , que parece estar ubiquitinada utilizando su amina N-terminal, formando así un enlace peptídico con la ubiquitina. [7]
Se estima que los seres humanos tienen entre 500 y 1000 ligasas E3, que imparten especificidad de sustrato a E1 y E2. [8] Las ligasas E3 se clasifican en cuatro familias: HECT, RING-finger, U-box y PHD-finger. [8] Las ligasas E3 RING-finger son la familia más grande y contienen ligasas como el complejo promotor de anafase (APC) y el complejo SCF ( complejo proteico Skp1 - Culin -F-box). Los complejos SCF constan de cuatro proteínas: Rbx1, Cul1, Skp1, que son invariables entre los complejos SCF, y una proteína F-box, que varía. Se han identificado alrededor de 70 proteínas F-box humanas. [9] Las proteínas F-box contienen una F-box, que se une al resto del complejo SCF, y un dominio de unión al sustrato, que le da a la E3 su especificidad de sustrato. [8]

La señalización de ubiquitina depende de la diversidad de etiquetas de ubiquitina para la especificidad de su mensaje. Una proteína puede estar etiquetada con una sola molécula de ubiquitina (monoubiquitilación) o con una variedad de diferentes cadenas de moléculas de ubiquitina (poliubiquitilación). [11] Las ligasas de ubiquitina E3 catalizan eventos de poliubiquitinación de la misma manera que el mecanismo de ubiquitinación simple, utilizando en su lugar un residuo de lisina de una molécula de ubiquitina actualmente unida a la proteína sustrato para atacar el extremo C de una nueva molécula de ubiquitina. [6] [11] Por ejemplo, una etiqueta común de 4-ubiquitina, unida a través de la lisina en la posición 48 (K48) recluta la proteína etiquetada al proteasoma y la posterior degradación. [11] Sin embargo, los siete residuos de lisina de la ubiquitina (K6, K11, K27, K29, K33, K48 y K63), así como la metionina N-terminal, se utilizan en cadenas in vivo. [11]
La monoubiquitinación se ha relacionado con las vías de endocitosis de proteínas de membrana . Por ejemplo, la fosforilación de la tirosina en la posición 1045 en el receptor del factor de crecimiento epidérmico (EGFR) puede reclutar la ligasa E3 de tipo RING c-Cbl, a través de un dominio SH2 . C-Cbl monoubiquitina el EGFR, lo que indica su internalización y tráfico al lisosoma. [12]
La monoubiquitinación también puede regular la localización de proteínas citosólicas. Por ejemplo, la ligasa E3 MDM2 ubiquitina p53 ya sea para degradación (cadena de poliubiquitina K48) o para exportación nuclear (monoubiquitinación). Estos eventos ocurren de manera dependiente de la concentración, lo que sugiere que la modulación de la concentración de la ligasa E3 es una estrategia reguladora celular para controlar la homeostasis y la localización de proteínas. [13]
Las ligasas de ubiquitina son el determinante final, y potencialmente el más importante, de la especificidad del sustrato en la ubiquitinación de proteínas . [14] Las ligasas deben distinguir simultáneamente su sustrato proteico de miles de otras proteínas en la célula y de otras formas (inactivas en la ubiquitinación) de la misma proteína. Esto se puede lograr mediante diferentes mecanismos, la mayoría de los cuales implican el reconocimiento de degrones : secuencias cortas específicas de aminoácidos o motivos químicos en el sustrato. [15]
La escisión proteolítica puede conducir a la exposición de residuos en el extremo N de una proteína. De acuerdo con la regla del extremo N , diferentes aminoácidos N-terminales (o N-degrones) son reconocidos en diferente medida por su ubiquitina ligasa apropiada (N-recognin), lo que influye en la vida media de la proteína. [16] Por ejemplo, los aminoácidos cargados positivamente ( Arg , Lys , His ) y voluminosos hidrofóbicos ( Phe , Trp , Tyr , Leu , Ile ) son reconocidos preferentemente y, por lo tanto, se consideran degrones desestabilizadores ya que permiten una degradación más rápida de sus proteínas. [17]

Un degron puede convertirse en su forma activa mediante una modificación postraduccional [19] como la fosforilación de un residuo de tirosina , serina o treonina . [20] En este caso, la ubiquitina ligasa reconoce exclusivamente la versión fosforilada del sustrato debido a la estabilización dentro del sitio de unión . Por ejemplo, FBW7 , la unidad de reconocimiento de sustrato F-box de una ubiquitina ligasa SCF FBW7 , estabiliza un sustrato fosforilado mediante la unión de hidrógeno de sus residuos de arginina al fosfato, como se muestra en la figura de la derecha. En ausencia del fosfato , los residuos de FBW7 repelen el sustrato. [18]
La presencia de oxígeno u otras moléculas pequeñas puede influir en el reconocimiento de degron. [18] La proteína von Hippel-Lindau (VHL) (parte de reconocimiento de sustrato de una ligasa E3 específica), por ejemplo, reconoce el factor inducible por hipoxia alfa (HIF-α) solo en condiciones normales de oxígeno, cuando su prolina está hidroxilada . En hipoxia , por otro lado, HIF-a no está hidroxilado, evade la ubiquitinación y, por lo tanto, opera en la célula en concentraciones más altas que pueden iniciar la respuesta transcripcional a la hipoxia. [21] Otro ejemplo de control de la degradación de proteínas por parte de moléculas pequeñas es la fitohormona auxina en las plantas. [22] La auxina se une a TIR1 (el dominio de reconocimiento de sustrato de la ligasa de ubiquitina SCF TIR1 ) aumentando la afinidad de TIR1 por sus sustratos ( represores transcripcionales : Aux/IAA) y promoviendo su degradación.
Además de reconocer aminoácidos, las ligasas de ubiquitina también pueden detectar características inusuales en sustratos que sirven como señales para su destrucción. [14] Por ejemplo, San1 (antagonista Sir 1), un control de calidad de proteína nuclear en levadura , tiene un dominio de unión al sustrato desordenado , que le permite unirse a dominios hidrofóbicos de proteínas mal plegadas . [14] Las glicoproteínas mal plegadas o en exceso sin ensamblar de la vía ERAD , por otro lado, son reconocidas por Fbs1 y Fbs2, proteínas F-box de mamíferos de las ligasas E3 SCF Fbs1 y SCF Fbs2 . [23] Estos dominios de reconocimiento tienen pequeños bolsillos hidrofóbicos que les permiten unirse a glicanos que contienen alto contenido de manosa .
Además de los degrones lineales , la ligasa E3 puede en algunos casos reconocer también motivos estructurales en el sustrato. [14] En este caso, el motivo 3D puede permitir que el sustrato relacione directamente su función bioquímica con la ubiquitinación . Esta relación se puede demostrar con la proteína TRF1 (regulador de la longitud del telómero humano ), que es reconocida por su ligasa E3 correspondiente ( FBXO4 ) a través de una interacción de lámina beta intermolecular . TRF1 no puede ser ubiquinado mientras está unido al telómero, probablemente porque el mismo dominio TRF1 que se une a su ligasa E3 también se une a los telómeros. [14]
Las ligasas de ubiquitina E3 regulan la homeostasis, el ciclo celular y las vías de reparación del ADN y, como resultado, varias de estas proteínas están involucradas en una variedad de cánceres, incluidos los famosos MDM2, BRCA1 y el supresor tumoral de Von Hippel-Lindau . [24] Por ejemplo, se ha encontrado una mutación de MDM2 en el cáncer de estómago , [25] el carcinoma de células renales , [26] y el cáncer de hígado [27] (entre otros) para desregular las concentraciones de MDM2 al aumentar la afinidad de su promotor por el factor de transcripción Sp1 , lo que provoca un aumento de la transcripción del ARNm de MDM2. [25] Hay varias técnicas experimentales basadas en la proteómica disponibles para identificar pares de ubiquitina ligasa-sustrato E3, [28] como la identificación de biotina dependiente de la proximidad (BioID), el atrapamiento de ubiquitina ligasa-sustrato y las entidades de unión a ubiquitina en tándem (TUBE).