En química orgánica , umpolung ( alemán: [ˈʔʊmˌpoːlʊŋ] ) o inversión de polaridad es la modificación química de un grupo funcional con el objetivo de invertir la polaridad de ese grupo. [1] [2] Esta modificación permite reacciones secundarias de este grupo funcional que de otro modo no serían posibles. [3] El concepto fue introducido por D. Seebach (de ahí la palabra alemana umpolung para polaridad invertida) y EJ Corey . El análisis de polaridad durante el análisis retrosintético le indica a un químico cuándo se requieren tácticas umpolung para sintetizar una molécula objetivo.
La gran mayoría de las moléculas orgánicas importantes contienen heteroátomos, que polarizan los esqueletos de carbono en virtud de su electronegatividad. Por lo tanto, en reacciones orgánicas estándar, la mayoría de los enlaces nuevos se forman entre átomos de polaridad opuesta. Este puede considerarse el modo de reactividad "normal".
Una consecuencia de esta polarización natural de las moléculas es que los esqueletos de carbono sustituidos con heteroátomos 1,3 y 1,5 son extremadamente fáciles de sintetizar ( reacción aldólica , condensación de Claisen , reacción de Michael , reordenamiento de Claisen , reacción de Diels-Alder ), mientras que 1, Es más difícil acceder a los patrones de sustitución de heteroátomos de 2, 1,4 y 1,6 mediante la reactividad "normal". Por tanto, es importante comprender y desarrollar métodos para inducir umpolung en reacciones orgánicas.
El método más sencillo para obtener patrones de sustitución de heteroátomos de 1,2, 1,4 y 1,6 es comenzar con ellos. Los procesos bioquímicos e industriales pueden proporcionar fuentes económicas de sustancias químicas que normalmente tienen patrones de sustitución inaccesibles. Por ejemplo, los aminoácidos, el ácido oxálico, el ácido succínico, el ácido adípico, el ácido tartárico y la glucosa son abundantes y proporcionan patrones de sustitución no rutinarios.
El reactivo umpolung canónico es el ion cianuro . El ion cianuro es inusual porque se esperaría que un carbono triplemente unido a un nitrógeno tuviera una polaridad (+) debido a la mayor electronegatividad del átomo de nitrógeno. Sin embargo, la carga negativa del ion cianuro está localizada en el carbono, dándole una carga formal (-). Esta ambivalencia química da como resultado la umpolung en muchas reacciones en las que interviene el cianuro.
Por ejemplo, el cianuro es un catalizador clave en la condensación de benjuí , un ejemplo clásico de inversión de polaridad.
El resultado neto de la reacción del benjuí es que se ha formado un enlace entre dos carbonos que normalmente son electrófilos.
Los carbenos N-heterocíclicos son similares al cianuro en reactividad. Al igual que el cianuro, tienen una ambivalencia química inusual, lo que les permite desencadenar reacciones en las que intervienen. El carbeno tiene seis electrones: dos en cada uno de los enlaces simples carbono-nitrógeno, dos en su orbital hibridado sp 2 y un orbital p vacío. El par solitario sp 2 actúa como donante de electrones, mientras que el orbital p vacío puede actuar como aceptor de electrones.
En este ejemplo, el carbono β del éster α,β-insaturado 1 actúa formalmente como un nucleófilo, [4] mientras que normalmente se esperaría que fuera un aceptor de Michael .

Este carbeno reacciona con el éster α,β-insaturado 1 en la posición β formando el enolato intermedio 2 . Mediante la tautomerización 2b se puede desplazar el átomo de bromo terminal a 3 . Una reacción de eliminación regenera el carbeno y libera el producto 4 .
A modo de comparación: en la reacción de Baylis-Hillman, el mismo átomo de carbono β electrófilo es atacado por un reactivo, pero provoca la activación de la posición α de la enona como nucleófilo.
Los procesos biológicos pueden emplear reactividad umpolung similar al cianuro sin tener que depender del ion cianuro tóxico. El pirofosfato de tiamina (que a su vez es un carbeno N-heterocíclico ) (TPP) cumple una función funcionalmente idéntica. El anillo de tiazolio en TPP se desprotona dentro del núcleo hidrofóbico de la enzima, [5] dando como resultado un carbeno que es capaz de umpolung.
Las enzimas que utilizan TPP como cofactor pueden catalizar la reactividad umpolung, como la descarboxilación del piruvato.
En ausencia de TPP, la descarboxilación del piruvato daría como resultado la colocación de una carga negativa en el carbono carbonilo, lo que iría en contra de la polarización normal del doble enlace carbono-oxígeno.
Los anillos de 3 miembros son restos tensos en química orgánica. Cuando un anillo de 3 miembros contiene un heteroátomo, como en un epóxido o en un intermedio de bromonio , los tres átomos del anillo se polarizan. Es imposible asignar polaridades (+) y (-) a un anillo de 3 miembros sin tener dos átomos adyacentes con la misma polaridad. Por lo tanto, siempre que un nucleófilo abre un anillo polarizado de 3 miembros, inevitablemente se produce una umpolung. [ cita necesaria ] Por ejemplo, la apertura del óxido de etileno con hidróxido conduce al etilenglicol .
La química del ditiano es un ejemplo clásico de inversión de polaridad. Esto se puede observar en la reacción de Corey-Seebach .
Normalmente, el átomo de oxígeno en el grupo carbonilo es más electronegativo que el átomo de carbono y, por lo tanto, el grupo carbonilo reacciona como un electrófilo en el carbono. Esta polaridad se puede invertir cuando el grupo carbonilo se convierte en un ditiano o un tioacetal . En terminología synthon, el grupo carbonilo ordinario es un catión acilo y el ditiano es un anión acilo enmascarado .
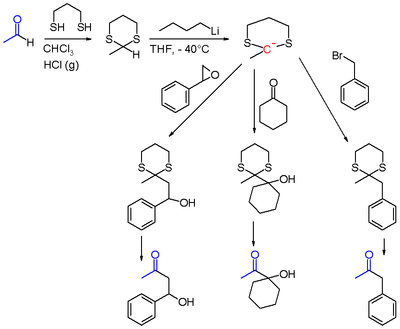
Cuando el ditiano se deriva de un aldehído como el acetaldehído, el protón acilo puede extraerse mediante n -butillitio en THF a bajas temperaturas. El 2-litio-1,3-ditiano así generado reacciona como nucleófilo en desplazamiento nucleofílico con haluros de alquilo como el bromuro de bencilo , con otros compuestos carbonílicos como la ciclohexanona u oxiranos como el fenilepoxietano, que se muestran a continuación. Después de la hidrólisis del grupo ditiano, los productos finales de la reacción son α-alquil-cetonas o α-hidroxi-cetonas . Un reactivo común para la hidrólisis del ditiano es el (bis(trifluoroacetoxi)yodo)benceno .
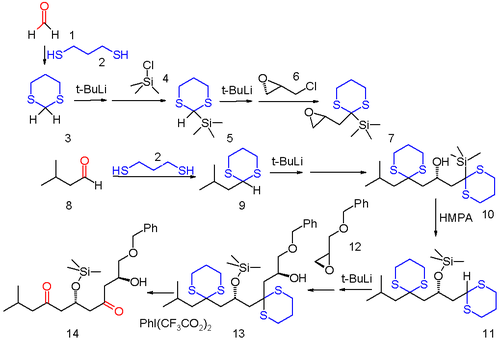
La química del ditiano abre el camino a muchas transformaciones químicas nuevas. Un ejemplo se encuentra en la llamada química de retransmisión aniónica , en la que una carga negativa de un grupo funcional aniónico resultante de una reacción orgánica se transfiere a una ubicación diferente dentro de la misma estructura de carbono y queda disponible para una reacción secundaria. [6] En este ejemplo de una reacción de múltiples componentes, tanto el formaldehído ( 1 ) como el isopropilaldehído ( 8 ) se convierten en ditianos 3 y 9 con 1,3-propanoditiol . El sulfuro 3 se silila primero mediante reacción con terc -butillitio y luego con cloruro de trimetilsililo 4 y luego se elimina el segundo protón de acilo y se hace reaccionar con (-)- epiclorhidrina 6 ópticamente activa reemplazando el cloro. Este compuesto sirve como sustrato para la reacción con el otro ditiano 9 para formar el producto de apertura del anillo de oxirano 10 . Bajo la influencia de la base polar HMPA , 10 se reordena en un reordenamiento de 1,4-Brook al éter sililo 11 reactivando el grupo formaldehído ditiano como un anión (de ahí el concepto de retransmisión aniónica). Este grupo ditiano reacciona con el oxirano 12 para formar el alcohol 13 y en el paso final los grupos sulfuro se eliminan con (bis(trifluoroacetoxi)yodo)benceno .
La táctica química de retransmisión aniónica se ha aplicado elegantemente en la síntesis total de moléculas complejas de importante actividad biológica, como la espongistatina 2 [7] y la mandelalida A. [8] [9]
Es posible formar un enlace entre dos carbonos de polaridad (-) utilizando un oxidante como el yodo . En esta síntesis total de enterolactona , [10] la relación 1,4- de los sustituyentes de oxígeno se ensambla mediante el homoacoplamiento oxidativo de un enolato de carboxilato utilizando yodo como oxidante.
Normalmente, el átomo de nitrógeno del grupo amino reacciona como un nucleófilo a través de su par solitario . Esta polaridad se puede invertir cuando una amina primaria o secundaria se sustituye por un buen grupo saliente (como un átomo de halógeno o un grupo alcoxi ). El compuesto N-sustituido resultante puede comportarse como un electrófilo en el átomo de nitrógeno y reaccionar con un nucleófilo como, por ejemplo, en la aminación electrófila de carbaniones . [11]
Recientemente, C.-J. Li y col. En presencia de un catalizador, similar a los reactivos organometálicos, las hidrazonas pueden sufrir adiciones nucleófilas, adiciones de conjugados y acoplamientos cruzados catalizados por metales de transición con varios electrófilos para formar nuevos enlaces CC. [12]
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )