La hemofilia B , también escrita como hemofilia B , es un trastorno de la coagulación sanguínea que provoca moretones y sangrado con facilidad debido a una mutación hereditaria del gen del factor IX , y que resulta en una deficiencia del factor IX. Es menos común que la deficiencia del factor VIII ( hemofilia A ). [3]
La hemofilia B fue reconocida por primera vez como una entidad patológica distinta en 1952. [4] También se la conoce con el epónimo enfermedad de Christmas , [1] que lleva el nombre de Stephen Christmas , el primer paciente descrito con hemofilia B. Además, el primer informe de su La identificación fue publicada en la edición navideña del British Medical Journal . [4] [5]
La mayoría de las personas que tienen hemofilia B y experimentan síntomas son hombres. [6] La prevalencia de la hemofilia B en la población es aproximadamente de uno entre 40.000; La hemofilia B representa aproximadamente el 15% de los pacientes con hemofilia. [6] Muchas mujeres portadoras de la enfermedad no presentan síntomas. [6] Sin embargo, se estima que entre el 10% y el 25% de las mujeres portadoras tienen síntomas leves; en casos raros, las mujeres pueden tener síntomas moderados o graves. [6]
Los síntomas incluyen aparición de hematomas con facilidad , hemorragias del tracto urinario ( hematuria ), hemorragias nasales ( epistaxis ) y hemorragias en las articulaciones ( hemartrosis ). [1]
Los pacientes con trastornos hemorrágicos presentan una mayor incidencia de enfermedad periodontal así como de caries dental, relacionado con el miedo al sangrado que conlleva a una falta de higiene y cuidado de la salud bucal. La manifestación bucal más destacada de una hemofilia B leve sería el sangrado gingival durante la exfoliación de la dentición primaria, o el sangrado prolongado después de un procedimiento invasivo/extracción de un diente; En la hemofilia grave, puede haber sangrado espontáneo de los tejidos bucales (p. ej., paladar blando, lengua, mucosa bucal), labios y encías, con equimosis. En casos raros, se puede observar hemartrosis (sangrado en el espacio articular) de la articulación temporomandibular (ATM). [7]
Los pacientes con hemofilia experimentarán muchos episodios de hemorragia bucal a lo largo de su vida. Un promedio de 29,1 eventos hemorrágicos por año son lo suficientemente graves como para requerir reemplazo de factor en pacientes con deficiencia de F VIII, de los cuales el 9% involucra estructuras orales. Los niños con hemofilia grave tienen una prevalencia significativamente menor de caries dental y puntuaciones de placa más bajas en comparación con controles sanos comparables. [8]
El gen del factor IX se encuentra en el cromosoma X (Xq27.1-q27.2). Es un rasgo recesivo ligado al cromosoma X , lo que explica por qué los hombres se ven afectados en mayor número. [9] [10]
En 1990, George Brownlee y Merlin Crossley demostraron que dos conjuntos de mutaciones genéticas impedían que dos proteínas clave se unieran al ADN de personas con una forma rara e inusual de hemofilia B ( la hemofilia B de Leyden ), en la que los pacientes experimentan episodios de sangrado excesivo en la infancia. pero tienen pocos problemas de sangrado después de la pubertad. [10]
Esta falta de unión de proteínas al ADN estaba desactivando el gen que produce el factor IX de coagulación , que previene el sangrado excesivo. [10]
La deficiencia de factor IX conduce a una mayor propensión a sufrir hemorragias , que pueden ocurrir de forma espontánea o en respuesta a un traumatismo leve. [11]
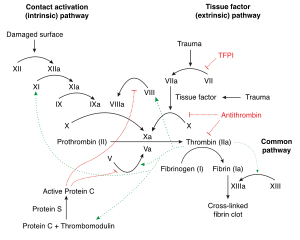
La deficiencia de factor IX puede causar interferencia en la cascada de coagulación, provocando así hemorragia espontánea cuando hay un traumatismo. El factor IX, cuando se activa, activa el factor X , que ayuda a la conversión del fibrinógeno en fibrina . [11]
El factor IX se vuelve activo eventualmente en la coagulación por el cofactor factor VIII (específicamente IXa). Las plaquetas proporcionan un sitio de unión para ambos cofactores. Este complejo (en la vía de la coagulación) eventualmente activará el factor X. [12]
El diagnóstico de hemofilia B se puede realizar mediante las siguientes pruebas/métodos: [2]
El diagnóstico diferencial de esta condición hereditaria es el siguiente: hemofilia A , deficiencia de factor XI , enfermedad de von Willebrand , trastornos del fibrinógeno y síndrome de Bernard-Soulier [10].
El tratamiento se administra de forma intermitente, cuando hay sangrado importante. Incluye infusión intravenosa de factor IX y/o transfusiones de sangre. Se deben evitar los AINE una vez realizado el diagnóstico, ya que pueden exacerbar un episodio hemorrágico. Cualquier procedimiento quirúrgico debe realizarse con ácido tranexámico concomitante . [4] [13]
El etranacogene dezaparvovec (Hemgenix) fue aprobado para uso médico en los Estados Unidos en noviembre de 2022. [6] Es la primera terapia génica aprobada por la Administración de Medicamentos y Alimentos de los EE. UU. (FDA) para tratar la hemofilia B. [6]
Se debe planificar el tratamiento quirúrgico, incluida una simple extracción dental, para minimizar el riesgo de sangrado, hematomas excesivos o formación de hematomas. Se pueden utilizar férulas blandas formadas al vacío para brindar protección local después de una extracción dental o de un sangrado prolongado posterior a la extracción. [14]
En julio de 2022 se anunciaron los resultados de una terapia génica candidata para la hemofilia B llamada FLT180, que funciona utilizando un virus adenoasociado (AAV) para restaurar la proteína del factor de coagulación IX (FIX), se observaron niveles normales de la proteína con dosis bajas de la terapia, pero se requirió inmunosupresión para disminuir el riesgo de respuestas inmunes relacionadas con vectores. [15] [16] [17]

Stephen Christmas (12 de febrero de 1947 - 20 de diciembre de 1993) fue el primer paciente que padecía la enfermedad de Christmas (o hemofilia B) en 1952 por un grupo de médicos británicos. La Navidad nació en una familia británica en Londres . Era hijo del actor de cine y televisión Eric Christmas . [18] Emigró a Toronto, Ontario , Canadá, con su familia, y fue allí a la edad de dos años cuando le diagnosticaron hemofilia en el Hospital para Niños Enfermos . La familia regresó a Londres en 1952 para visitar a sus familiares y durante el viaje Stephen fue ingresado en el hospital. Una muestra de su sangre fue enviada al Centro de Hemofilia de Oxford en Oxford , donde Rosemary Biggs y Robert Gwyn Macfarlane descubrieron que no tenía deficiencia del factor VIII , que normalmente está disminuido en la hemofilia clásica, sino de una proteína diferente, que recibió el nombre de Christmas. Factor en su honor (y posteriormente Factor IX ). [18] Stephen dependía de transfusiones de sangre y plasma , y se infectó con el VIH en el período durante el cual la sangre no se analizaba de forma rutinaria para detectar este virus. Se convirtió en un trabajador activo de la Sociedad Canadiense de Hemofilia e hizo campaña por la seguridad de las transfusiones desde que se infectó, pero desarrolló SIDA y murió a causa de ello en 1993. [18]
En las décadas de 1950 y 1960, con nuevas tecnologías y avances graduales en la medicina, los científicos farmacéuticos encontraron una manera de tomar el factor IX del plasma fresco congelado (PFC) y administrárselo a personas con hemofilia B. Aunque encontraron una manera de tratar la enfermedad. , el PFC contenía solo una pequeña cantidad de factor IX , lo que requería grandes cantidades de PFC para tratar un episodio hemorrágico real, lo que provocó que la persona requiriera hospitalización. A mediados de la década de 1960, los científicos encontraron una manera de obtener una mayor cantidad de factor IX del FFP. A finales de la década de 1960, los científicos farmacéuticos encontraron métodos para separar el factor IX del plasma , lo que permitió preparar botellas de concentrados de factor IX cuidadosamente empaquetadas. Con el aumento de los concentrados de factor IX, a las personas les resultó más fácil recibir tratamiento en casa. [19] Aunque estos avances en la medicina tuvieron un impacto positivo significativo en el tratamiento de la hemofilia, hubo muchas complicaciones que conllevaron. A principios de la década de 1980, los científicos descubrieron que los medicamentos que habían creado transferían virus transmitidos por la sangre , como la hepatitis , y el VIH , el virus que causa el SIDA. Con el aumento de estos virus mortales, los científicos tuvieron que encontrar métodos mejorados para examinar los productos sanguíneos que recibían de los donantes. En 1982, los científicos lograron un gran avance en la medicina y lograron clonar el gen del factor IX . Con este nuevo desarrollo disminuyó el riesgo de muchos virus. Aunque se creó el nuevo factor, no estuvo disponible para pacientes con hemofilia B hasta 1997. [ cita necesaria ]
En 2009, un análisis de marcadores genéticos reveló que la hemofilia B era la enfermedad de la sangre que afectaba a muchas familias reales europeas del Reino Unido, Alemania, Rusia y España: la llamada "enfermedad real". [20] [21]