
La celulasa ( EC 3.2.1.4; nombre sistemático 4-β- D -glucano 4-glucanohidrolasa ) es cualquiera de varias enzimas producidas principalmente por hongos , bacterias y protozoos que catalizan la celulolisis , la descomposición de la celulosa y de algunos polisacáridos relacionados :
El nombre también se usa para cualquier mezcla o complejo natural de varias de estas enzimas, que actúan en serie o sinérgicamente para descomponer el material celulósico.
Las celulasas descomponen la molécula de celulosa en monosacáridos ("azúcares simples") como β- glucosa , o polisacáridos y oligosacáridos más cortos . La descomposición de la celulosa tiene una importancia económica considerable, porque hace que un componente importante de las plantas esté disponible para el consumo y uso en reacciones químicas. La reacción específica involucrada es la hidrólisis de los enlaces 1,4-β- D - glucosídicos en celulosa, hemicelulosa , liquenina y β -D- glucanos de cereales . Debido a que las moléculas de celulosa se unen fuertemente entre sí, la celulolisis es relativamente difícil en comparación con la descomposición de otros polisacáridos como el almidón. [2]
La mayoría de los mamíferos tienen una capacidad muy limitada para digerir fibras dietéticas como la celulosa por sí mismos. En muchos animales herbívoros, como rumiantes como el ganado vacuno y ovino, y fermentadores del intestino posterior como los caballos, las celulasas son producidas por bacterias simbióticas . Las celulasas endógenas son producidas por algunos tipos de animales , como algunas termitas , caracoles, [3] [4] [5] y lombrices de tierra .
Recientemente, también se han encontrado celulasas en microalgas verdes ( Chlamydomonas reinhardtii , Gonium pectorale y Volvox carteri ) y sus dominios catalíticos (CD) pertenecientes a la familia GH9 muestran la mayor homología de secuencia con las celulasas endógenas de metazoos. Las celulasas de algas son modulares y consisten en supuestos nuevos módulos de unión a carbohidratos (CBM) ricos en cisteína, conectores ricos en prolina/serina (PS), además de supuestos dominios desconocidos y similares a Ig en algunos miembros. La celulasa de Gonium pectorale constaba de dos CD separadas por conectores y con un CBM C-terminal. [6]
Se conocen varios tipos diferentes de celulasas, que se diferencian estructural y mecánicamente. Los sinónimos, derivados y enzimas específicas asociados con el nombre "celulasa" incluyen endo-1,4-β- D- glucanasa (β-1,4-glucanasa, β-1,4-endoglucano hidrolasa, endoglucanasa D, 1,4 -(1,3;1,4)-β -D- glucano 4-glucanohidrolasa), carboximetilcelulasa (CMCase), avicelasa, celudextrinasa , celulasa A, celulosina AP , celulasa alcalina , celulasa A 3 , 9,5 celulasa , celoxilanasa y pancelasa SS . Las enzimas que escinden la lignina en ocasiones se han denominado celulasas, pero este antiguo uso está en desuso; son enzimas modificadoras de la lignina .
Cinco tipos generales de celulasas según el tipo de reacción catalizada:
La avicelasa tiene actividad casi exclusivamente exocelulasa, ya que el avicel es un sustrato altamente microcristalino.
Dentro de los tipos anteriores también existen tipos progresivos (también conocidos como procesivo) y no progresivos. La celulasa progresiva continuará interactuando con una única hebra de polisacárido, la celulasa no progresiva interactuará una vez y luego se desconectará y se enganchará con otra hebra de polisacárido.
La acción de la celulasa se considera sinérgica ya que las tres clases de celulasa pueden producir mucho más azúcar que la adición de las tres por separado. Aparte de los rumiantes, la mayoría de los animales (incluidos los humanos) no producen celulasa en sus cuerpos y sólo pueden descomponer parcialmente la celulosa mediante la fermentación, lo que limita su capacidad para utilizar la energía del material vegetal fibroso.
La mayoría de las celulasas fúngicas tienen una estructura de dos dominios, con un dominio catalítico y un dominio de unión a celulosa, que están conectados por un conector flexible. Esta estructura está adaptada para trabajar sobre un sustrato insoluble y permite que la enzima se difunda bidimensionalmente sobre una superficie en forma de oruga. Sin embargo, también existen celulasas (principalmente endoglucanasas) que carecen de dominios de unión a celulosa.
Tanto la unión de sustratos como la catálisis dependen de la estructura tridimensional de la enzima que surge como consecuencia del nivel de plegamiento de las proteínas . La secuencia de aminoácidos y la disposición de sus residuos que se producen dentro del sitio activo, la posición donde se une el sustrato, pueden influir en factores como la afinidad de unión de los ligandos, la estabilización de los sustratos dentro del sitio activo y la catálisis. La estructura del sustrato es complementaria a la estructura precisa del sitio activo de la enzima. Los cambios en la posición de los residuos pueden provocar la distorsión de una o más de estas interacciones. [8] Factores adicionales como la temperatura, el pH y los iones metálicos influyen en las interacciones no covalentes entre la estructura de la enzima. [9] La especie Thermotoga maritima produce celulasas que constan de 2 láminas β (estructuras proteicas) que rodean una región catalítica central que es el sitio activo. [10] La enzima se clasifica como una endoglucanasa, que escinde internamente los enlaces β-1,4-glucosídicos en las cadenas de celulosa, lo que facilita una mayor degradación del polímero. Diferentes especies de la misma familia que T. maritima producen celulasas con estructuras diferentes. [10] Las celulasas producidas por la especie Coprinopsis cinerea constan de siete cadenas de proteínas en forma de un túnel cerrado llamado barril β/α. [11] Estas enzimas hidrolizan el sustrato carboximetilcelulosa. La unión del sustrato en el sitio activo induce un cambio de conformación que permite la degradación de la molécula.
En muchas bacterias, las celulasas in vivo son estructuras enzimáticas complejas organizadas en complejos supramoleculares , los celulosomas . Pueden contener, entre otras, cinco subunidades enzimáticas diferentes que representan endocelulasas, exocelulasas, celobiasas, celulasas oxidativas y celulosas fosforilasas, en las que sólo las exocelulasas y las celobiasas participan en la hidrólisis real del enlace β(1→4). El número de subunidades que componen los celulosomas también puede determinar la tasa de actividad enzimática. [12]
Las celulasas multidominio están muy extendidas en muchos grupos taxonómicos; sin embargo, las celulasas de bacterias anaeróbicas, que se encuentran en los celulosomas, tienen la arquitectura más compleja que consta de diferentes tipos de módulos. Por ejemplo, Clostridium cellulolyticum produce 13 celulasas modulares GH9 que contienen un número y disposición diferentes de dominio catalítico (CD), módulo de unión a carbohidratos (CBM), dockerina, conector y dominio similar a Ig. [13]
El complejo de celulasa de Trichoderma reesei , por ejemplo, comprende un componente denominado C1 (57.000 daltons ) que separa las cadenas de celulosa cristalina, una endoglucanasa (alrededor de 52.000 daltons), una exoglucanasa (alrededor de 61.000 daltons) y una β-glucosidasa (76.000 daltons). daltons). [14]
Se han identificado numerosas secuencias "firmas" conocidas como dockerinas y cohesinas en los genomas de bacterias que producen celulosomas. Dependiendo de su secuencia de aminoácidos y estructuras terciarias , las celulasas se dividen en clanes y familias. [15]
Las celulasas multimodulares son más eficientes que las enzimas libres (solo con CD) debido al sinergismo debido a la estrecha proximidad entre la enzima y el sustrato celulósico. Los CBM participan en la unión de la celulosa, mientras que los conectores glicosilados proporcionan flexibilidad a la CD para una mayor actividad y protección de proteasa, así como una mayor unión a la superficie de la celulosa. [6]


La celulasa se utiliza para el procesamiento comercial de alimentos en el café . Realiza la hidrólisis de la celulosa durante el secado de los frijoles . Además, las celulasas se utilizan ampliamente en la industria textil y en detergentes para ropa. También se han utilizado en la industria de la pulpa y el papel para diversos fines, e incluso se utilizan para aplicaciones farmacéuticas. La celulasa se utiliza en la fermentación de biomasa para convertirla en biocombustibles , aunque este proceso es relativamente experimental en la actualidad. La celulasa se utiliza en medicina como tratamiento para los fitobezoares, una forma de bezoar de celulosa que se encuentra en el estómago humano , y ha demostrado eficacia en la degradación de biopelículas bacterianas polimicrobianas al hidrolizar los enlaces glicosídicos β(1-4) dentro de los exopolisacáridos estructurales de la matriz de la sustancia polimérica extracelular (EPS). [17] [18]
Como el sustrato nativo, la celulosa , es un polímero insoluble en agua, los ensayos tradicionales de azúcar reductor que utilizan este sustrato no se pueden emplear para medir la actividad celulasa. Los científicos analíticos han desarrollado una serie de métodos alternativos.
Se puede utilizar un viscosímetro para medir la disminución de la viscosidad de una solución que contiene un derivado de celulosa soluble en agua, como la carboximetilcelulosa, tras la incubación con una muestra de celulasa. [20] La disminución de la viscosidad es directamente proporcional a la actividad celulasa. Si bien estos ensayos son muy sensibles y específicos para la endocelulasa ( las enzimas celulasas de acción exo producen poco o ningún cambio en la viscosidad), están limitados por el hecho de que es difícil definir la actividad en unidades enzimáticas convencionales (micromoles de sustrato hidrolizado o producto producido por minuto).
Los celooligosacáridos de DP inferior (DP2-6) son suficientemente solubles en agua para actuar como sustratos viables para las enzimas celulasas. [21] Sin embargo, como estos sustratos son en sí mismos " azúcares reductores ", no son adecuados para su uso en ensayos tradicionales de azúcares reductores porque generan un alto valor "en blanco". Sin embargo, su hidrólisis mediada por celulasa se puede controlar mediante métodos HPLC o IC para obtener información valiosa sobre los requisitos de sustrato de una enzima celulasa particular.
Los celooligosacáridos se pueden reducir químicamente mediante la acción del borohidruro de sodio para producir sus correspondientes alcoholes de azúcar . Estos compuestos no reaccionan en los ensayos de azúcares reductores, pero sus productos de hidrólisis sí lo hacen. Esto hace que los celooligosacáridos reducidos con borohidruro sean sustratos valiosos para el ensayo de celulasa utilizando ensayos de azúcar reductor tradicionales como el método Nelson-Symogyi. [22] [23]
[24]
Estos sustratos se pueden subdividir en dos clases:
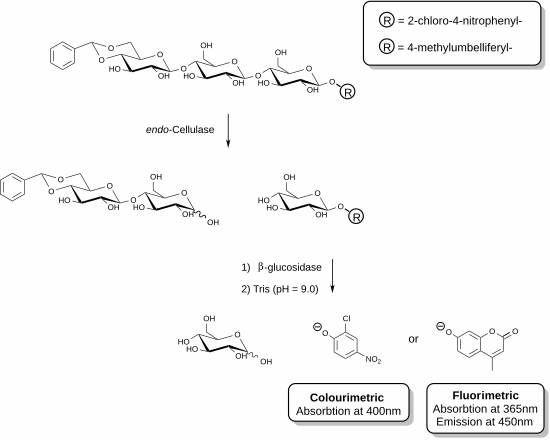
Recientemente, se han desarrollado nuevos reactivos que permiten la medición específica de endocelulasa . [25] [26] Estos métodos implican el uso de sustratos de oligosacáridos funcionalizados en presencia de una enzima auxiliar. En el ejemplo mostrado, una enzima celulasa es capaz de reconocer el fragmento de trisacárido de celulosa y escindir esta unidad. La enzima auxiliar presente en la mezcla de reactivos (β-glucosidasa) actúa entonces para hidrolizar el fragmento que contiene el cromóforo o fluoróforo. El ensayo finaliza mediante la adición de una solución básica que detiene la reacción enzimática y desprotona el compuesto fenólico liberado para producir la especie de fenolato. La actividad celulasa de una muestra determinada es directamente proporcional a la cantidad de fenolato liberado que puede medirse utilizando un espectrofotómetro. La funcionalización de acetal en el extremo no reductor del sustrato trisacárido previene la acción de la β-glucosidasa auxiliar sobre el sustrato original.