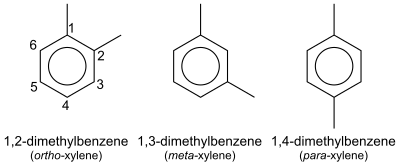
En química orgánica , el xileno o xilol (del griego ξύλον (xylon) 'madera'; [1] [2] nombre IUPAC : dimetilbenceno ) son cualquiera de los tres compuestos orgánicos con la fórmula (CH 3 ) 2 C 6 H 4 . Se derivan de la sustitución de dos átomos de hidrógeno con grupos metilo en un anillo de benceno ; qué hidrógenos se sustituyen determina cuál de los tres isómeros estructurales resulta. Es un líquido incoloro, inflamable, ligeramente grasiento de gran valor industrial. [3]
La mezcla se denomina tanto xileno como, más precisamente, xilenos. Los xilenos mixtos se refieren a una mezcla de xilenos más etilbenceno . Los cuatro compuestos tienen fórmulas moleculares idénticas C 8 H 10 . Por lo general, los cuatro compuestos se producen juntos mediante varios métodos de reformado catalítico y pirólisis . [4]
Los xilenos son un importante producto petroquímico producido por reformado catalítico y también por carbonización del carbón en la fabricación de combustible de coque . También se encuentran en el petróleo crudo en concentraciones de aproximadamente 0,5 a 1 %, según la fuente. Se encuentran en pequeñas cantidades en la gasolina y los combustibles para aviones .
Los xilenos se producen principalmente como parte de los aromáticos BTX ( benceno , tolueno y xilenos) extraídos del producto del reformado catalítico conocido como reformado .
Se producen varios millones de toneladas anualmente. [3] En 2011, un consorcio global comenzó la construcción de una de las plantas de xileno más grandes del mundo en Singapur . [5]
El xileno fue aislado y nombrado por primera vez en 1850 por el químico francés Auguste Cahours (1813-1891), habiendo sido descubierto como un componente del alquitrán de madera . [6]
Los xilenos se producen por la metilación de tolueno y benceno . [3] [7] El xileno comercial o de grado de laboratorio producido generalmente contiene alrededor de 40–65% de m -xileno y hasta 20% cada uno de o -xileno , p -xileno y etilbenceno . [8] [9] [10] La proporción de isómeros se puede cambiar para favorecer al altamente valorado p -xileno a través del proceso patentado UOP- Isomar [11] o por transalquilación de xileno consigo mismo o con trimetilbenceno. Estas conversiones son catalizadas por zeolitas . [3]
El ZSM-5 se utiliza para facilitar algunas reacciones de isomerización que conducen a la producción en masa de plásticos modernos.
Las propiedades físicas de los isómeros del xileno difieren ligeramente. El punto de fusión varía de −47,87 °C (−54,17 °F) ( m -xileno) a 13,26 °C (55,87 °F) ( p -xileno); como es habitual, el punto de fusión del isómero para es mucho más alto porque se compacta más fácilmente en la estructura cristalina. El punto de ebullición de cada isómero es de alrededor de 140 °C (284 °F). La densidad de cada isómero es de alrededor de 0,87 g/mL (7,3 lb/gal EE. UU.; 8,7 lb/gal imp) y, por lo tanto, es menos denso que el agua . El olor del xileno es detectable en concentraciones tan bajas como 0,08 a 3,7 ppm (partes de xileno por millón de partes de aire) y se puede percibir en agua a 0,53 a 1,8 ppm. [9]
Los xilenos forman azeótropos con agua y una variedad de alcoholes. El azeótropo con agua consta de un 60% de xilenos y hierve a 94,5 °C. [3] Al igual que con muchos compuestos de alquilbenceno , los xilenos forman complejos con varios halocarbonos . [12] Los complejos de diferentes isómeros a menudo tienen propiedades radicalmente diferentes entre sí. [13]
El p -xileno es el principal precursor del ácido tereftálico y del tereftalato de dimetilo , ambos monómeros utilizados en la producción de botellas de plástico de tereftalato de polietileno (PET) y ropa de poliéster . El 98% de la producción de p -xileno, y la mitad de todos los xilenos producidos se consumen de esta manera. [10] [14] El o -xileno es un precursor importante del anhídrido ftálico . La demanda de ácido isoftálico es relativamente modesta, por lo que rara vez se busca m -xileno (y de ahí la utilidad de su conversión a los isómeros o y p ).
Los xilenos se utilizan como disolventes en las industrias de impresión , caucho y cuero . Es un componente común de la tinta, el caucho y los adhesivos . [15] En la dilución de pinturas y barnices , se puede sustituir por tolueno cuando se desea un secado más lento, y por lo tanto lo utilizan los conservadores de objetos de arte en las pruebas de solubilidad. [16] De manera similar, es un agente de limpieza , por ejemplo, para acero , obleas de silicio y circuitos integrados . En odontología, el xileno se puede utilizar para disolver gutapercha , un material utilizado para endodoncia (tratamientos de conductos radiculares). En la industria del petróleo, el xileno también es un componente frecuente de los disolventes de parafina, que se utilizan cuando los tubos se obstruyen con cera de parafina.
El xileno se utiliza en el laboratorio para hacer baños con hielo seco para enfriar los recipientes de reacción, [17] y como disolvente para eliminar el aceite de inmersión sintético del objetivo del microscopio en la microscopía óptica . [18] En histología , el xileno es el agente de limpieza más utilizado. [19] El xileno se utiliza para eliminar la parafina de los portaobjetos de microscopio secos antes de la tinción. Después de la tinción, los portaobjetos de microscopio se colocan en xileno antes de montarlos con un cubreobjetos.
En una aplicación a gran escala, el para-xileno se convierte en ácido tereftálico . La principal aplicación del orto-xileno es como precursor de ésteres de ftalato , utilizados como plastificantes . El meta-xileno se convierte en derivados del ácido isoftálico , que son componentes de las resinas alquídicas . [3]
En general, con los xilenos se producen dos tipos de reacciones: las que involucran a los grupos metilo y las que involucran los enlaces C–H del anillo. Al ser bencílicos y, por lo tanto, debilitados, los enlaces C–H de los grupos metilo son susceptibles a reacciones de radicales libres, incluida la halogenación a los correspondientes dicloruros de xileno (bis(clorometil)bencenos), mientras que la monobromación produce bromuro de xililo , un agente gaseoso lacrimógeno . La oxidación y la amoxidación también tienen como objetivo los grupos metilo, lo que produce ácidos dicarboxílicos y dinitrilos. Los electrófilos atacan el anillo aromático, lo que da lugar a cloro- y nitroxilenos. [3]
El xileno es inflamable pero presenta una toxicidad aguda moderada, con una LD50 que oscila entre 200 y 5000 mg/kg para animales. La LD50 oral para ratas es de 4300 mg/kg. El principal mecanismo de desintoxicación es la oxidación a ácido metilbenzoico y la hidroxilación a hidroxileno. [3]
El principal efecto de la inhalación de vapor de xileno es la depresión del sistema nervioso central (SNC), con síntomas como dolor de cabeza, mareos, náuseas y vómitos. Con una exposición de 100 ppm, se pueden experimentar náuseas o dolor de cabeza. Con una exposición entre 200 y 500 ppm, los síntomas pueden incluir sensación de euforia, mareos, debilidad, irritabilidad, vómitos y tiempo de reacción más lento. [20] [21]
Los efectos secundarios de la exposición a bajas concentraciones de xileno ( < 200 ppm ) son reversibles y no causan daño permanente. La exposición a largo plazo puede provocar dolores de cabeza, irritabilidad, depresión, insomnio, agitación, cansancio extremo, temblores, pérdida de audición, problemas de concentración y pérdida de memoria a corto plazo. [22] [ Aclaración necesaria ] Una afección llamada encefalopatía crónica inducida por disolventes , comúnmente conocida como "síndrome de disolventes orgánicos", se ha asociado con la exposición al xileno. Hay muy poca información disponible que aísle el xileno de la exposición a otros disolventes en el examen de estos efectos. [20]
Los trastornos auditivos también se han relacionado con la exposición al xileno, tanto en estudios con animales de experimentación, [23] [24] como en estudios clínicos. [25] [26] [27]
El xileno también es un irritante cutáneo y elimina los aceites de la piel, lo que la hace más permeable a otras sustancias químicas. Se recomienda el uso de guantes y mascarillas impermeables, junto con respiradores cuando sea necesario, para evitar problemas de salud ocupacional derivados de la exposición al xileno. [20]
Los xilenos se metabolizan a ácidos metilhipúricos . [28] [29] La presencia de ácido metilhipúrico se puede utilizar como biomarcador para determinar la exposición al xileno. [29] [30]