Un ciclo biogeoquímico , o más generalmente un ciclo de la materia , [1] es el movimiento y transformación de elementos y compuestos químicos entre los organismos vivos, la atmósfera y la corteza terrestre. Los principales ciclos biogeoquímicos incluyen el ciclo del carbono , el ciclo del nitrógeno y el ciclo del agua . En cada ciclo, el elemento químico o molécula es transformado y ciclado por organismos vivos y a través de diversas formas y reservorios geológicos, incluida la atmósfera, el suelo y los océanos. Se puede considerar como la vía por la cual una sustancia química circula (cambia o se mueve a través de) el compartimento biótico y los compartimentos abióticos de la Tierra . El compartimento biótico es la biosfera y los compartimentos abióticos son la atmósfera , la litosfera y la hidrosfera .
Por ejemplo, en el ciclo del carbono, el dióxido de carbono atmosférico es absorbido por las plantas a través de la fotosíntesis , que lo convierte en compuestos orgánicos que los organismos utilizan para obtener energía y crecimiento. Luego, el carbono se libera nuevamente a la atmósfera a través de la respiración y la descomposición . Además, el carbono se almacena en combustibles fósiles y se libera a la atmósfera mediante actividades humanas como la quema de combustibles fósiles . En el ciclo del nitrógeno, las plantas convierten el gas nitrógeno atmosférico en formas utilizables como amoníaco y nitratos mediante el proceso de fijación de nitrógeno . Estos compuestos pueden ser utilizados por otros organismos y el nitrógeno regresa a la atmósfera mediante desnitrificación y otros procesos. En el ciclo del agua, el agua , solvente universal, se evapora de la tierra y los océanos para formar nubes en la atmósfera y luego vuelve a precipitarse en diferentes partes del planeta. La precipitación puede filtrarse en el suelo y convertirse en parte de los sistemas de agua subterránea utilizados por plantas y otros organismos, o puede escurrirse de la superficie para formar lagos y ríos. El agua subterránea puede entonces filtrarse al océano junto con las descargas de los ríos , ricas en materia orgánica disuelta y particulada y otros nutrientes.
Existen ciclos biogeoquímicos para muchos otros elementos, como el oxígeno , el hidrógeno , el fósforo , el calcio , el hierro , el azufre , el mercurio y el selenio . También existen ciclos para moléculas, como el agua y la sílice . Además, existen ciclos macroscópicos como el ciclo de las rocas y ciclos inducidos por el hombre para compuestos sintéticos como los bifenilos policlorados (PCB). En algunos ciclos existen reservorios geológicos donde las sustancias pueden permanecer o ser secuestradas por largos períodos de tiempo.
Los ciclos biogeoquímicos implican la interacción de procesos biológicos, geológicos y químicos. Los procesos biológicos incluyen la influencia de los microorganismos , que son impulsores críticos del ciclo biogeoquímico. Los microorganismos tienen la capacidad de llevar a cabo una amplia gama de procesos metabólicos esenciales para el ciclo de nutrientes y sustancias químicas en los ecosistemas globales. Sin microorganismos muchos de estos procesos no se producirían, con importantes repercusiones en el funcionamiento de los ecosistemas terrestres y oceánicos y en los ciclos biogeoquímicos del planeta en su conjunto. Los cambios en los ciclos pueden afectar la salud humana. Los ciclos están interconectados y desempeñan funciones importantes en la regulación del clima, apoyando el crecimiento de plantas , fitoplancton y otros organismos, y manteniendo la salud de los ecosistemas en general. Las actividades humanas, como la quema de combustibles fósiles y el uso de grandes cantidades de fertilizantes, pueden alterar los ciclos y contribuir al cambio climático, la contaminación y otros problemas ambientales.


La energía fluye direccionalmente a través de los ecosistemas, ingresando como luz solar (o moléculas inorgánicas para los quimioautótrofos ) y saliendo como calor durante las numerosas transferencias entre niveles tróficos . Sin embargo, la materia que forma los organismos vivos se conserva y se recicla. Los seis elementos más comunes asociados con las moléculas orgánicas (carbono, nitrógeno, hidrógeno, oxígeno, fósforo y azufre) toman una variedad de formas químicas y pueden existir durante largos períodos en la atmósfera, en la tierra, en el agua o debajo de la superficie de la Tierra. . Los procesos geológicos, como la meteorización , la erosión , el drenaje de agua y la subducción de las placas continentales , desempeñan un papel en este reciclaje de materiales. Debido a que la geología y la química desempeñan papeles importantes en el estudio de este proceso, el reciclaje de materia inorgánica entre los organismos vivos y su entorno se denomina ciclo biogeoquímico. [3]
Los organismos utilizan los seis elementos antes mencionados de diversas formas. El hidrógeno y el oxígeno se encuentran en el agua y en las moléculas orgánicas , los cuales son esenciales para la vida. El carbono se encuentra en todas las moléculas orgánicas, mientras que el nitrógeno es un componente importante de los ácidos nucleicos y las proteínas . El fósforo se utiliza para producir ácidos nucleicos y fosfolípidos que componen las membranas biológicas . El azufre es fundamental para la forma tridimensional de las proteínas. El ciclo de estos elementos está interconectado. Por ejemplo, el movimiento del agua es fundamental para la lixiviación de azufre y fósforo en los ríos, que luego pueden desembocar en los océanos. Los minerales circulan a través de la biosfera entre los componentes bióticos y abióticos y de un organismo a otro. [4]
Los sistemas ecológicos ( ecosistemas ) tienen muchos ciclos biogeoquímicos que operan como parte del sistema, por ejemplo, el ciclo del agua, el ciclo del carbono, el ciclo del nitrógeno, etc. Todos los elementos químicos que ocurren en los organismos son parte de ciclos biogeoquímicos. Además de ser parte de organismos vivos, estos elementos químicos también circulan a través de factores abióticos de ecosistemas como el agua ( hidrosfera ), la tierra ( litosfera ) y/o el aire ( atmósfera ). [5]
Los factores vivos del planeta pueden denominarse colectivamente biosfera . Todos los nutrientes (como el carbono , el nitrógeno , el oxígeno , el fósforo y el azufre ) utilizados en los ecosistemas por los organismos vivos son parte de un sistema cerrado ; por lo tanto, estos químicos se reciclan en lugar de perderse y reponerse constantemente, como en un sistema abierto. [5]
Las partes principales de la biosfera están conectadas por el flujo de elementos y compuestos químicos en ciclos biogeoquímicos. En muchos de estos ciclos, la biota juega un papel importante. La materia del interior de la Tierra es liberada por los volcanes. La atmósfera intercambia rápidamente algunos compuestos y elementos con la biota y los océanos. En comparación, los intercambios de materiales entre rocas, suelos y océanos son generalmente más lentos. [2]
El flujo de energía en un ecosistema es un sistema abierto ; El Sol constantemente le da al planeta energía en forma de luz, mientras que eventualmente se usa y se pierde en forma de calor a lo largo de los niveles tróficos de una red alimentaria. El carbono se utiliza para producir carbohidratos, grasas y proteínas, las principales fuentes de energía alimentaria . Estos compuestos se oxidan para liberar dióxido de carbono, que las plantas pueden capturar para producir compuestos orgánicos. La reacción química está impulsada por la energía luminosa del sol.
Se requiere la luz del sol para combinar el carbono con el hidrógeno y el oxígeno en una fuente de energía, pero los ecosistemas en las profundidades del mar , donde la luz del sol no puede penetrar, obtienen energía del azufre. El sulfuro de hidrógeno cerca de los respiraderos hidrotermales puede ser utilizado por organismos como el gusano tubular gigante . En el ciclo del azufre , el azufre puede reciclarse para siempre como fuente de energía. Se puede liberar energía mediante la oxidación y reducción de compuestos de azufre (por ejemplo, oxidando azufre elemental a sulfito y luego a sulfato ).
Aunque la Tierra recibe constantemente energía del Sol, su composición química es esencialmente fija, ya que los meteoritos añaden materia adicional sólo ocasionalmente. Debido a que esta composición química no se repone como la energía, todos los procesos que dependen de estos químicos deben reciclarse. Estos ciclos incluyen tanto la biosfera viva como la litosfera , la atmósfera y la hidrosfera no vivas .
Los ciclos biogeoquímicos se pueden contrastar con los ciclos geoquímicos . Este último se ocupa únicamente de los reservorios corticales y subcorticales, aunque algunos procesos de ambos se superponen.


El océano global cubre más del 70% de la superficie de la Tierra y es notablemente heterogéneo. Las áreas marinas productivas y los ecosistemas costeros comprenden una fracción menor del océano en términos de superficie, pero tienen un enorme impacto en los ciclos biogeoquímicos globales llevados a cabo por las comunidades microbianas , que representan el 90% de la biomasa del océano. [8] El trabajo de los últimos años se ha centrado en gran medida en el ciclo del carbono y los macronutrientes como el nitrógeno, el fósforo y el silicato: otros elementos importantes, como el azufre o los oligoelementos, han sido menos estudiados, lo que refleja cuestiones técnicas y logísticas asociadas. [9] Cada vez más, estas áreas marinas, y los taxones que forman sus ecosistemas, están sujetos a una importante presión antropogénica, lo que afecta la vida marina y el reciclaje de energía y nutrientes. [10] [11] [12] Un ejemplo clave es el de la eutrofización cultural , donde la escorrentía agrícola conduce al enriquecimiento de nitrógeno y fósforo de los ecosistemas costeros, lo que aumenta considerablemente la productividad, lo que resulta en floraciones de algas , desoxigenación de la columna de agua y el fondo marino, y un aumento del efecto invernadero. emisiones de gases, [13] con impactos directos locales y globales en los ciclos del nitrógeno y el carbono . Sin embargo, la escorrentía de materia orgánica desde el continente hacia los ecosistemas costeros es solo una de una serie de amenazas apremiantes que presionan a las comunidades microbianas debido al cambio global. El cambio climático también ha provocado cambios en la criosfera , a medida que los glaciares y el permafrost se derriten, lo que resulta en una estratificación marina intensificada , mientras que los cambios del estado redox en diferentes biomas están remodelando rápidamente los conjuntos microbianos a un ritmo sin precedentes. [14] [15] [16] [17] [9]
Por lo tanto, el cambio global está afectando procesos clave que incluyen la productividad primaria , la fijación de CO 2 y N 2 , la respiración/ remineralización de la materia orgánica y el hundimiento y enterramiento del CO 2 fijo . [17] Además de esto, los océanos están experimentando un proceso de acidificación , con un cambio de ~0,1 unidades de pH entre el período preindustrial y la actualidad, lo que afecta la química del amortiguador de carbonato / bicarbonato . A su vez, se ha informado que la acidificación afecta a las comunidades planctónicas , principalmente a través de efectos sobre los taxones calcificantes. [18] También hay evidencia de cambios en la producción de productos volátiles intermedios clave, algunos de los cuales tienen marcados efectos de invernadero (por ejemplo, N 2 O y CH 4 , revisado por Breitburg en 2018, [15] debido al aumento de la contaminación global). temperatura, estratificación del océano y desoxigenación, provocando entre un 25 y un 50% de la pérdida de nitrógeno del océano a la atmósfera en las llamadas zonas mínimas de oxígeno [19] o zonas marinas anóxicas , [20] impulsadas por procesos microbianos. , que suelen ser tóxicos para el necton marino , incluidas las especies con contenido reducido de azufre, como el H 2 S, tienen un impacto negativo para los recursos marinos como la pesca y la acuicultura costera. Si bien el cambio global se ha acelerado, ha habido un aumento paralelo de la conciencia sobre su complejidad. de los ecosistemas marinos, y especialmente el papel fundamental de los microbios como impulsores del funcionamiento de los ecosistemas [16] [9] .
Los microorganismos impulsan gran parte del ciclo biogeoquímico del sistema terrestre. [21] [22]
A veces, los productos químicos se mantienen durante largos períodos de tiempo en un solo lugar. Este lugar se llama depósito , que incluye, por ejemplo, depósitos de carbón que almacenan carbono durante un largo período de tiempo. [23] Cuando las sustancias químicas se retienen sólo por períodos cortos de tiempo, se retienen en fondos comunes de intercambio . Ejemplos de grupos de intercambio incluyen plantas y animales. [23]
Las plantas y los animales utilizan el carbono para producir carbohidratos, grasas y proteínas, que luego pueden usarse para construir sus estructuras internas o para obtener energía. Las plantas y los animales utilizan temporalmente carbono en sus sistemas y luego lo liberan nuevamente al aire o al medio circundante. Generalmente, los reservorios son factores abióticos, mientras que los depósitos de intercambio son factores bióticos. El carbono se retiene durante un tiempo relativamente corto en plantas y animales en comparación con los depósitos de carbón. La cantidad de tiempo que una sustancia química permanece en un lugar se llama tiempo de residencia o tiempo de renovación (también llamado tiempo de renovación o edad de salida). [23]
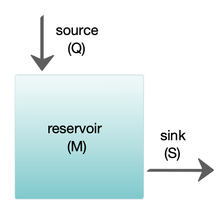
Los modelos de caja se utilizan ampliamente para modelar sistemas biogeoquímicos. [24] [25] Los modelos de caja son versiones simplificadas de sistemas complejos, reduciéndolos a cajas (o depósitos de almacenamiento ) para materiales químicos, unidos por flujos de materiales (flujos). Los modelos de cajas simples tienen una pequeña cantidad de cajas con propiedades, como el volumen, que no cambian con el tiempo. Se supone que las cajas se comportan como si estuvieran mezcladas de forma homogénea. [25] Estos modelos se utilizan a menudo para derivar fórmulas analíticas que describen la dinámica y la abundancia en estado estacionario de las especies químicas involucradas.
El diagrama de la derecha muestra un modelo básico de una sola caja. El depósito contiene la cantidad de material M considerado, según lo definido por sus propiedades químicas, físicas o biológicas. La fuente Q es el flujo de material hacia el depósito y el sumidero S es el flujo de material que sale del depósito. El presupuesto es el control y equilibrio de las fuentes y sumideros que afectan la rotación de material en un embalse. El embalse está en estado estacionario si Q = S , es decir, si las fuentes equilibran los sumideros y no hay cambios en el tiempo. [25]
El tiempo de residencia o rotación es el tiempo promedio que el material permanece residente en el yacimiento. Si el depósito está en estado estable, este es el mismo tiempo que lleva llenar o vaciar el depósito. Por lo tanto, si τ es el tiempo de rotación, entonces τ = M / S . [25] La ecuación que describe la tasa de cambio del contenido en un yacimiento es
Cuando dos o más depósitos están conectados, se puede considerar que el material circula entre los depósitos y puede haber patrones predecibles en el flujo cíclico. [25] Los modelos multibox más complejos generalmente se resuelven utilizando técnicas numéricas.

Los modelos de cajas biogeoquímicas globales suelen medir:
- masas de yacimientos en petagramos (Pg)
- flujos de flujo en petagramos por año (Pg yr −1 )
El diagrama de la izquierda muestra un presupuesto simplificado de los flujos de carbono oceánico. Se compone de tres modelos de cajas simples interconectados, uno para la zona eufótica , otro para el interior del océano u océano oscuro y otro para los sedimentos oceánicos . En la zona eufótica, la producción neta de fitoplancton es de aproximadamente 50 Pg C cada año. Alrededor de 10 Pg se exportan al interior del océano mientras que los otros 40 Pg se respiran. La degradación del carbono orgánico se produce cuando las partículas ( nieve marina ) se depositan en el interior del océano. Sólo 2 Pg finalmente llegan al fondo del mar, mientras que los otros 8 Pg son respirados en el océano oscuro. En los sedimentos, la escala de tiempo disponible para la degradación aumenta en órdenes de magnitud, con el resultado de que el 90% del carbono orgánico liberado se degrada y sólo 0,2 Pg C año −1 finalmente se entierra y se transfiere de la biosfera a la geosfera. [26]

El diagrama de la derecha muestra un modelo más complejo con muchos cuadros que interactúan. Las masas de los yacimientos aquí representan reservas de carbono , medidas en Pg C. Los flujos de intercambio de carbono, medidos en Pg C año −1 , ocurren entre la atmósfera y sus dos sumideros principales, la tierra y el océano. Los números negros y las flechas indican la masa del yacimiento y los flujos de intercambio estimados para el año 1750, justo antes de la Revolución Industrial . Las flechas rojas (y los números asociados) indican los cambios de flujo anual debidos a actividades antropogénicas, promediados durante el período 2000-2009. Representan cómo ha cambiado el ciclo del carbono desde 1750. Los números rojos en los embalses representan los cambios acumulativos en el carbono antropogénico desde el inicio del Período Industrial, 1750-2011. [28] [29] [27]

Hay ciclos biogeoquímicos rápidos y lentos. Los ciclos rápidos operan en la biosfera y los ciclos lentos operan en las rocas . Los ciclos rápidos o biológicos pueden completarse en años, trasladando sustancias de la atmósfera a la biosfera y luego de regreso a la atmósfera. Los ciclos lentos o geológicos pueden tardar millones de años en completarse, moviendo sustancias a través de la corteza terrestre entre las rocas, el suelo, el océano y la atmósfera. [31]
Como ejemplo, el ciclo rápido del carbono se ilustra en el diagrama siguiente a la izquierda. Este ciclo implica procesos biogeoquímicos de relativamente corto plazo entre el medio ambiente y los organismos vivos de la biosfera. Incluye movimientos de carbono entre la atmósfera y los ecosistemas terrestres y marinos, así como los suelos y los sedimentos del fondo marino . El ciclo rápido incluye ciclos anuales que implican la fotosíntesis y ciclos decenales que implican crecimiento vegetativo y descomposición. Las reacciones del rápido ciclo del carbono a las actividades humanas determinarán muchos de los impactos más inmediatos del cambio climático. [32] [33] [34] [35]
El ciclo lento se ilustra en el diagrama de arriba a la derecha. Implica procesos geoquímicos de mediano a largo plazo pertenecientes al ciclo de las rocas . El intercambio entre el océano y la atmósfera puede llevar siglos y la erosión de las rocas puede tardar millones de años. El carbono del océano se precipita al fondo del océano, donde puede formar rocas sedimentarias y ser subducido al manto de la Tierra . Los procesos de formación de montañas dan como resultado el retorno de este carbono geológico a la superficie de la Tierra. Allí las rocas se erosionan y el carbono regresa a la atmósfera mediante la desgasificación y al océano a través de los ríos. Otro carbono geológico regresa al océano a través de la emisión hidrotermal de iones de calcio. En un año determinado, entre 10 y 100 millones de toneladas de carbono se mueven en este ciclo lento. Esto incluye volcanes que devuelven carbono geológico directamente a la atmósfera en forma de dióxido de carbono. Sin embargo, esto es menos del uno por ciento del dióxido de carbono que se libera a la atmósfera al quemar combustibles fósiles. [31] [32]
El subsuelo terrestre es la mayor reserva de carbono de la Tierra y contiene entre 14 y 135 Pg de carbono [36] y entre el 2 y el 19% de toda la biomasa. [37] Los microorganismos impulsan transformaciones de compuestos orgánicos e inorgánicos en este entorno y, por lo tanto, controlan los ciclos biogeoquímicos. El conocimiento actual de la ecología microbiana del subsuelo se basa principalmente en las secuencias del gen del ARN ribosomal 16S (ARNr). Estimaciones recientes muestran que <8% de las secuencias de ARNr 16S en bases de datos públicas derivan de organismos del subsuelo [38] y solo una pequeña fracción de ellas está representada por genomas o aislados. Por lo tanto, hay muy poca información confiable sobre el metabolismo microbiano en el subsuelo. Además, se sabe poco sobre cómo los organismos de los ecosistemas subterráneos están interconectados metabólicamente. Algunos estudios basados en cultivos de consorcios sintróficos [39] [40] [41] y análisis metagenómicos a pequeña escala de comunidades naturales [42] [43] [44] sugieren que los organismos están vinculados a través de transferencias metabólicas: la transferencia de productos de reacción redox de un organismo a otro. Sin embargo, ningún entorno complejo ha sido diseccionado lo suficiente como para resolver las redes de interacción metabólica que los sustentan. Esto restringe la capacidad de los modelos biogeoquímicos para capturar aspectos clave del ciclo del carbono y de otros nutrientes. [45] Nuevos enfoques como la metagenómica resuelta por el genoma, un enfoque que puede producir un conjunto completo de borradores e incluso genomas completos para organismos sin el requisito de aislamiento en laboratorio [42] [46] [47] tienen el potencial de proporcionar este enfoque crítico. nivel de comprensión de los procesos biogeoquímicos. [48]
Algunos de los ciclos biogeoquímicos más conocidos se muestran a continuación:
Actualmente se están estudiando por primera vez muchos ciclos biogeoquímicos. El cambio climático y los impactos humanos están cambiando drásticamente la velocidad, la intensidad y el equilibrio de estos ciclos relativamente desconocidos, que incluyen:
Los ciclos biogeoquímicos siempre implican estados de equilibrio activo: un equilibrio en el ciclo del elemento entre compartimentos. Sin embargo, el equilibrio global puede implicar compartimentos distribuidos a escala global.
Como los ciclos biogeoquímicos describen los movimientos de sustancias en todo el mundo, su estudio es inherentemente multidisciplinario. El ciclo del carbono puede estar relacionado con la investigación en ecología y ciencias atmosféricas . [53] La dinámica bioquímica también estaría relacionada con los campos de la geología y la pedología . [54]
{{cite book}}: CS1 maint: numeric names: authors list (link)