Un acetato es una sal formada por la combinación de ácido acético con una base (por ejemplo , alcalina , terrosa , metálica , no metálica o radicalaria ). "Acetato" también describe la base o ion conjugado (específicamente, el ion con carga negativa llamado anión ) que se encuentra típicamente en solución acuosa y se escribe con la fórmula química C
2yo
3Oh−
2Las moléculas neutras formadas por la combinación del ion acetato y un ion positivo (llamado catión ) también se denominan comúnmente "acetatos" (de ahí, acetato de plomo , acetato de aluminio , etc.). El más simple de ellos es el acetato de hidrógeno (llamado ácido acético ) con sus sales correspondientes, ésteres y el anión poliatómico CH
3CO−
2, o CH
3ARRULLO−
.
La mayor parte de los aproximadamente 5 millones de toneladas de ácido acético que se producen anualmente en la industria se utilizan en la producción de acetatos, que suelen adoptar la forma de polímeros . En la naturaleza, el acetato es el componente básico más común para la biosíntesis .
Cuando forma parte de una sal , la fórmula del ion acetato se escribe como CH
3CO−
2, C
2yo
3Oh−
2, o CH
3ARRULLO−
Los químicos suelen representar el acetato como OAc − o, con menos frecuencia, AcO − . Por lo tanto, HOAc es el símbolo del ácido acético, NaOAc del acetato de sodio y EtOAc del acetato de etilo [1] (ya que Ac es el símbolo común del grupo acetilo CH 3 CO [2] [3] ). El símbolo del pseudoelemento "Ac" también se encuentra a veces en fórmulas químicas para indicar el ion acetato completo ( CH
3CO−
2). [ cita requerida ] No debe confundirse con el símbolo del actinio , el primer elemento de la serie de los actínidos ; el contexto guía la desambiguación. Por ejemplo, la fórmula del acetato de sodio podría abreviarse como "NaOAc", en lugar de "NaC 2 H 3 O 2 ". También se debe tener cuidado para evitar la confusión con el ácido peracético cuando se utiliza la abreviatura OAc; para mayor claridad y para evitar errores al traducir, se debe evitar HOAc en la literatura que menciona ambos compuestos.
Aunque su nombre sistemático es etanoato ( / ɪ ˈ θ æ n oʊ . eɪ t / ), el acetato común sigue siendo el nombre IUPAC preferido . [4]

El anión acetato , [CH 3 COO] − , (o [C 2 H 3 O 2 ] − ) pertenece a la familia de los carboxilato . Es la base conjugada del ácido acético . Por encima de un pH de 5,5, el ácido acético se convierte en acetato: [1]
Muchas sales de acetato son iónicas, lo que se indica por su tendencia a disolverse bien en agua. Un acetato que se encuentra comúnmente en el hogar es el acetato de sodio , un sólido blanco que se puede preparar combinando vinagre y bicarbonato de sodio ("bicarbonato de sodio"):
Los metales de transición pueden formarse complejos con acetato. Algunos ejemplos de complejos de acetato son el acetato de cromo (II) y el acetato de cinc básico.
Las sales de acetato de importancia comercial son el acetato de aluminio , utilizado en teñido , el acetato de amonio , un precursor de la acetamida , y el acetato de potasio , utilizado como diurético . Las tres sales son incoloras y muy solubles en agua. [5]
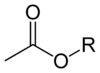
Los ésteres de acetato tienen la fórmula general CH3CO2R , donde R es un grupo organilo . Los ésteres son las formas dominantes de acetato en el mercado. A diferencia de las sales de acetato, los ésteres de acetato suelen ser líquidos, lipofílicos y, a veces, volátiles. Son populares porque tienen olores inofensivos, a menudo dulces, son económicos y, por lo general, tienen baja toxicidad.
Casi la mitad de la producción de ácido acético se consume en la producción de acetato de vinilo , precursor del alcohol polivinílico , que es un componente de muchas pinturas . El segundo uso más importante del ácido acético se consume en la producción de acetato de celulosa . De hecho, "acetato" es la jerga del acetato de celulosa, que se utiliza en la producción de fibras o productos diversos, por ejemplo, los discos de acetato utilizados en la producción de grabaciones de audio. El acetato de celulosa se puede encontrar en muchos productos domésticos. Muchos disolventes industriales son acetatos, incluidos el acetato de metilo , el acetato de etilo, el acetato de isopropilo y el acetato de etilhexilo. El acetato de butilo es una fragancia utilizada en productos alimenticios. [5]
El acetato es un anión común en biología. Los organismos lo utilizan principalmente en forma de acetil coenzima A. [ 6]
Se ha descubierto que la inyección intraperitoneal de acetato de sodio (20 o 60 mg por kg de masa corporal) induce dolor de cabeza en ratas sensibilizadas, y se ha propuesto que el acetato resultante de la oxidación del etanol es un factor importante en la aparición de resacas . El aumento de los niveles séricos de acetato conduce a la acumulación de adenosina en muchos tejidos, incluido el cerebro, y se ha descubierto que la administración del antagonista del receptor de adenosina, cafeína, a ratas después de la ingestión de etanol disminuye el comportamiento nociceptivo . [7] [8]
El acetato tiene propiedades inmunomoduladoras conocidas y puede afectar la respuesta inmune innata a bacterias patógenas como el patógeno respiratorio Haemophilus influenzae . [9]
El piruvato se convierte en acetil-coenzima A (acetil-CoA) por acción de la enzima piruvato deshidrogenasa . Esta acetil-CoA se convierte luego en acetato en E. coli , mientras se produce ATP por fosforilación a nivel de sustrato . La formación de acetato requiere dos enzimas: fosfato acetiltransferasa y acetato quinasa. [10]
.jpg/440px-E._coli_Bacteria_(7316101966).jpg)
acetil-CoA + fosfato → acetil-fosfato + CoA
acetilfosfato + ADP → acetato + ATP
El ácido acético también puede sufrir una reacción de dismutación para producir metano y dióxido de carbono : [11] [12]
Esta reacción de desproporción es catalizada por las arqueas metanógenas en su metabolismo fermentativo. Un electrón se transfiere desde la función carbonilo ( e− donante ) del grupo carboxílico al grupo metilo (e− aceptor ) del ácido acético para producir respectivamente CO2 y gas metano.