El 1,3,5,7-ciclooctatetraeno ( COT ) es un derivado insaturado del ciclooctano , de fórmula C 8 H 8 . También se le conoce como [8] anuleno . Este hidrocarburo poliinsaturado es un líquido inflamable de incoloro a amarillo claro a temperatura ambiente. Debido a su relación estequiométrica con el benceno , el COT ha sido objeto de mucha investigación y cierta controversia.
A diferencia del benceno, C 6 H 6 , el ciclooctatetraeno, C 8 H 8 , no es aromático , aunque su dianión , C
8h2-8
( ciclooctatetraenida ), es. Su reactividad es característica de un polieno ordinario , es decir, sufre reacciones de adición . El benceno, por el contrario, se caracteriza por sufrir reacciones de sustitución , no adiciones.
El 1,3,5,7-ciclooctatetraeno fue sintetizado inicialmente por Richard Willstätter en Munich en 1905 utilizando pseudopeletierina como material de partida y la eliminación de Hofmann como transformación clave: [2] [3]
Willstätter observó que el compuesto no presentaba la aromaticidad esperada. Entre 1939 y 1943, químicos de todo Estados Unidos intentaron sin éxito sintetizar COT. Racionalizaron su falta de éxito con la conclusión de que Willstätter en realidad no había sintetizado el compuesto sino su isómero, el estireno . Willstätter respondió a estas críticas en su autobiografía, donde señaló que los químicos estadounidenses "no se preocuparon" por la reducción de su ciclooctatetraeno a ciclooctano (una reacción imposible para el estireno). Durante la Segunda Guerra Mundial , Walter Reppe de BASF Ludwigshafen desarrolló una síntesis sencilla en un solo paso de ciclooctatetraeno a partir de acetileno, proporcionando un material idéntico al preparado por Willstätter. [4] Cualquier duda restante sobre la exactitud de la síntesis original de Willstätter se resolvió cuando Arthur C. Cope y sus compañeros de trabajo en el MIT informaron, en 1947, una repetición completa de la síntesis de Willstätter, paso a paso, utilizando las técnicas reportadas originalmente. Obtuvieron el mismo ciclooctatetraeno [5] y posteriormente informaron sobre la caracterización espectral moderna de muchos de los productos intermedios, confirmando nuevamente la precisión del trabajo original de Willstätter. [6] Sin embargo, la temperatura de congelación del producto era diferente a la del COT puro, y los autores lo interpretaron como una contaminación con aproximadamente un 30% de estireno.

Los primeros estudios demostraron que el COT no presentaba la química de un compuesto aromático. [7] Luego, los primeros experimentos de difracción de electrones concluyeron que las distancias de los enlaces CC eran idénticas. [8] Sin embargo, los datos de difracción de rayos X de HS Kaufman demostraron que el ciclooctatetraeno adopta varias conformaciones y contiene dos distancias de enlace C-C distintas. [9] Este resultado indicó que COT es un anuleno con enlaces CC simples y dobles alternos fijos.
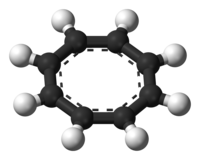
En su estado normal, el ciclooctatetraeno no es plano y adopta una conformación de tina con ángulos C = C − C = 126,1 ° y C = C − H = 117,6 °. [10] El grupo puntual del ciclooctatetraeno es D 2d . [11]
En su estado de transición planar, el estado de transición D 4h es más estable que el estado de transición D 8h debido al efecto Jahn-Teller . [12]
La síntesis original de Richard Willstätter (cuatro reacciones de eliminación consecutivas en una estructura de ciclooctano) arroja rendimientos relativamente bajos. La síntesis de ciclooctatetraeno de Reppe, que implica tratar acetileno a alta presión con una mezcla tibia de cianuro de níquel y carburo de calcio , fue mucho mejor, con rendimientos químicos cercanos al 90%: [4]
La COT también se puede preparar mediante fotólisis del barrileno , uno de sus isómeros estructurales , y la reacción se desarrolla a través de otro isómero aislable, el semibullvaleno . [13] Los derivados de COT también se pueden sintetizar mediante intermedios de semibullvaleno. En la secuencia ilustrada a continuación, el octaetilciclooctatetraeno (C 8 Et 8 ) se forma mediante isomerización térmica de octaetilsemibullvaleno, a su vez formado por ciclodimerización mediada por bromuro de cobre (I) de 1,2,3,4-tetraetil-1,4-dilitio-1, 3-butadieno. [14]
Debido a que el COT es inestable y forma fácilmente peróxidos orgánicos explosivos , generalmente se agrega una pequeña cantidad de hidroquinona al material disponible comercialmente. Se recomienda realizar pruebas de peróxidos cuando se utiliza una botella previamente abierta; Los cristales blancos alrededor del cuello de la botella pueden estar compuestos de peróxido, que puede explotar si se lo perturba mecánicamente.
El ciclooctatetraeno se ha aislado de ciertos hongos. [15]
Los enlaces π en COT reaccionan como es habitual en las olefinas, en lugar de como sistemas de anillos aromáticos. Los mono y poliepóxidos se pueden generar mediante la reacción de COT con peroxiácidos o con dimetildioxirano . También se conocen otras reacciones de adición. Además, el poliacetileno se puede sintetizar mediante la polimerización con apertura de anillo de ciclooctatetraeno. [16] El propio COT, y también sus análogos con cadenas laterales, se han utilizado como ligandos metálicos y en compuestos tipo sándwich .
El ciclooctatetraeno también sufre reacciones de reordenamiento para formar sistemas de anillos aromáticos . Por ejemplo, la oxidación con sulfato acuoso de mercurio (II) forma fenilacetaldehído [4] [17] y la transposición fotoquímica de su monoepóxido forma benzofurano . [18]
COT reacciona fácilmente con potasio metálico para formar la sal K 2 COT, que contiene el dianión C.
8h2-8
. [19] El dianión es plano, octogonal y aromático con un recuento de electrones de Hückel de 10.
El ciclooctatetraeno forma complejos organometálicos con algunos metales, incluidos el itrio , lantánidos y actínidos. [20] El compuesto sándwich uranoceno (U(COT) 2 ) presenta dos ligandos η 8 -COT. En bis(ciclooctatetraeno)hierro (Fe(COT) 2 ), un COT es η 6 y el otro es η 4 . (Ciclooctatetraeno)tricarbonilo de hierro características η 4 -COT. Los espectros de 1 H NMR a temperatura ambiente de estos complejos de hierro son singletes, indicativos de fluxionalidad . [21]

El ciclooctatetraeno se clora para dar un compuesto [4.2.0] -bicíclico , que reacciona aún más con acetilendicarboxilato de dimetilo en una reacción de Diels-Alder (DA). Retro-DA a 200 °C libera cis-diclorociclobuteno. Este compuesto reacciona con dihierro nonacarbonilo para dar ciclobutadieneiron tricarbonilo . [22] [23]
{{cite book}}: Mantenimiento CS1: DOI inactivo a partir de junio de 2024 ( enlace )