
En química , un complejo de pinza de metal de transición es un tipo de complejo de coordinación con un ligando de pinza. Los ligandos de pinza son agentes quelantes que se unen firmemente a tres sitios coplanares adyacentes en una configuración meridional. [1] [2] La inflexibilidad de la interacción pinza-metal confiere alta estabilidad térmica a los complejos resultantes. Esta estabilidad se atribuye en parte a la geometría restringida de la pinza, que inhibe la ciclometalación de los sustituyentes orgánicos en los sitios donantes en cada extremo. En ausencia de este efecto, la ciclometalación es a menudo un proceso de desactivación significativo para los complejos, en particular limitando su capacidad para efectuar la activación del enlace CH . Los sustituyentes orgánicos también definen un bolsillo hidrófobo alrededor del sitio de coordinación reactivo. Las aplicaciones estequiométricas y catalíticas de los complejos de pinza se han estudiado a un ritmo acelerado desde mediados de la década de 1970. La mayoría de los ligandos de pinza contienen fosfinas . [3] Las reacciones de los complejos de metal-pinza se localizan en tres sitios perpendiculares al plano del ligando de pinza, aunque en algunos casos un brazo es hemilábil y se genera un sitio de coordinación adicional de manera transitoria. Los primeros ejemplos de ligandos de pinza (originalmente no llamados así) eran aniónicos con un carbanión como sitio donante central y donantes de fosfina flanqueantes; estos compuestos se conocen como pinzas de PCP.
Aunque la clase más común de ligandos de pinza presenta conjuntos de donantes de PCP, se han desarrollado variaciones en las que las fosfinas se reemplazan por tioéteres y aminas terciarias. Muchos ligandos de pinza también presentan donantes nitrogenados en la posición central del grupo de coordinación (ver figura), como las piridinas . [4]

Un ligando de pinza que se prepara fácilmente es el POCOP . Muchos tipos de ligandos tridentados ocupan tres sitios de coordinación coplanares contiguos. El ligando más famoso de este tipo es la terpiridina (“terpy”). La terpy y sus parientes carecen del volumen estérico de los dos sitios donantes terminales que se encuentran en los ligandos de pinza tradicionales.
Los complejos de pinza metálica a menudo se preparan mediante la activación del enlace CH . [5] [6]
Los complejos de pinza Ni(II) N,N,N son activos en las reacciones de acoplamiento de Kumada , Sonogashira y Suzuki-Miyaura con haluros de alquilo no activados. [7] [8]

El ligando de pinza es, con mayor frecuencia, un donador aniónico de dos electrones al centro metálico. Consiste en una cadena principal rígida y plana que generalmente consta de estructuras arilo y tiene dos grupos donantes neutros de dos electrones en las posiciones meta. La fórmula general para los ligandos de pinza es 2,6-(ER 2 ) 2 C 6 H 3 – abreviado ECE – donde E es el donador de dos electrones y C es el ipsocarbono de la cadena principal aromática (por ejemplo, PCP – dos donantes de fosfina ). [9] Debido al modo de coordinación tridentado firme , permite que los complejos metálicos exhiban una alta estabilidad térmica, así como estabilidad al aire. [5] También implica que hay un número reducido de sitios de coordinación disponibles para la reactividad, lo que a menudo limita el número de productos indeseables formados en la reacción debido al intercambio de ligando, ya que este proceso se suprime.
Existen varios tipos de ligandos de pinza que se utilizan en la catálisis de metales de transición . A menudo, tienen el mismo donante de dos electrones flanqueando el centro metálico, pero esto no es un requisito.

Los diseños de ligando de pinza más comunes son PCP, NCN, PCN, SCS y PNO. Otros elementos que se han empleado en diferentes posiciones en el ligando son boro , arsénico , silicio e incluso selenio .
Al alterar las propiedades de los ligandos de pinza, es posible alterar significativamente la química en el centro metálico. El cambio de la dureza/suavidad del donante, el uso de grupos atractores de electrones (EWG) en la cadena principal y la alteración de las restricciones estéricas de los ligandos son métodos que se utilizan para ajustar la reactividad en el centro metálico.
La síntesis de los ligandos a menudo implica la reacción entre 1,3-dibromoetilbenceno con una fosfina secundaria seguida de la desprotonación de los intermediarios de fósforo cuaternario para generar el ligando. [10]
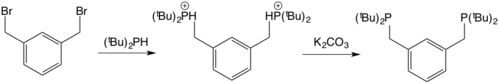
Para generar el complejo metálico se emplean dos rutas comunes. Una es una simple adición oxidativa del enlace ipso-CX donde X = Br, I a un centro metálico, a menudo un M(0) (M = Pd, Mo, Fe, Ru, Ni, Pt) aunque también se pueden utilizar otros complejos metálicos con estados de oxidación más altos (por ejemplo, Rh(COD)Cl 2 ). [11] [12]
El otro método significativo de introducción de metales es a través de la activación del enlace CH ., [5] La principal diferencia es que el metal utilizado en este método ya está en un estado de oxidación más alto (por ejemplo, especies PdCl 2 – Pd(II)). Sin embargo, se ha descubierto que estas reacciones proceden de manera mucho más eficiente al emplear complejos metálicos con ligandos débilmente unidos (por ejemplo, Pd(BF 4 ) 2 (CH 3 CN) 2 o Pd(OTf) 2 (CH 3 CN) 2 donde OTf = F 3 CO 2 SO − ). [6]
Se ha investigado el valor potencial de los ligandos de pinza en la catálisis, aunque no se ha comercializado ningún proceso. Las aplicaciones aspiracionales están motivadas por la alta estabilidad térmica y rigidez. Las desventajas incluyen el costo de los ligandos.

Se ha demostrado que los complejos de pinza catalizan las reacciones de acoplamiento de Suzuki-Miyaura , una reacción versátil de formación de enlaces carbono-carbono.
El acoplamiento Suzuki típico emplea catalizadores de Pd(0) con ligandos de fosfina terciaria monodentada (por ejemplo, Pd(PPh 3 ) 4 ). Es un método muy selectivo para acoplar sustituyentes arilo, pero requiere temperaturas elevadas. [13]
Utilizando catalizadores de pinza de paladio-PCP, se pueden lograr acoplamientos arilo-arilo con números de recambio (TON) superiores a 900.000 y altos rendimientos. [5] Además, otros grupos han descubierto que se pueden lograr cargas de catalizador muy bajas con complejos de pinza de paladio asimétricos. Se ha descubierto que cargas de catalizador de 0,0001 mol % tienen TON superiores a 190.000 y el límite superior de TON puede alcanzar 1.100.000.
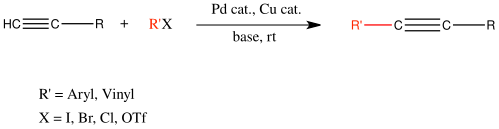
El acoplamiento Sonogashira se ha utilizado ampliamente para acoplar haluros de arilo con alquinos. Se pueden lograr TON superiores a 2.000.000 y cargas de catalizador bajas de 0,005 mol % con catalizadores basados en PNP. [14]
Los alcanos sufren deshidrogenación a altas temperaturas. Normalmente, esta conversión se promueve de forma heterogénea porque los catalizadores homogéneos no sobreviven a las temperaturas requeridas (~200 °C). La conversión correspondiente puede ser catalizada de forma homogénea por catalizadores de pinza, que son suficientemente resistentes térmicamente. La prueba de concepto fue establecida en 1996 por Jensen y colaboradores. Informaron que un complejo de pinza de iridio y rodio cataliza la deshidrogenación de ciclooctano con una frecuencia de recambio de 12 min −1 a 200 °C. Encontraron que la deshidrogenación se realizó a una velocidad dos órdenes de magnitud mayor que las informadas previamente. [15] También se encontró que el complejo de pinza de iridio exhibía una mayor actividad que el complejo de rodio. Esta diferencia de velocidad puede deberse a la disponibilidad del estado de oxidación Ir(V), que permite enlaces Ir-C e Ir-H más fuertes. [15]

El proceso catalizado homogéneamente se puede acoplar a otras reacciones como la metátesis de alquenos. Estas reacciones en tándem no se han demostrado con catalizadores heterogéneos. [16] [17]
El trabajo original sobre los ligandos de PCP surgió de estudios de los complejos de Pt(II) derivados de fosfinas diterciarias de cadena larga, especies del tipo R 2 P(CH 2 ) n PR 2 donde n >4 y R = terc-butilo . El platino metala un grupo metileno con liberación de HCl, dando especies como PtCl(R 2 P(CH 2 ) 2 CH(CH 2 ) 2 PR 2 ). [3]
Los complejos de pinza catalizan la deshidrogenación de alcanos. Los primeros informes describieron la deshidrogenación de ciclooctano mediante un complejo de pinza de Ir con una frecuencia de recambio de 12 min −1 a 200 °C. Los complejos son térmicamente estables a tales temperaturas durante días. [15]