Las células linfoides innatas ( ILC ) son la familia de células inmunes innatas descubierta más recientemente , derivadas de progenitores linfoides comunes (CLP). En respuesta al daño patógeno del tejido, las ILC contribuyen a la inmunidad mediante la secreción de moléculas de señalización y la regulación de las células inmunes tanto innatas como adaptativas. Las ILC son principalmente células residentes en los tejidos, que se encuentran tanto en tejidos linfoides (asociados inmunitariamente) como en tejidos no linfoides, y rara vez en la sangre. Son particularmente abundantes en las superficies mucosas y desempeñan un papel clave en la inmunidad y la homeostasis de las mucosas . Las características que permiten su diferenciación de otras células inmunes incluyen la morfología linfoide regular , la ausencia de receptores de antígenos reordenados que se encuentran en las células T y B (debido a la falta del gen RAG ) y marcadores fenotípicos generalmente presentes en las células mieloides o dendríticas . [1]
Con base en la diferencia en las vías de desarrollo, el fenotipo y las moléculas de señalización producidas, en 2013, las ILC se dividieron en tres grupos: 1, 2 y 3; sin embargo, después de una mayor investigación, ahora se dividen en cinco grupos: células NK , ILC1, ILC2 , ILC3 y células inductoras de tejido linfoide (LTi). [2] Las ILC están implicadas en múltiples funciones fisiológicas, incluida la homeostasis , morfogénesis , metabolismo , reparación y regeneración de los tejidos. Muchas de sus funciones son similares a las de las células T , por lo que se ha sugerido que son las contrapartes innatas de las células T. [3] La desregulación de las ILC puede provocar patologías inmunitarias como alergia , asma bronquial y enfermedades autoinmunes . [4]
El desarrollo de las ILC se inicia en respuesta a la presencia de factores de transcripción que se activan debido a la presencia de factores microambientales circundantes, como: citoquinas , ligandos de muesca y ritmo circadiano (cambios de comportamiento incorporados después de un ciclo diario). Una vez maduradas, las ILC liberan citoquinas. Por lo tanto, la clasificación de las ILC se basa en las diferencias en el factor de transcripción y los perfiles de citoquinas asociados con el desarrollo y la función de los diferentes subtipos de ILC. [5]
Los linajes de células ILC1 y NK divergen temprano en sus vías de desarrollo y pueden discriminarse por su diferencia en la dependencia de los factores de transcripción , su citotoxicidad y la expresión de sus marcadores residentes. Las células NK son células citotóxicas que circulan en el torrente sanguíneo y matan las células infectadas por virus y tumorales . Las ILC1 son células residentes en tejidos, no citotóxicas o débilmente citotóxicas, que funcionan en la defensa contra infecciones por virus y ciertas bacterias .
Debido a que las ILC1 y las células NK tienen características compartidas y no compartidas, la clasificación de las ILC1 humanas ha sido problemática. Ambos tipos de células producen IFN-γ como su citoquina principal y requieren el factor de transcripción T-bet para hacerlo. [6] Ambas células también pueden producir IFN-γ cuando las citoquinas IL-15 o IL-12 están reguladas positivamente en los tejidos después de una infección o lesión, y secretan TGFβ1 junto con IFN-γ cuando se estimulan. Esto impulsa la remodelación de la matriz extracelular y epitelial intestinal. [7] La coestimulación con IL-18 también aumenta significativamente los niveles de IFN-γ. [8] La liberación de IFN-γ estimula los macrófagos y otros fagocitos mononucleares , para inducir un efecto antimicrobiano para erradicar las infecciones intracelulares. Los radicales de oxígeno producidos por ambos tipos de células también ayudan a erradicar la infección. Las ILC1 y las células NK también pueden producir TNF-α , lo que contribuye aún más a la respuesta inflamatoria, dependiendo de la expresión de su molécula.
Existen diferencias en la dependencia de los factores de transcripción entre las células NK y las ILC1. Aunque ambos tipos de células utilizan T-bet para el desarrollo, se ha descubierto que las células NK están presentes en huéspedes deficientes en T-bet, pero las ILC1 dependen completamente de su presencia. [6] Sin embargo, el desarrollo de las células NK depende completamente de la presencia del factor de transcripción Eomes, mientras que las ILC1 pueden desarrollarse independientemente de su presencia. [6] Esto significa que los Eomes generalmente se pueden utilizar como marcador de células NK, lo que sugiere que las células NK maduras son Tbet + Eomes + y las ILC1 son Tbet + Eomes -. [9]
Las ILC1 y las células NK tienen algunos marcadores fenotípicos en común, que incluyen: NK1.1 en ratones y receptores de células NK (NCR) como NKp44 y NKp46 tanto en humanos como en ratones. [10] [6] También tienen diferencias en los marcadores fenotípicos, incluida la expresión de CD127 en ILC1 humanas, que no está presente en todas las células NK. Además, NKp80, un marcador de células NK humanas, no se expresa en ILC1. En ratones, se ha demostrado que CD200R distingue las células NK de las ILC1. [11] La relación entre los linajes de células ILC1 y NK aún sigue siendo confusa debido a la falta de estos marcadores característicos presentes en algunas células NK/ILC1 en ciertos tejidos, o después de ciertos eventos de infección/inflamación. Esto apoya la teoría de la función específica del tejido. [10] Por ejemplo, CD127 , aunque expresado por la mayoría de las ILC1, está ausente en las ILC1 residentes en las glándulas salivales, que también tienen la capacidad de expresar Eomes , una característica fundamental de las células NK. [12]
Debido a la producción de granzimas y perforina , las células NK se consideran las contrapartes innatas de las células T CD8+ citotóxicas , mientras que las ILC1 se consideran la contraparte innata de las células T colaboradoras , debido a la producción exclusiva de IFN-γ sin actividad citotóxica. [13]
Las ILC2 residen en los tejidos y participan en la respuesta innata a los parásitos, como la infección por helmintos, al ayudar a reparar el daño tisular. Son abundantes en los tejidos de la piel, [14] [15] pulmón, hígado e intestino. [6] [16] Se caracterizan por la producción de anfirregulina y citocinas tipo 2, incluidas IL-4 , IL-5 e IL-13 , en respuesta a IL-25 , TSLP e IL-33 . [6] Debido a su firma de citoquinas, se consideran las contrapartes innatas de las células Th2 .
Expresan marcadores de superficie característicos y receptores para quimiocinas , que participan en la distribución de células linfoides a sitios de órganos específicos. En humanos, las ILC2 expresan CRTH2 , KLRG1 , SST2 , CD161 y CD25 . [3] En ratones, las ILC2 expresan CD44 , pero no CD161 . [3]
Las ILC2 requieren IL-7 para su desarrollo, activando los factores de transcripción fundamentales RORα y GATA3 . GATA3 también es necesario para el mantenimiento de la función ILC2, y la privación de GATA3 inhibe el desarrollo y la función de las células.
Aunque se consideran homogéneas, las ILC2 se pueden clasificar en subpoblaciones de ILC2 naturales (nILC2) e ILC2 inflamatorias (iILC2), dependiendo de su capacidad de respuesta a IL-33 e IL-25. [3] Los nILC2 son aquellos que responden a la IL-33 en tejidos en un estado inmunológico natural, mientras que los iILC2 responden a la IL-25 o al parásito helminto. [3] Los nILC2 expresan más Thy1 y ST2 , y reducen KLRG1 . [3] iILC2, expresan más KLRG1 y reducen Thy1 y ST2. [3] Además de estas subpoblaciones, otra población, denominada célula ILC210, se caracteriza por su capacidad para producir IL-10 . [3]
Las ILC3 participan en la respuesta inmune innata a bacterias y hongos extracelulares. Desempeñan un papel clave en la homeostasis de las bacterias intestinales y en la regulación de las respuestas de las células Th17 . [17] Las ILC3 de adultos humanos se encuentran principalmente en la lámina propia del intestino y las amígdalas; sin embargo, también se encuentran en el bazo , el endometrio , la decidua y la piel. [18]
Las ILC3 dependen del factor de transcripción RORγt para su desarrollo y función. [19] Expresan RORγt en respuesta a IL-1β e IL-23, o señales patógenas. [20] La IL-22 es la principal citocina producida por las ILC3 y desempeña un papel fundamental en el mantenimiento de la homeostasis intestinal. Sin embargo, las ILC3 producen una variedad de otras citoquinas, incluidas IL-17, IL-22, IFN-γ y GM-CSF , dependiendo de los estímulos ambientales. [21]
Hay dos subconjuntos de ILC3, NCR- y NCR+ ILC3, siendo la NCR mostrada en las ILC3 de ratones NKp46, en comparación con la NKp44 mostrada en las ILC3 humanas. [21] Las ILC3 NKp44+ están altamente enriquecidas en las amígdalas y los intestinos, como fuente exclusiva de IL-22. [21] Algunas ILC3 también pueden expresar otros marcadores de células NK, incluidos NKp30 y CD56 . [22] Las NCR-ILC3 producen principalmente IL-17A e IL-17F y, en determinadas circunstancias, IL-22. [23] Las NCR-ILC3 pueden diferenciarse en NCR+ al aumentar los niveles de expresión de T-bet. [5] A pesar de expresar marcadores de células NK, las ILC3 difieren mucho de las células NK, con diferentes vías de desarrollo y funciones efectoras.

Las células LTi se consideran un linaje separado debido a su vía de desarrollo única; sin embargo, a menudo se las considera parte del grupo ILC3 debido a sus muchas características similares. Al igual que las ILC3, las células LTi dependen de RORγt. Intervienen en la formación de ganglios linfáticos secundarios y placas de Peyer promoviendo el desarrollo del tejido linfoide, lo que hacen mediante la acción de la linfotoxina , un miembro de la superfamilia del TNF . [6] Son fundamentales durante las etapas de desarrollo embrionario y adulto del sistema inmunológico y, por lo tanto, las células LTi están presentes en órganos y tejidos en las primeras etapas del desarrollo embrionario. [6] Tienen un papel fundamental en la organización del tejido linfoide primario y secundario y en el tejido linfoide adulto, regulando la respuesta inmune adaptativa y manteniendo las estructuras del tejido linfoide secundario. [25]
Su producción es estimulada por el ácido retinoico , CXCL13, RANK-L y las citoquinas IL-1B, IL-23 e IL-6. [26] Expresan c-Kit , CCR6 , CD25 , CD127 y CD90 , sin embargo, no NCR. [6] La expresión de OX40L es otro buen marcador de células LTi en ratones adultos y humanos. [24] Pueden ser CD4+/-. Al igual que las ILC3, tras la activación, las células LTi producen principalmente IL-17A , IL-17F e IL-22. [23] Están mediados por RANK, TNF , IL-17 e IL-22.
Las células LTi inducen la expresión de AIRE , el gen regulador autoinmune, al permitir el desarrollo de células epiteliales del timo embrionario. [24] Lo hacen a través de la señalización de linfotoxina α4β7 y RANK-L. [24] Las células LTi también permiten la supervivencia de las células T CD4+ de memoria y, por lo tanto, de las respuestas inmunitarias de memoria, dentro de los ganglios linfáticos recién formados. [24] Lo hacen a través de los miembros de la superfamilia TNF OX40L y CD30L , que envían señales a las células T CD4+. [24] Esta función podría utilizarse para prevenir la autoinmunidad y mejorar las respuestas de memoria después de la vacunación. [24]
Nuestra comprensión de las vías involucradas en el desarrollo de las ILC solo se ha aclarado en los últimos años, y nuestro conocimiento se basa principalmente en las vías del ratón. [6] Las CLP tienen la capacidad de diferenciarse en varios tipos de células diferentes, incluidas células T, células B e ILC, según las señales celulares presentes. Con la excepción de las células NK, todas las ILC requieren señalización de IL-7 para sobrevivir. El represor transcripcional ID2 parece antagonizar la diferenciación de las células B y T , produciendo un precursor dependiente de ID2 que puede diferenciarse aún más con factores de transcripción específicos del linaje. [4]
Las ILC son independientes del gen activador de recombinación (RAG); en cambio, dependen de la señalización de citocinas a través de la cadena gamma del receptor de citocina común y de la vía de la quinasa JAK3 para su desarrollo. [27]
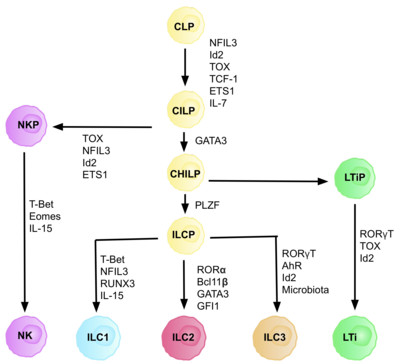
Las ILC se derivan de progenitores linfoides innatos comunes (CILP), que se derivan de CLP, que tienen la capacidad de diferenciarse en varios tipos diferentes de células linfoides, incluidas las células T y B. [6] Los CILP luego pueden diferenciarse en precursores de células NK (NKP) o en los progenitores linfoides innatos auxiliares comunes (CHILP) descritos más recientemente. [6] Los CHILP luego pueden diferenciarse en progenitores inductores de tejido linfoide (LTiP) y precursores de células linfoides innatas (ILCP). Los factores presentes en el microambiente determinan la progresión de los CLP hacia subtipos de ILC específicos, incluidos los ligandos de muesca, las citoquinas, el ritmo circadiano y la expresión de factores de transcripción. [ cita necesaria ]
El desarrollo de CLP a CILP y luego a ILC requiere el factor de transcripción ID2 , para mediar en la supresión de los destinos de las células linfoides que generan células T y B. [27] Lo hace reduciendo la actividad de los factores de transcripción de la caja E ( E2A , E2-2 y HEB ), fundamentales en el desarrollo de las células B y T. [27] Inicialmente se asumió que se requería ID2 para que las CLP se diferenciaran en todos los subconjuntos de ILC; sin embargo, la investigación demostró que la eliminación de ID2 durante el desarrollo de CLP paraliza el desarrollo de todos los subconjuntos de ILC distintos de los progenitores de células NK, que son no depende de la presencia de Id2. [28] Debido a esta comprensión, se identificó un grupo de células de linaje negativo (requisito de cualquier célula precursora verdadera), que dependían completamente de la presencia de ID2 y expresaban otros marcadores ILC clave, con el fenotipo: Lin-ID2. +IL7Ra+CD25-α4β7+, que ahora se conocen como el ayudante común como los progenitores linfoides innatos CHILP. [28] Se denominan "tipo auxiliar común" debido a su similitud con los destinos de las células efectoras T auxiliares.
Cada etapa de diferenciación depende de la expresión de diferentes factores de transcripción, incluidos: NFIL3 , TCF-1 , ETS1 , GATA3, PLZF, T-bet, Eomes, RUNX3 , RORα, Bcl11b , Gfi1, RORγt y AhR . [6] La expresión coordinada de estos factores de transcripción específicos activa o reprime genes diana críticos en la diferenciación de los subconjuntos de linfocitos. [27] En particular, Nfil3, cuya expresión está regulada por citoquinas, controla la diferenciación de ILC a través de los factores de transcripción Id2, RORγt, Eomes y Tox . [29] Esto proporciona evidencia de que las señales tisulares desempeñan un papel clave en las decisiones sobre el destino de los linajes ILC.
Los estudios sugieren que el sitio principal de desarrollo de ILC es el hígado del feto y la médula ósea de los adultos, ya que es aquí donde se han encontrado CLP, NKP y CHILP. [27] Luego, las células salen y circulan en la sangre hasta llegar a los tejidos designados, codificados por moléculas de adhesión y quimiocinas . [27] Sin embargo, también se ha demostrado que la maduración de las ILC puede tener lugar fuera de los tejidos linfoides primarios, similar a la maduración de las células T auxiliares vírgenes.
Se han encontrado precursores de células NK y precursores de ILC3 en la amígdala humana, y ILCP fetales presentes en el intestino del ratón, acumulándose en las placas de Peyer. [30] [31] El ácido retinoico, producido por muchos tipos de células, como las células nerviosas, las células dendríticas y las células estromales , favorece la diferenciación de las ILC3, en lugar de las ILC2, y es necesario para su maduración completa. [27] Además, AhR, que puede activarse a través de ligandos producidos después del catabolismo alimentario, es necesario para el mantenimiento de la función y la expresión de las ILC3 intestinales. [30]
Las ILC participan en nuestra respuesta inmune a patógenos en todos los órganos, en particular en las superficies mucosas. [13] Son clave en la respuesta inmune innata debido a su capacidad para secretar rápidamente citocinas inmunorreguladoras; sin embargo, también desempeñan un papel en la configuración de la respuesta adaptativa al interactuar con otras células inmunes. El microambiente del tejido en el que residen determina y afina la expresión de los diversos perfiles de ILC, facilitando su interacción en múltiples funciones efectoras.
El posicionamiento estratégico y el enraizamiento profundo de las ILC dentro de los tejidos les permiten mantener la homeostasis y, por lo tanto, el funcionamiento saludable de los tejidos. Sin embargo, las ILC también tienen funciones perjudiciales en diferentes sitios de la mucosa. [32]
Dado que la función de las ILC está vinculada a su localización tisular específica, la determinación de las señales involucradas en su localización y patrones de migración será importante en la identificación de nuevas vías para el tratamiento de enfermedades. [21]
Una propiedad fundamental de la inmunidad tipo 2, y por tanto de las células ILC2, es hacer frente a organismos de gran tamaño, que no pueden ser digeridos, como los helmintos . [33] En el intestino, en respuesta a una infección por helmintos, las células epiteliales secretan altos niveles de IL-25, lo que activa las células ILC2. Las ILC2 producen IL-13, que impulsa la diferenciación de células epiteliales adicionales, a través de las vías de señalización de Notch. Esta instrucción permite remodelar el tejido para permitir la expulsión del parásito helminto y otros patógenos grandes.
La IL-13 también activa las células T, induciendo más respuestas fisiológicas para expulsar el parásito. [34] Las células T estimulan la secreción de moco de las células caliciformes, la contracción del músculo liso y secretan señales que reclutan mastocitos y eosinófilos en el sitio, estimulando la proliferación de células B. [34]
La infección puede provocar daños en los tejidos debido a la migración de los helmintos. Las ILC2 tienen un papel clave en la reparación del daño tisular después de la infección, al producir ligandos como AREG , para los receptores del factor de crecimiento epitelial, lo que facilita la diferenciación de las células epiteliales para la reparación del tejido. [6] Esto puede funcionar para mejorar la función de barrera del epitelio y retardar la entrada de patógenos. [34]

En múltiples nichos tisulares, las ILC tienen una relación con células no hematopoyéticas, como las células estromales. En el pulmón, las ILC2 tienen una localización distinta en las células estromales, que liberan IL-33 y TSLP, lo que promueve la homeostasis de ILC2, tanto en el estado estacionario como en respuesta a la infección por helmintos, después de que el helminto se ha desarrollado en el intestino y ha migrado. al pulmón a través de la sangre. [35]
Las ILC2 pulmonares se colocan cerca de los vasos sanguíneos para permitir el reclutamiento de eosinófilos de la sangre. También están ubicados dentro de las vías respiratorias, donde pueden acumularse patógenos potenciales. Esto significa que están en estrecho contacto con las células neuroendocrinas , que activan las ILC2 mediante la liberación del péptido relacionado con el gen de la calcitonina . [36] Otros estudios también confirman la regulación de la función de las ILC a través de circuitos neuronales .
Además, las ILC1 y las ILC3 liberan radicales de oxígeno y enzimas letalmente dañinas en respuesta a una infección patógena, lo que daña el tejido del huésped. Las respuestas de reparación del tejido están coordinadas por la respuesta inmune tipo 2, después de que las ILC3 y las ILC1 hayan limpiado el tejido de microbios y desechos.
Las CLI intestinales están expuestas a metabolitos dietéticos, microbianos y endógenos. La localización de ILC en el intestino delgado está mediada por la integrina α4β7 y el receptor CCR9. Las ILC2 expresan CCR9 en la médula ósea, por lo que pueden llegar directamente al intestino; sin embargo, se requiere ácido retinoico para permitir la expresión de CCR9 en las ILC1 y las ILC3.
Las ILC facilitan el mantenimiento de la integridad de la barrera en el intestino, protegiendo de diversas bacterias e infecciones virales. Las ILC3 son el subconjunto más abundante presente tanto en el intestino adulto como en el fetal. [37] La distribución de las ILC en el intestino cambia durante el desarrollo y se distribuyen de manera desigual en todos los segmentos del tracto gastrointestinal. Esta distribución a diferentes nichos dentro del intestino está mediada por distintas cascadas de señalización. [38] En los seres humanos, aproximadamente el 70% de las ILC intestinales son NCR+ y el 15% son NCR-. [39]

Las ILC3 interactúan directamente con la flora bacteriana , creando una red entre la microbiota y el huésped, favoreciendo la homeostasis. Las ILC3 restringen la colonización de múltiples bacterias no beneficiosas en el intestino, mediante la secreción de IL-22, estimulando las células epiteliales para que produzcan péptidos antimicrobianos. [40] La producción de IL-22 se induce debido a la producción de IL-23 e IL-1β por macrófagos y CD, y promueve la curación de la capa mucosa. [3] Por ejemplo, la IL-22 puede promover la reparación del daño intestinal después de la quimioterapia o la radioterapia . Las ILC3 regulan la contención de bacterias comensales en la luz, lo que permite que quede expuesta a los fagocitos de la lámina propia, lo que lleva al cebado de las células T. Aunque pueden presentar antígenos a través de los receptores MHC de clase II , las ILC carecen de moléculas coestimuladoras y, por lo tanto, desempeñan un papel en la anergia de las células T , promoviendo la tolerancia a los comensales beneficiosos. [39] La relación entre las ILC3 y las células T en el intestino es, por lo tanto, crucial para mantener la homeostasis, ya que en ausencia de ILC3, podría haber una activación incontrolada de las células T. Además, la microbiota desempeña un papel en el ajuste de la producción de IL-22 por parte de las ILC3; por ejemplo, las bacterias filamentosas segmentadas en el íleon regulan la producción de IL-22 y permiten la diferenciación de las células Th17. [41] [42]
Las ILC3 interactúan con el sistema nervioso entérico para mantener la homeostasis intestinal, ya que en respuesta a las bacterias, las células gliales de la lámina propia secretan factores neurotróficos que, a través del receptor neurorregulador RET , inducen la producción de IL-22 por las ILC3. [43] Las células dendríticas también pueden producir IL-23 durante el estrés inducido por patógenos, activando también las ILC3, lo que permite la producción de IL-22. Uno de los mecanismos por los cuales la IL-22 regula la microbiota presente en el intestino es a través de los patrones de glicosilación de las células epiteliales. [44] La expresión de IL-22 y linfotoxina por parte de ILC3 controla la expresión de fucosiltransferasa 2, que permite la fucosilación de las células epiteliales, proporcionando una fuente de nutrientes para las bacterias luminales. [44]
Los ligandos AHR de la dieta o la microbiota son reconocidos por las células inmunitarias y regulan el desarrollo de ILC y las funciones de las células NK en el intestino. En respuesta a los metabolitos del triptófano, la señalización del AhR mantiene la expresión de IL-22 y la homeostasis intestinal. [6] El ácido retinoico, producido por células dendríticas, promueve la expresión de receptores intestinales en ILC1 e ILC3, y mejora la función de ILC3 mediante la regulación positiva de RORγt e IL-22. [6] También existe una interferencia entre los macrófagos y las ILC3, a través de la producción de GM-CSF impulsada por RORγt, que depende de la señalización microbiana, y la producción de IL-1β por los macrófagos. [39] Una deficiencia de vitamina A en la dieta da como resultado un número anormalmente pequeño de ILC3 y, por lo tanto, una reducción de la producción de IL-22 y una mayor susceptibilidad a las infecciones. Por el contrario, el ácido retinoico suprime la proliferación de ILC2 al regular negativamente el IL-7Ra , y se ha demostrado que la privación de vitamina A mejora la resistencia mediada por ILC2 a la infección por helmintos en ratones. [39] Por lo tanto, las ILC3 forman una red de interacciones para mantener la homeostasis intestinal, entre el microbioma , el epitelio intestinal, las células neurogliales y otras células inmunitarias.
Las células LTi están presentes en las placas de Peyer y en los folículos linfoides , interactuando con las células B facilitando la producción de IgA , lo que promueve el comensalismo del huésped con la microbiota local. [45] Las ILC1 y las células NK producen IFN-γ para combatir los patógenos intracelulares. Tras la infección por C. difficile , las ILC1 y las ILC3 cooperan para combatir la infección. [46] Las ILC2 inducen la diferenciación de las células caliciformes y la producción de moco en el intestino para proteger del daño tisular tras una infección parasitaria.
Diferentes grupos de células linfoides innatas tienen la capacidad de influir en la tumorigénesis de varias maneras. [47] [48]
Las ILC del grupo 1 son la población de ILC con el potencial antitumoral más significativo, y las células NK poseen la capacidad de reconocer el MHC Clase I faltante en la superficie de las células tumorales. [49] De esta manera, actúan de manera complementaria con las células T citotóxicas que reconocen y matan las células tumorales que presentan un antígeno extraño en el MHC de clase I. [50] [51] Las células NK expresan una serie de células NK que activan la superficie celular. receptores celulares con especificidad por ligandos inducidos por estrés sobreexpresados en células tumorales. Consulte la página de células asesinas naturales para obtener más información sobre las células NK en la vigilancia de tumores.
Las ILC1 influyen en el microambiente tumoral mediante la producción de las citoquinas IFN-γ y TNF-α, que al comienzo de la respuesta inmune polarizan otras células inmunes, como los macrófagos M1 , las células dendríticas y las células T citotóxicas hacia el sitio, creando una inflamación. ambiente. [52] Si tiene éxito, el reclutamiento de estas células matará las células tumorigénicas; sin embargo, en algunos casos, el IFN-γ y el TNF-α pueden desempeñar un papel en la inducción de células inmunes inmunosupresoras, como las MDSC , y por lo tanto antiinflamatorias. citocinas, lo que permite un entorno inmunológico del que las células tumorales pueden escapar . [53] [54] [48]
El papel de las ILC2 y las ILC3 en la vigilancia de tumores depende del microambiente encontrado en sus tejidos residentes.
Las ILC2 producen citoquinas que promueven una respuesta inmune antiinflamatoria, por ejemplo, IL-13, IL-4, anfirregulina, favoreciendo el crecimiento tumoral. [55] Sin embargo, en algunos entornos, las ILC2 pueden producir IL-5 que promueve una respuesta citotóxica de los eosinófilos y, por lo tanto, una respuesta antitumoral. [56] [57]
Las ILC3 también pueden participar en entornos pro o antitumorales. La producción de IL-17 puede favorecer el crecimiento de tumores y metástasis, ya que induce la permeabilidad de los vasos sanguíneos; sin embargo, la regulación positiva del MHC Clase II en su superficie puede estimular las células T CD4+, teniendo un efecto antitumoral. [58] Además, se ha informado que las ILC3 promueven la formación de estructuras linfoides terciarias en el cáncer de pulmón, desempeñando un papel protector. [59]

Todos los subconjuntos de ILC están presentes en el hígado y regulan la respuesta inmune para proteger el tejido de infecciones virales y bacterianas. [60] Las ILC1 son el subconjunto de ILC dominante presente en el hígado. Su producción de IFN-γ promueve la supervivencia de los hepatocitos . [61] La producción de IFN-γ por las ILC1 depende de la expresión del receptor de células NK CD226 . [61] La producción de IFN-γ impulsada por IL-12 por parte de ILC1 se acelera mediante ATP extracelular , y el IFN-γ regula positivamente las moléculas de supervivencia Bcl-2 y Bcl-xL en los hepatocitos. [61]
Las células NK desempeñan un papel en la respuesta inmune contra la hepatitis viral B y C , limitando la fibrosis hepática y el cáncer de hígado . Eliminan las células hepáticas en el hígado fibrótico mediante TRAIL y/o NKG2D .
Las ILC desempeñan un papel importante en el mantenimiento del estrés dietético y la homeostasis metabólica. La producción de metabolitos de triptófano hace que el factor de transcripción AhR induzca la expresión de IL-22, manteniendo el número de ILC3 presentes y, por tanto, la homeostasis intestinal. [6] El metabolito de la vitamina A, el ácido retinoico, también regula positivamente la expresión de IL-22 y, por lo tanto, la ausencia de la vía de señalización AhR y del ácido retinoico da como resultado una inmunidad reducida a las infecciones bacterianas, como la infección gastrointestinal por Citrobacter rodentium. . [6] El ácido retinoico también mejora la expresión de marcadores de localización intestinal en ILC1 e ILC3. Por lo tanto, la disponibilidad de nutrientes en la dieta modifica la respuesta inmune de la ILC a la infección y la inflamación, destacando la importancia de una dieta equilibrada y saludable.
Las ILC2 apoyan un entorno inmunológico tipo 2 en el tejido adiposo , mediante la producción de IL-5, IL-4 e IL-13. Esto regula la adiposidad, la resistencia a la insulina y el gasto calórico. [6] La desregulación de esto causa inflamación persistente tipo 1, lo que lleva a la obesidad . Las ILC2 promueven el color beige de los adipocitos y, por tanto, aumentan el gasto energético. Por lo tanto, la disminución de las respuestas de las ILC2 en el tejido es una característica de la obesidad, ya que esto interrumpe su papel crucial en la homeostasis energética, lo que resulta en una reducción del gasto energético y un aumento de la adiposidad. [62] Además de las ILC2, las ILC1 contribuyen a la homeostasis de los macrófagos del tejido adiposo en condiciones tanto magras como obesas, y constituyen entre el 5 y el 10 % de la población de linfocitos residentes en los depósitos adiposos magros humanos. [10] Una dieta rica en grasas aumenta el número de ILC1 y la activación del tejido adiposo, aumentando los niveles de IFN-γ y TNF-α. Las ILC1 producen el quimioatrayente de macrófagos CCL2 y, por lo tanto, la señalización de macrófagos ILC1 es un regulador clave del tejido adiposo. [63] Esta vía podría ser un objetivo potencial para el tratamiento de pacientes con enfermedad hepática .
Las ILC2 promueven la proliferación de células epiteliales y caliciformes y, por lo tanto, la producción de moco en el tracto respiratorio. Estas funciones contribuyen a la restauración y mantenimiento de la integridad epitelial. Las ILC2 proporcionan una defensa contra las infecciones por helmintos en los pulmones mediante la producción de AhR, IL-9 e IL-13. [64] Se cree que estas ILC2 se originan en el intestino y migran al pulmón para combatir la infección por helmintos. [sesenta y cinco]
Las ILC1 y las células NK secretan IFN-γ en respuesta a una infección viral en los pulmones, incluido el rinovirus y el virus respiratorio sincitial (VRS). [3]
Las ILC3 también están implicadas en infecciones pulmonares, a través de la secreción de IL-17 e IL-22, por ejemplo en la infección por S. pneumoniae . Se requieren más estudios para descifrar el papel de las ILC en las infecciones respiratorias humanas. [66]

La evidencia muestra que las ILC3 y las ILC2 se reclutan en la dermis herida tanto en ratones como en humanos, a través de la señalización epidérmica Notch1. [39] Las ILC3 secretan IL-17F, que desempeña un papel en las respuestas celulares inmunes y epiteliales durante la cicatrización de heridas, al reclutar macrófagos en el sitio. La expresión de TNF también desempeña un papel en la cicatrización de heridas, ya que dirige la localización de ILC3 en la epidermis de la piel dañada. [39] En respuesta a la liberación de IL-33 por la epidermis, las ILC2 secretan altos niveles de anfirregulina, un factor de crecimiento epidérmico crítico, que por lo tanto contribuye a la cicatrización de heridas cutáneas . [39]
La mucosa oral está colonizada por comensales y expuesta a antígenos y patógenos de la dieta. Las ILC de la mucosa oral ayudan a mantener la barrera y protegen contra las infecciones. Las ILC3 y las ILC1 intraepiteliales se identificaron inicialmente en las amígdalas y se encontraron en las encías humanas. Aproximadamente entre el 10 y el 15% de los linfocitos se identificaron como ILC y la mayoría de ellos producían ILC1 de IFN-γ. Las ILC3 en la orofaringe protegen contra la infección de Candida albicans que produce IL-17A e IL-17F inducida por IL-23. Los ratones que carecían de ILC3 debido a la eliminación o el agotamiento de RORγt sufrieron infecciones graves por Candida albicans. [67]
Se ha demostrado que las ILC pueden secretar neurotransmisores y neuropéptidos en los pulmones. Las ILC2 interactúan con las neuronas del tracto respiratorio por la proximidad a las fibras nerviosas, y las ILC2 residentes en los pulmones productoras de IL-5 se encuentran en regiones ricas en colágeno cercanas a la confluencia de vasos sanguíneos y vías respiratorias de tamaño mediano. Además, las ILC2 productoras de IL-5 se encuentran en las células neuroendocrinas pulmonares en las uniones de las ramas de las vías respiratorias en las que se concentran las partículas que ingresan a las vías respiratorias. La localización de ILC2 en las vías respiratorias sugiere que la residencia de ILC2 está definida por microambientes en diferentes zonas del tejido. [68]
El reloj circadiano y las interacciones ILC se han demostrado mediante el estudio de la regulación del reloj del gen maestro Arntl. Su eliminación resultó en la desregulación de ILC3 causada por cambios epigenéticos, impulsando la expresión de IL-22 y contribuyendo a la alteración del microbioma, las células epiteliales y una absorción alterada de lípidos en el intestino. Por otro lado, la eliminación de Nr1d1, una proteína implicada en la regulación de las respuestas metabólicas circadianas, resultó en la reducción de NCR+ ILC3 y el aumento de la producción de IL-17, mientras que no afectó a la ILC3 similar a LTi. [69]

Se ha confirmado que las ILC2 desempeñan un papel patogénico durante la inflamación pulmonar. Las células epiteliales del pulmón expresan las citocinas IL-33 e IL-25, o TSLP, en respuesta a diversos alérgenos , hongos y virus. Estas citoquinas activan las ILC2 y, por lo tanto, hay un mayor número de ILC2 y citocinas tipo 2 (IL-4/5/13) en pacientes con asma alérgica. [3] Secretan IL-13, lo que inicia la inflamación pulmonar alérgica y, además, promueven la diferenciación Th2, lo que aumenta la producción de IL-13 y, por lo tanto, amplifica la respuesta alérgica. [70]
La producción de IL-5 por las ILC2 en el pulmón conduce al reclutamiento de eosinófilos, y se sabe que otras poblaciones de células interactúan y dan forma a la presencia de ILC2 pulmonares en la inflamación de las vías respiratorias en pacientes asmáticos. Además, también promueven la proliferación de células B. Se cree que el aumento de las ILC2 presentes se correlaciona con la gravedad de la enfermedad, y la evidencia confirma que algunas ILC2 "experimentadas con alérgenos" persisten después de la resolución de la inflamación inicial, lo que presenta similitudes con las células T de memoria. La presencia de ILC2 "experimentadas con alérgenos" puede ser la razón por la que los pacientes asmáticos suelen estar sensibilizados a diversos alérgenos. [39]
Esta respuesta inmune alérgica parece ser independiente de las células T y B, y la evidencia confirma que se pueden inducir respuestas alérgicas que se asemejan a síntomas similares al asma en ratones que carecen de células T y B, utilizando IL-33. [71] [72]
No está tan claro cómo otras ILC afectan el asma; sin embargo, los estudios muestran una correlación entre la cantidad de ILC3 que producen IL-17 y la gravedad de la enfermedad. Se ha demostrado en ratones que las células NK y las ILC1 inhiben la expansión de ILC2 debido a la producción de IFN-γ y, por tanto, pueden ayudar a controlar la enfermedad. Se requiere más investigación en pacientes humanos para determinar cómo el equilibrio entre los diferentes subconjuntos afecta el asma. [73]
Las células NK expresan muchos receptores de la superficie celular que pueden ser activadores, inhibidores, de adhesión, de citoquinas o quimiotácticos. La integración de la información recopilada a través de estas numerosas entradas permite a las células NK mantener la autotolerancia y reconocer las señales de estrés de las propias células. [74] Si la regulación dinámica y matizada de la activación de las células NK se desequilibra a favor del ataque de las células propias, se produce una patología de la enfermedad autoinmune. La desregulación de las células NK se ha implicado en una serie de trastornos autoinmunes que incluyen la esclerosis múltiple , el lupus eritematoso sistémico y la diabetes mellitus tipo I. [75]
La evidencia sugiere que apuntar a las ILC puede ser beneficioso en el diseño de terapias para trastornos autoinmunes. Como las ILC y las células T tienen muchas funciones redundantes, apuntar y neutralizar sus citocinas efectoras podría ser una mejor opción. Alternativamente, apuntar a sus mediadores activadores aguas arriba (IL-23, IL-1B o IL-6) o a sus factores de supervivencia (IL-7) podría usarse como un enfoque para tratar enfermedades inflamatorias. [21]

También se ha descubierto que la frecuencia de ILC2 está elevada en otros tejidos con síntomas alérgicos, como los pólipos nasales de pacientes con rinosinusitis crónica y en pacientes con enfermedad respiratoria exacerbada por aspirina . [3] La concentración de ILC2 se correlaciona positivamente con la gravedad de las enfermedades.
Las ILC2 se activan debido a la presencia de TSLP e IL-4, producidas por células epiteliales y eosinófilos respectivamente. Luego producen IL-4, IL-5 e IL-13, activando aún más los eosinófilos, en un circuito de retroalimentación positiva , promoviendo la inflamación. Interrumpir este circuito podría ser una terapia potencial para la rinitis. Las células NK parecen desempeñar un papel beneficioso, y hay menos presencia en personas con rinitis alérgica. [76]
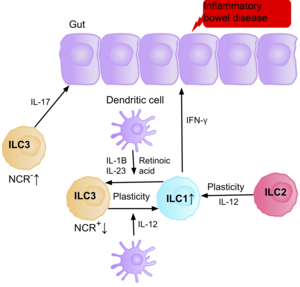
Las investigaciones sugieren que las NCR-ILC3 productoras de IL-17 contribuyen a la fisiopatología de la EII debido a su mayor abundancia en el intestino de los pacientes con enfermedad de Crohn . [39] Además, el número de ILC1 en la mucosa intestinal de pacientes con enfermedad de Crohn aumenta de aproximadamente el 10 % al 40 % del total de ILC presentes. [39] El aumento de las CLI presentes se correlaciona con la gravedad de la enfermedad. La evidencia sugiere que la plasticidad entre las ILC3 y las ILC1 en el intestino es un factor importante de la enfermedad de Crohn, y las ILC3 se diferencian en ILC1 cuando se exponen a la IL-12 producida por las células dendríticas. [39] Sin embargo, la IL-23, la IL-1B y el ácido retinoico presentes en el intestino pueden impulsar la diferenciación de las ILC1 de nuevo a las ILC3. [39] La evidencia también sugiere la capacidad de las ILC2 para adquirir el fenotipo proinflamatorio, con ILC2 produciendo IFN-γ presente en el intestino de pacientes con enfermedad de Crohn, en respuesta a ciertos factores ambientales como las citocinas. [39]
Los pacientes con EII tienen un mayor riesgo de padecer cáncer intestinal debido a la inflamación crónica, cuando las ILC3 adquieren el fenotipo proinflamatorio ILC1 durante la inflamación crónica. Dado que las ILC se acumulan en el intestino de los pacientes con EII, se cree que pueden tener un papel protumoral. En apoyo de esto, los estudios muestran un aumento en la cantidad de citoquinas efectoras IL-23, IL-17 e IL-22, en el microambiente tumoral del cáncer intestinal. [77] [78] [79]
Las células NK secretan IFN-γ, que tiene efectos antitumorales. Múltiples estudios muestran una disminución de la frecuencia de células NK e IFN-γ presentes en el intestino o la sangre periférica de pacientes con cáncer intestinal. [80] [81] Se requieren más estudios para abordar su papel exacto en el entorno del cáncer intestinal.
Las ILC1 hepáticas contribuyen a la patogénesis de la hepatitis B crónica debido a la producción de IFN-γ y TNF-α. La alteración del epitelio que recubre los conductos biliares hepáticos se observa con frecuencia en respuesta a la inflamación crónica del hígado, y el aumento de la proliferación de estos conductos se asocia con el cáncer de hígado. [60] La evidencia sugiere que la proliferación mejorada es desencadenada por IL-13, que se produce mediante la producción de células ILC2 inducida por IL-33. También se ha demostrado que las ILC2 mejoran la progresión de la fibrosis hepática, lo que a su vez promueve el desarrollo de cáncer de hígado. [60]
La disponibilidad de nutrientes dietéticos específicos puede afectar la homeostasis inmune de las ILC al alterar la energía almacenada en el tejido adiposo. El tejido adiposo mantiene la homeostasis del metabolismo y ahora se considera un órgano totalmente inmunocompetente. La desnutrición y la glotonería pueden desregular las respuestas de las ILC mediante cambios en los nutrientes de la dieta, lo que tiene efectos directos sobre la energía almacenada en el tejido adiposo. [10] La obesidad se asocia con cambios en la flora gastrointestinal, aumento de la afluencia de ácidos grasos libres desde el tejido adiposo al hígado y aumento de la permeabilidad intestinal. [10] La estrecha proximidad anatómica del tracto gastrointestinal y el hígado significa que el transporte de metabolitos bacterianos a través de la vena porta desencadena la inflamación, actuando sobre las células inmunes innatas, incluidas las ILC1, por lo que desempeña un papel importante en la activación de un estado inflamatorio en el hígado. . Por tanto, la inflamación asociada a la obesidad puede influir en la progresión de la enfermedad hepática, debido al desarrollo de resistencia a la insulina y desregulación metabólica. [10] Las ILC1, como regulador clave de la inflamación del tejido adiposo, son, por lo tanto, un objetivo terapéutico potencial para el tratamiento de personas con enfermedad hepática o síndrome metabólico .
También se han identificado ILC2 en tejido adiposo blanco humano y de ratón , lo que contribuye al desarrollo de la obesidad. Tras la desregulación de la homeostasis en el tejido adiposo, la disminución de las respuestas de las ILC2 es una característica de la obesidad, ya que esto interrumpe su papel crucial en la homeostasis energética, lo que resulta en una reducción del gasto energético y un aumento de la adiposidad. [62]
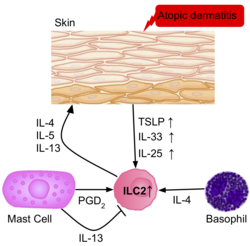
La frecuencia de ILC2 es mayor en la piel inflamada de pacientes con dermatitis atópica que en pacientes sanos. [39] Las ILC2 de la piel de los pacientes tenían una regulación positiva de los receptores IL-25, IL-33, TSLP y PGD2, lo que sugiere su papel en la activación de las ILC2. Los basófilos y los mastocitos también están presentes en estas lesiones cutáneas, lo que produce IL-4 y PGD2 , lo que activa aún más las ILC2.

La psoriasis , otra enfermedad inflamatoria de la piel, provoca un engrosamiento epidérmico, formando placas pobladas principalmente de células T y células dendríticas. Las células T representan una respuesta inmune tipo 1; sin embargo, se cree que el engrosamiento y la inflamación de la epidermis son causados por la producción de IL-22, IL-17A e IL-17F por otras células T como las células T Th17 o γδ . [39] Sin embargo, datos más recientes sugieren que las ILC3 de hecho producen una gran cantidad de estas citoquinas, con un aumento en la cantidad de ILC3 en la sangre periférica de pacientes con psoriasis. [39]
Las ILC se han estudiado en las barreras mucosas y su interacción con la inmunidad adaptativa, implicándolas así con enfermedades autoinmunes. En la artritis caracterizada por la presencia de autoanticuerpos, la comunicación cruzada desregulada entre Tfh y las células B se ha implicado en la generación de esos anticuerpos. Curiosamente, se ha sugerido que las respuestas inflamatorias Th17 y Tfh se generan en el tracto gastrointestinal y que la microbiota puede aumentar esta respuesta. Así, el desarrollo de ILC implicadas en la regulación de la respuesta inmune contra la microbiota en el intestino se ha asociado con la artritis. En el caso de ILC2, tiene un papel importante en la regulación de las respuestas inflamatorias mediante la producción de IL-4, IL-9 e IL-13. [82]
En el caso de ILC3 en la esclerosis múltiple, estas células han sido implicadas con agregados linfoides terciarios en el cerebro de pacientes con enfermedad progresiva. Además, el aumento de ILC3 similar a LTi se correlacionó con los autoanticuerpos en el líquido cerebral. [82]
Nuestra clasificación de ILC en subconjuntos proporciona un marco simplificado; sin embargo, a pesar del sistema de clasificación anterior, varios estudios sugieren que su desarrollo y mantenimiento fenotípico es mucho más complejo, con un alto nivel de plasticidad entre los subconjuntos. Los estudios han confirmado la capacidad de algunos subconjuntos de ILC para convertirse en un subconjunto diferente en presencia de citocinas específicas. [13] [47] Esta también es una característica común en las células T, y se cree que esta plasticidad es fundamental para permitir que nuestro sistema inmunológico sintonice las respuestas a tantos patógenos diferentes. [13] La plasticidad de ILC requiere receptores de citocinas, sus factores de transcripción y el acceso de regiones de cromatina definidas a los factores de transcripción; sin embargo, aún no está claro dónde se producen estas citocinas y dónde se produce la diferenciación in vivo. [6]

Las CLI presentes en pacientes con enfermedad pulmonar obstructiva crónica (EPOC) son un ejemplo prototípico de plasticidad de las CLI. Los estudios tanto en humanos como en ratones han demostrado que las ILC2 residentes en los pulmones adquieren un fenotipo ILC1 durante la EPOC, lo que aumenta la secreción de IFN-γ y, por lo tanto, la inflamación. [83] Varios desencadenantes, incluido el humo del cigarrillo, provocan la secreción de IL-12 e IL-18, lo que provoca la diferenciación de ILC2 en ILC1. GATA3 está regulado a la baja y la expresión de T-bet está regulada al alza. [83] Por lo tanto, los pacientes tienen una proporción de ILC1:ILC2 en sangre más alta, y la abundancia de ILC1 presentes se correlaciona con la gravedad de la enfermedad. [83]
La capacidad de las ILC3 para convertirse en células similares a ILC1 se ha demostrado in vitro e in vivo. [84] [85] [47] Cuando las ILC3 se cultivan con IL-2 e IL-15, se produce una regulación positiva de T-bet y del receptor de IL-12 (IL-12R) β2, lo que permite la conversión de ILC3. a las ILC1. Además, los estudios sugieren que la IL-23 puede promover la conversión de ILC1 en ILC3. [85]
Cada vez hay más pruebas que indican que las ILC2 también tienen un cierto grado de plasticidad, y los estudios confirman su capacidad para convertirse en ILC1 e ILC3 tras la exposición a estímulos ambientales específicos, como citoquinas o ligandos de muesca. [86] [47]
La señalización inducida por las citoquinas gobierna la plasticidad entre ILC3 e ILC1, induciendo la expresión de T-bet. En pacientes con enfermedad de Crohn, el aumento de ILC1 a expensas de ILC3 posiblemente se deba a la producción de IL-2 a partir de células T reguladoras, lo que conduce a un estado patogénico y eventos inflamatorios. Aunque la plasticidad es reversible, durante la diferenciación de NKp46+ ILC3 a ILC1, la modulación de la expresión de T-bet depende de IL-23, IL-2 e IL-1b y mejora con el ácido retinoico. Por tanto, la plasticidad de ILC3 a ILC1 depende de las células dendríticas que producen estas citocinas. Aunque la interconversión de ILC1 e ILC3 está modulada por la expresión diferencial de RORγt y T-bet, quedan diferentes preguntas que deben explicarse para comprender la inflamación causada por estas células. [87]
En el caso de ILC2, Gata3 puede regularse negativamente debido a la exposición a agentes infecciosos como el virus de la influenza, el virus respiratorio sincitial y Staphylococcus aureus, aumentando la expresión de IL12Rb2, IL-18Ra y T-bet. La diferenciación de ILC2 a ILC1 también puede ser reversible, aunque aún no se comprende el mecanismo. [87]
En determinados entornos, como inflamación, enfermedades crónicas o microambientes tumorales, las células NK activadas pueden comenzar a expresar CD49a y CXCR6 , marcadores ILC1 comunes, fortaleciendo sus propiedades plásticas. [88] [89]
Determinar el alcance de la plasticidad de las ILC durante la enfermedad podría ser útil para permitirnos prevenir o mejorar su conversión en otros subconjuntos que pueden estar contribuyendo a la patogenicidad. [47] [90]
Históricamente, la distinción entre el sistema inmunológico innato y adaptativo se centró en la naturaleza inespecífica y la falta de memoria del sistema innato. [91] A medida que ha surgido información sobre las funciones de las células NK y otras ILC como efectoras y orquestadoras de la respuesta inmune adaptativa, esta distinción se ha vuelto menos clara. Algunos investigadores sugieren que la definición debería centrarse más en la codificación de la línea germinal de los receptores del sistema inmunológico innato frente a los receptores reordenados del sistema inmunológico adaptativo. [74]